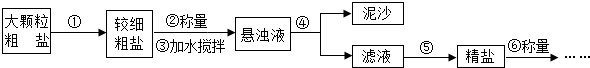
5.下列实验设计不能够成功的是( )
| 实验目的 | 实验操作 | |
| A | 实验室制备二氧化碳 | 将石灰石和稀盐酸混合 |
| B | 除去硫酸钠溶液中少量氯化钠杂质 | 向含有氯化钠杂质的硫酸钠溶液中加入适量的硝酸银溶液,过滤 |
| C | 除去氯化钠固体中的少量碳酸钠 | 加入过量的稀盐酸,充分反应后,蒸发 |
| D | 证明铁、铜、银的活动性强弱 | 向盛有少量的氯化亚铁、氯化银的两支试管中,分别加入大小相同的铜片 |
| A. | A | B. | B | C. | C | D. | D |
4.某工厂在装配一件设备时,不小心把一个用镁合金制造的精密空心小球(已知该小球的密度为1.60g/cm3)掉到一个又深、又小的坚固的水泥小洞中,用各种工具都取不出来,有人提出往小洞中倒入某种溶液使小球浮起的方法.现有三种物质的溶解度数据(注:水的密度为1g/cm3,溶液的体积变化忽略不计.).在保证不损坏小球的前提下,理论上可以用上表中物质配制成溶液,倒入小洞中使小球浮起,该溶液可以选择( )
| 物质 | 溶解度/克 | ||||
| 20℃ | 40℃ | 60℃ | 80℃ | 100℃ | |
| 硝酸铜 | 125.1 | 159.8 | 178.8 | 207.8 | 239.6 |
| 硝酸钾 | 31.6 | 64.0 | 110.0 | 169.0 | 246.0 |
| 氯化钾 | 34.0 | 40.0 | 45.0 | 51.1 | 56.7 |
| A. | 20℃的饱和硝酸铜溶液 | B. | 20℃的饱和硝酸钾溶液 | ||
| C. | 40℃的饱和硝酸钾溶液 | D. | 80℃的饱和氯化钾溶液 |
3.下列实验操作不正确的是( )
| A. | 实验后剩余的药品放回原试剂瓶内 | |
| B. | 电流表串联在电路中测通过电路的电流 | |
| C. | 做过滤实验时,滤纸低于漏斗边缘 | |
| D. | 显微镜实验时,环境中光线较暗选用凹面镜 |
20.一份溶质质量分数为8%的氯化钠溶液蒸发掉100g水后,其溶质质量分数变为24%,则原溶液中溶质的质量为( )
| A. | 4g | B. | 8g | C. | 12g | D. | 24g |
19. 溶解度曲线为我们定量描述物质的溶解性强弱提供了便利.请你根据如图的溶解度曲线判断下列说法,其中不正确的是( )
溶解度曲线为我们定量描述物质的溶解性强弱提供了便利.请你根据如图的溶解度曲线判断下列说法,其中不正确的是( )
 溶解度曲线为我们定量描述物质的溶解性强弱提供了便利.请你根据如图的溶解度曲线判断下列说法,其中不正确的是( )
溶解度曲线为我们定量描述物质的溶解性强弱提供了便利.请你根据如图的溶解度曲线判断下列说法,其中不正确的是( )| A. | 20℃时,甲物质的溶解度小于乙物质的溶解度 | |
| B. | 40℃时,两种物质溶解度相等 | |
| C. | 60℃时,将80g甲物质放入100g水中,所得溶液的质量为160g | |
| D. | 40℃时,甲、乙两种物质的溶质质量分数相等 |
18.除去下列各组物质中含有的杂质,所用试剂和方法均正确的是( )
| 物质(杂质) | 所以试剂和方法 | |
| A | H2(HCl气体) | 先通过NaOH溶液,再通过浓硫酸 |
| B | NaOH溶液Na2CO3溶液 | 加入过量的稀硫酸至不再产生气泡 |
| C | CaCO3粉末(NaCl粉末) | 加水溶解、过滤、蒸发 |
| D | CaO固体[Ca(OH)2固体] | 加入过量水,再过滤 |
| A. | A | B. | B | C. | C | D. | D |
17.下列图象能反映对应变化关系的是( )
0 166203 166211 166217 166221 166227 166229 166233 166239 166241 166247 166253 166257 166259 166263 166269 166271 166277 166281 166283 166287 166289 166293 166295 166297 166298 166299 166301 166302 166303 166305 166307 166311 166313 166317 166319 166323 166329 166331 166337 166341 166343 166347 166353 166359 166361 166367 166371 166373 166379 166383 166389 166397 211419
| A. | 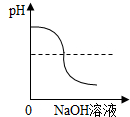 向一定量的稀硫酸中滴加氢氧化钠溶液至过量 | |
| B. | 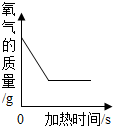 加热氯酸钾和二氧化锰混合物制氧气 | |
| C. |  将浓盐酸敞口放置在空气中 | |
| D. | 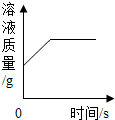 表示向足量的稀HCI中加入少量Fe,溶液质量与时间的关系图 |