题目内容
17.下列图象能反映对应变化关系的是( )| A. | 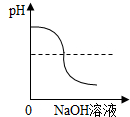 向一定量的稀硫酸中滴加氢氧化钠溶液至过量 | |
| B. | 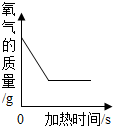 加热氯酸钾和二氧化锰混合物制氧气 | |
| C. |  将浓盐酸敞口放置在空气中 | |
| D. | 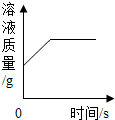 表示向足量的稀HCI中加入少量Fe,溶液质量与时间的关系图 |
分析 A、向一定量的稀硫酸中滴加氢氧化钠溶液至过量的过程中,是酸不断消耗酸性不断减弱,恰好反应时PH=7,直至过量PH大于7.
B、根据化学变化时生成物的质量增加;
C、根据浓盐酸具有挥发性,易挥发出溶质氯化氢,导致溶质质量分数降低进行解答;
D、稀HCl与Fe反应,溶液质量会增加,直到反应结束,溶液质量不再变化.
解答 解:A、稀硫酸呈酸性,故起初溶液的pH小于7,但随着氢氧化钠溶液的加入,会发生酸碱中和反应,使稀硫酸逐渐减少,酸性渐弱,两者恰好完全反应时溶液呈中性pH=7,继续加入氢氧化钠则碱加量,溶液呈碱性,图象相反,故错误;
B、随着反应的进行生成物的质量在增加,反应停止生成物的质量不变,故错误;
C、浓盐酸具有挥发性,易挥发出溶质氯化氢,导致溶质质量分数降低,而图象显示其质量分数增大,故错误;
D、稀HCl与Fe反应,溶液质量会增加,直到反应结束,溶液质量不再变化,正确
故选:D
点评 在处理图象类问题时,曲线的起点、折点及变化趋势是进行判断的要点.

练习册系列答案
相关题目
2.下列有关溶液的说法,不正确的是( )
| A. | 冷却或加入硝酸钾固体都能使接近饱和的硝酸钾溶液达到饱和 | |
| B. | 氨水是氨气的水溶液,根据气体溶解度的影响因素,贮存时要阴凉密封 | |
| C. | 在相同温度下,同种溶质的饱和溶液,一定比它的不饱和溶液的浓度大 | |
| D. | 氯化钠在20℃时的溶解度是36g,该温度时,100g饱和氯化钠溶液中含有氯化钠36g |
8.现有四瓶失去标签的无色溶液,分别是Ca(OH)2,KCl,Na2CO3,HCl溶液中的一种,已知甲可以和丙反应,也可以和丁反应.则下列说法中,正确的是( )
| A. | 甲不可能是KCl | B. | 丙不一定是Ca(OH)2 | C. | 乙可能是HCl | D. | 丁一定是Na2CO3 |
6. 玻璃钢如图所示,可以代替钢材制造机器零件和汽车、船舶外壳等.它是以玻璃纤维及其制品(玻璃布、带、毡、纱等)作为增强材料,以合成树脂作基体材料,玻璃钢属于( )
玻璃钢如图所示,可以代替钢材制造机器零件和汽车、船舶外壳等.它是以玻璃纤维及其制品(玻璃布、带、毡、纱等)作为增强材料,以合成树脂作基体材料,玻璃钢属于( )
 玻璃钢如图所示,可以代替钢材制造机器零件和汽车、船舶外壳等.它是以玻璃纤维及其制品(玻璃布、带、毡、纱等)作为增强材料,以合成树脂作基体材料,玻璃钢属于( )
玻璃钢如图所示,可以代替钢材制造机器零件和汽车、船舶外壳等.它是以玻璃纤维及其制品(玻璃布、带、毡、纱等)作为增强材料,以合成树脂作基体材料,玻璃钢属于( )| A. | 金属材料 | B. | 合成材料 | C. | 复合材料 | D. | 无机非金属材料 |
7.海水蕴藏着丰富的化学资源,目前世界60%的镁是从海水中提取的.其主要流程如图所示.某校兴趣小组同学对从海水中提取金属镁的过程进行了有关探究.
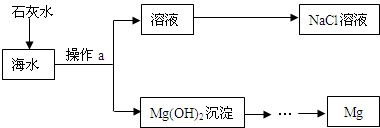
(1)在实验室进行操作a分离后的溶液(海水)中含有CaCl2等杂质,可向其中加入过量的Na2CO3(填化学式,后同)、适量的HCl,蒸发结晶,以除去CaCl2制得较为纯净的NaCl晶体.
(2)兴趣小组同学取一定量的海水样品,分别加入NaOH溶液,进行实验,测得的实验数据如表:
观察与分析上述数据,并计算
①海水样品中氯化镁的质量分数是多少?(计算结果精确到0.001%)
②若从1t这种海水中可提取多少千克金属镁?

(1)在实验室进行操作a分离后的溶液(海水)中含有CaCl2等杂质,可向其中加入过量的Na2CO3(填化学式,后同)、适量的HCl,蒸发结晶,以除去CaCl2制得较为纯净的NaCl晶体.
(2)兴趣小组同学取一定量的海水样品,分别加入NaOH溶液,进行实验,测得的实验数据如表:
| 实验1 | 实验2 | 实验3 | |
| 海水样品质量/g | 100 | 100 | 100 |
| 加入NaOH溶液质量/g | 10 | 15 | 20 |
| 生成沉淀物的质量/g | 0.22 | 0.29 | 0.29 |
①海水样品中氯化镁的质量分数是多少?(计算结果精确到0.001%)
②若从1t这种海水中可提取多少千克金属镁?
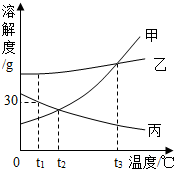 如图是甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题.
如图是甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题.