18.鉴别下列各组物质的方法中,不可行的是( )
| A. | 用水鉴别固体氯化钙和碳酸钙 | |
| B. | 用扇闻气味的方法鉴别白酒和白醋 | |
| C. | 用稀盐酸鉴别黄金和黄铜(锌铜合金) | |
| D. | 用碳酸钡鉴别硫酸钠溶液和氯化钠溶液 |
17.合理使用化肥,有利于农作物的生长和减少环境污染.下列有关化肥的说法正确的是( )
| A. | KNO3是一种常见的复合化肥 | |
| B. | 加熟石灰研磨能闻到刺激性气味的是磷肥的性质 | |
| C. | 氮肥、磷肥、钾肥三种化肥中,只有钾肥可溶于水 | |
| D. | 为保证高产应大量施用化肥 |
16.人体中骨骼与牙齿的重要成分是羟基磷酸钙[Ca10(PO4)6(OH)2],关于羟基磷酸钙的说法中正确的是( )
| A. | 羟基磷酸钙由5种元素组成 | |
| B. | 羟基磷酸钙的相对分子质量为104 | |
| C. | 羟基磷酸钙是一种有机物 | |
| D. | 根据羟基磷酸钙的化学式,推测其可与盐酸发生反应 |
15.关于碳和碳的化合物说法中,正确的是( )
| A. | 常温下,碳的化学性质活泼 | |
| B. | 金刚石和石墨的物理性质相似 | |
| C. | 在一定条件下CO2能够转变成CO | |
| D. | C和CO2都可以将CuO中的Cu还原出来 |
14.下列物质中,属于纯净物的是( )
| A. | 矿泉水 | B. | 氯酸钾 | C. | 稀盐酸 | D. | 生铁 |
12.实验室可利用碱式碳酸铜(化学式:Cu2(OH)2CO3)制备氧化铜,并进行碳粉还原氧化铜的实验.
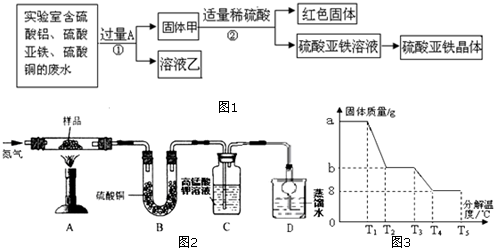
①制备氧化铜并检验产物,装置如图1所示(省略夹持仪器):已知烧碱可与二氧化碳反应,无水硫酸铜为白色固体可吸收水、变蓝.
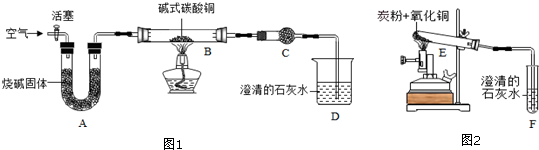
步骤一:连接A和B,打开活塞,通入空气.
步骤二:关闭活塞,连上C和D,开始加热.
步骤三:在加热过程中,记录在B中固体质量变化如下表,在t3时停止加热.
B中发生反应的化学方程式为:□Cu2(OH)2CO3═□CuO+□H2O+□CO2↑
请在□中填入配平后的系数,依次为1、2、1、1.C中试剂是无水硫酸铜 无水硫酸铜.A的作用是吸收空气中的水蒸气和二氧化碳 水蒸气和二氧化碳,防止对产物检验造成干扰.选择t3时停止加热的理由是固体质量不再减少,证明碱式碳酸铜已经完全分解
②一定量碳粉还原①中制得的氧化铜并检验产物,装置如图2所示:实验过程中,观察到F中溶液变浑浊,E中的现象是黑色粉末变成红色,反应完全后,若仅撤走酒精喷灯停止加热,可能导致的后果是F中的液体通过导管流入E中,造成试管炸裂
③分析:若①中省略步骤三,对②中反应产物判断可能产生的影响及其原因.不能确定炭粉还原氧化铜的生成物中是否含有二氧化碳.
因为可能有①中未分解的碱式碳酸铜在实验②中分解,产生二氧化碳气体,干扰对炭粉还原氧化铜反应生成物的判断.
①制备氧化铜并检验产物,装置如图1所示(省略夹持仪器):已知烧碱可与二氧化碳反应,无水硫酸铜为白色固体可吸收水、变蓝.

步骤一:连接A和B,打开活塞,通入空气.
步骤二:关闭活塞,连上C和D,开始加热.
步骤三:在加热过程中,记录在B中固体质量变化如下表,在t3时停止加热.
| 加热时间(min) | 0 | t1 | t2 | t3 |
| B中固体质量(g) | 6.66 | 5.20 | 4.80 | 4.80 |
请在□中填入配平后的系数,依次为1、2、1、1.C中试剂是无水硫酸铜 无水硫酸铜.A的作用是吸收空气中的水蒸气和二氧化碳 水蒸气和二氧化碳,防止对产物检验造成干扰.选择t3时停止加热的理由是固体质量不再减少,证明碱式碳酸铜已经完全分解
②一定量碳粉还原①中制得的氧化铜并检验产物,装置如图2所示:实验过程中,观察到F中溶液变浑浊,E中的现象是黑色粉末变成红色,反应完全后,若仅撤走酒精喷灯停止加热,可能导致的后果是F中的液体通过导管流入E中,造成试管炸裂
③分析:若①中省略步骤三,对②中反应产物判断可能产生的影响及其原因.不能确定炭粉还原氧化铜的生成物中是否含有二氧化碳.
因为可能有①中未分解的碱式碳酸铜在实验②中分解,产生二氧化碳气体,干扰对炭粉还原氧化铜反应生成物的判断.
9.小钢同学在家里用“除垢净”去除热水瓶中的水垢时,发现有大量的气泡产生.联想水垢的主要成分是碳酸钙,小钢猜想“除垢净”的成分中可能有酸.
(1)为证实自己的猜想,设计实验证明“除垢净”呈酸性,小明从家中找来如下试剂:光亮的铁钉、生锈的铁钉、纯碱溶液、蒸馏水.根据以上试剂,请你帮助他设计出两种不同实验方案,并写出实验现象,填入下表:
(2)小明想试制一瓶“除垢净”,你认为HCl、H2SO4两种酸中的HCl更合适,理由是硫酸与水垢反应生成微溶的硫酸钙,除垢不彻底.
(3)结合上面对“除垢净”的了解,在铝制水壶除垢时,使用“除垢净”应注意:去除铝壶中的水垢时,应控制“除垢净”的浓度,(或不要滴到手上或衣服上、防止腐蚀、除垢后要将“除垢净”冲洗干净等).
0 166075 166083 166089 166093 166099 166101 166105 166111 166113 166119 166125 166129 166131 166135 166141 166143 166149 166153 166155 166159 166161 166165 166167 166169 166170 166171 166173 166174 166175 166177 166179 166183 166185 166189 166191 166195 166201 166203 166209 166213 166215 166219 166225 166231 166233 166239 166243 166245 166251 166255 166261 166269 211419
(1)为证实自己的猜想,设计实验证明“除垢净”呈酸性,小明从家中找来如下试剂:光亮的铁钉、生锈的铁钉、纯碱溶液、蒸馏水.根据以上试剂,请你帮助他设计出两种不同实验方案,并写出实验现象,填入下表:
| 方案 | 具体操作 | 实验现象 | 结论 |
方案一 | “除垢净”中一定有酸 | ||
| 方案二 |
(3)结合上面对“除垢净”的了解,在铝制水壶除垢时,使用“除垢净”应注意:去除铝壶中的水垢时,应控制“除垢净”的浓度,(或不要滴到手上或衣服上、防止腐蚀、除垢后要将“除垢净”冲洗干净等).