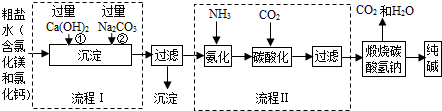
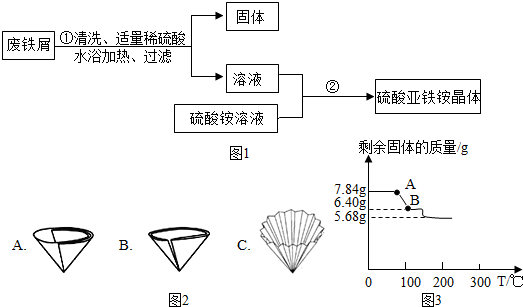
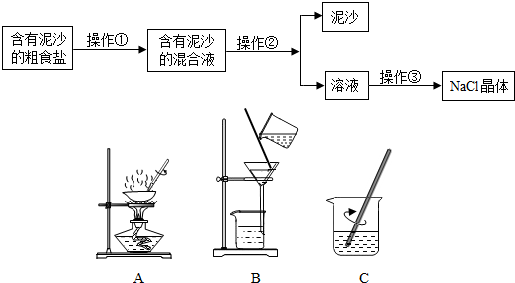
5.下列图象不能正确反映对应变化关系的是( )
| A. |  向一定量的二氧化锰中加入过氧化氢溶液 向一定量的二氧化锰中加入过氧化氢溶液 | |
| B. |  向稀盐酸中滴加氢氧化钠溶液 向稀盐酸中滴加氢氧化钠溶液 | |
| C. |  向两份完全相同的稀硫酸中分别加入Mg、Fe 向两份完全相同的稀硫酸中分别加入Mg、Fe | |
| D. |  将水通电一段时间 将水通电一段时间 |
3.地沟油中含有一种强烈致癌物黄曲霉素B2(C17H14O6),长期食用会引起消化道癌变,下列有关黄曲霉素B2的叙述,正确的是( )
| A. | 含有碳、氢、氧四种元素 | B. | .相对分子质量为247.5 g | ||
| C. | 属于有机化合物 | D. | .每个分子中含有27个原子 |
17.下列性质属于物理性质的是( )
0 166004 166012 166018 166022 166028 166030 166034 166040 166042 166048 166054 166058 166060 166064 166070 166072 166078 166082 166084 166088 166090 166094 166096 166098 166099 166100 166102 166103 166104 166106 166108 166112 166114 166118 166120 166124 166130 166132 166138 166142 166144 166148 166154 166160 166162 166168 166172 166174 166180 166184 166190 166198 211419
| A. | 沸点 | B. | 酸性 | C. | 可燃性 | D. | 毒性 |
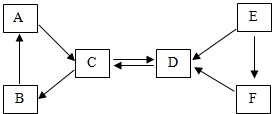 取A----F六种常见物质,其中A常用于改良酸性土壤,B是常用的固体干燥剂,A、B、C固体都含有同种金属元素,E是黑色固体单质,D、E、F都含有同种非金属元素,它们的转化关系如图所示,请回答:
取A----F六种常见物质,其中A常用于改良酸性土壤,B是常用的固体干燥剂,A、B、C固体都含有同种金属元素,E是黑色固体单质,D、E、F都含有同种非金属元素,它们的转化关系如图所示,请回答: