题目内容
4.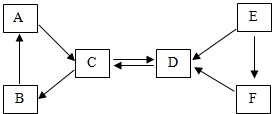 取A----F六种常见物质,其中A常用于改良酸性土壤,B是常用的固体干燥剂,A、B、C固体都含有同种金属元素,E是黑色固体单质,D、E、F都含有同种非金属元素,它们的转化关系如图所示,请回答:
取A----F六种常见物质,其中A常用于改良酸性土壤,B是常用的固体干燥剂,A、B、C固体都含有同种金属元素,E是黑色固体单质,D、E、F都含有同种非金属元素,它们的转化关系如图所示,请回答:(1)写出下列物质的化学式:
CCaCO3; FCO; EC;
(2)写出下列变化的化学方程式:
B→A:CaO+H2O=Ca(0H)2.
分析 由A常用于改良酸性土壤,B是食品包装中常用的干燥剂,可知A为氢氧化钙,B为氧化钙;A、B、C固体都含有同种金属元素结合转化关系图中A、B、C的转化关系,可推断C为碳酸钙;再由C(碳酸钙)、D两种物质相互转化的关系,可推断出D为二氧化碳;题中说明E为黑色固体单质,且D、E、F都含有同种非金属元素,根据关系图中D(二氧化碳)、E(单质)、F的转化关系,可以判断:E为单质C,F为一氧化碳,据此分析.
解答 解:由A常用于改良酸性土壤,B是食品包装中常用的干燥剂,可知A为氢氧化钙,B为氧化钙;A、B、C固体都含有同种金属元素结合转化关系图中A、B、C的转化关系,可推断C为碳酸钙;再由C(碳酸钙)、D两种物质相互转化的关系,可推断出D为二氧化碳;题中说明E为黑色固体单质,且D、E、F都含有同种非金属元素,根据关系图中D(二氧化碳)、E(单质)、F的转化关系,可以判断:E为单质C,F为一氧化碳,带入验证符合转化关系,因此:
(1)C是碳酸钙,F是一氧化碳,E是碳;故答案为:CaCO3;CO;C;
(2)B→A是氧化钙和水反应产生氢氧化钙,故反应的方程式为:CaO+H2O=Ca(0H)2.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
12.除去下表所列物质中含有的杂质,所选试剂及操作方法均正确的是( )
| 选项 | 物质 | 杂质 | 除去杂质所选试剂 | 操作方法 |
| A | 二氧化碳 | 一氧化碳 | 氧气 | 点燃 |
| B | 铜 | 氧化铜 | 氢气 | 加热 |
| C | 锌 | 铁 | 稀硫酸 | 过滤 |
| D | 氧化钙 | 碳酸钙 | 稀盐酸 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
9.下列说法中,正确的是( )
| A. | 纯净物一定由同种元素组成,混合物一定由不同种元素组成 | |
| B. | 铁丝在氧气中燃烧时有红色火焰产生 | |
| C. | 二氧化碳的密度比空气密度大,可以像倾倒液体一样由集气瓶倒进烧杯中 | |
| D. | 化学反应中的能量变化通常表现为热量的变化,如:镁和盐酸反应吸收热量,碳与二氧化碳反应放出热量 |
16.已知某种元素的原子核中含有1个质子和2个中子,那么( )
| A. | 该原子是一种氢原子 | B. | 该元素是金属元素 | ||
| C. | 该原子核外有2个电子 | D. | 该原子核带2个单位的正电荷 |
13.在反应2A+B=3C+D中,反应物的质量比为A:B=5:2.若完全反应后生成C和D共2.1g,则消耗反应物A为( )
| A. | 2.1g | B. | 1.5 g | C. | 1.05 g | D. | 0.6g |