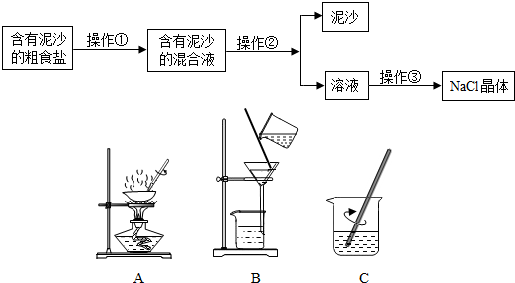
题目内容
3.地沟油中含有一种强烈致癌物黄曲霉素B2(C17H14O6),长期食用会引起消化道癌变,下列有关黄曲霉素B2的叙述,正确的是( )| A. | 含有碳、氢、氧四种元素 | B. | .相对分子质量为247.5 g | ||
| C. | 属于有机化合物 | D. | .每个分子中含有27个原子 |
分析 A、根据黄曲霉素的化学式进行分析判断.
B、根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析判断.
C、根据有机化合物的概念进行分析判断.
D、根据每个黄曲霉素分子的构成进行分析判断.
解答 解:A、黄曲霉素是由碳、氢、氧三种元素组成,故选项说法错误.
B、其相对分子质量为12×17+1×12+16×6=312,故选项说法错误.
C、黄曲霉素(化学式为C17H12O6)中含有碳元素,属于有机化合物,故选项说法正确.
D、每个黄曲霉素分子是由17个碳原子、12个氢原子、6个氧原子构成的,共37个原子,故选项说法错误.
故选:C.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
14.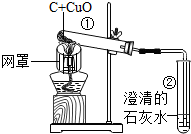 某化学兴趣小组按照如图装置进行木炭还原氧化铜的实验,很快发现试管①、试管②中分别出现黑色的粉末变成红色的粉末,澄清的石灰水变浑浊的现象.从而得到的结论是2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑、Ca(OH)2+CO2=CaCO3↓+H2O(用化学方程式表示).在对该实验进行总结时,大家对木炭还原氧化铜的最终产物产生的兴趣:碳还原氧化铜得到氧会不会生成CO?而CuO失去氧会不会生成Cu2O(氧化亚铜)?并为此进行了以下探究过程.
某化学兴趣小组按照如图装置进行木炭还原氧化铜的实验,很快发现试管①、试管②中分别出现黑色的粉末变成红色的粉末,澄清的石灰水变浑浊的现象.从而得到的结论是2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑、Ca(OH)2+CO2=CaCO3↓+H2O(用化学方程式表示).在对该实验进行总结时,大家对木炭还原氧化铜的最终产物产生的兴趣:碳还原氧化铜得到氧会不会生成CO?而CuO失去氧会不会生成Cu2O(氧化亚铜)?并为此进行了以下探究过程.
【查阅资料】
①红色固体不仅只有Cu,还有Cu2O
②Cu2O+H2SO4(稀)=Cu+CuSO4+H2O (CuSO4溶于水溶液呈蓝色)
③微量的CO气体能使湿润的黄色氯化钯试纸变蓝色.
【猜想】
(a)红色固体只有Cu,气体只有CO2.
(b)红色固体是Cu2O,气体是CO.
(c)红色固体是Cu和Cu2O的混合物,气体是CO2和CO的混合物
【探究步骤】
Ⅰ.兴趣小组首先对C和CuO反应的气体产物进行了探究.以下是他们进行实验的部分流程(装置气密性良好,浓硫酸起干燥作用):
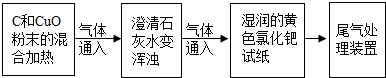
通过以上实验,观察到澄清石灰水变浑浊和湿润的黄色氯化钯试纸变蓝色的现象,说明气体产物是CO2和CO的混合物.
Ⅱ.首先对C和CuO反应的固体产物进行了探究.以下是他们进行实验后的实验报告,请你仔细阅读后完成相关的报告内容
 某化学兴趣小组按照如图装置进行木炭还原氧化铜的实验,很快发现试管①、试管②中分别出现黑色的粉末变成红色的粉末,澄清的石灰水变浑浊的现象.从而得到的结论是2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑、Ca(OH)2+CO2=CaCO3↓+H2O(用化学方程式表示).在对该实验进行总结时,大家对木炭还原氧化铜的最终产物产生的兴趣:碳还原氧化铜得到氧会不会生成CO?而CuO失去氧会不会生成Cu2O(氧化亚铜)?并为此进行了以下探究过程.
某化学兴趣小组按照如图装置进行木炭还原氧化铜的实验,很快发现试管①、试管②中分别出现黑色的粉末变成红色的粉末,澄清的石灰水变浑浊的现象.从而得到的结论是2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑、Ca(OH)2+CO2=CaCO3↓+H2O(用化学方程式表示).在对该实验进行总结时,大家对木炭还原氧化铜的最终产物产生的兴趣:碳还原氧化铜得到氧会不会生成CO?而CuO失去氧会不会生成Cu2O(氧化亚铜)?并为此进行了以下探究过程.【查阅资料】
①红色固体不仅只有Cu,还有Cu2O
②Cu2O+H2SO4(稀)=Cu+CuSO4+H2O (CuSO4溶于水溶液呈蓝色)
③微量的CO气体能使湿润的黄色氯化钯试纸变蓝色.
【猜想】
(a)红色固体只有Cu,气体只有CO2.
(b)红色固体是Cu2O,气体是CO.
(c)红色固体是Cu和Cu2O的混合物,气体是CO2和CO的混合物
【探究步骤】
Ⅰ.兴趣小组首先对C和CuO反应的气体产物进行了探究.以下是他们进行实验的部分流程(装置气密性良好,浓硫酸起干燥作用):

通过以上实验,观察到澄清石灰水变浑浊和湿润的黄色氯化钯试纸变蓝色的现象,说明气体产物是CO2和CO的混合物.
Ⅱ.首先对C和CuO反应的固体产物进行了探究.以下是他们进行实验后的实验报告,请你仔细阅读后完成相关的报告内容
| 实 验 操 作 | 实 验 现 象 | 实 验 结 论 |
| 取7.2g红色固体,置于烧杯中,向其中加入足量稀硫酸,充分搅拌,静置. | 若无现象. | 证明红色固体是铜. |
| 若有无色变成蓝色, 且有不溶物现象. | 证明红色固体肯定含有氧化亚铜,可能含有铜. | |
| 取上述反应液过滤、洗涤、干燥和称量,得固体6.8g. | 确认红色固体是铜和氧化亚铜.(写出详尽的计算过程) |
11.某化学兴趣小组的学生,发现金属R不在初中学到的金属活动性顺序表中,该小组为了了解R与常见金属铝、铜的金属活动性顺序,进行如下探究活动:
【作出猜想】他们考虑到铝的活动性比铜强,对三种金属的活动性顺序作出如下猜想:
猜想一:Al>Cu>R,猜想二:Al>R>Cu,猜想三:R>Al>Cu,
【查阅资料】R是一种银白色的金属,在R的盐溶液中只有+2价R的盐溶液呈蓝色,常温下铝的表面会形成一层致密的氧化膜;硫酸铝、氯化铝、硝酸铝的溶液均为无色.
【实验探究】为了探究哪一种猜想成立,甲、乙、丙三位同学分别针对猜想一、猜想二、猜想三设计实验方案并展开实验探究.
【交流反思】
究竟哪种猜想成立?三位同学经讨论交流,发现丙同学在实验前没有打磨铝丝,这可能会导致实验结论错误.于是他们先打磨铝丝,再将其插入到丙同学做实验用过的溶液中,一段时间后,溶液的颜色由蓝色变成无色;进而确认猜想三不成立,猜想二成立.
【归纳总结】探究结束后,他们总结得出:通过金属与酸反应或金属与盐溶液反应可以比较金属活动性强弱.
【作出猜想】他们考虑到铝的活动性比铜强,对三种金属的活动性顺序作出如下猜想:
猜想一:Al>Cu>R,猜想二:Al>R>Cu,猜想三:R>Al>Cu,
【查阅资料】R是一种银白色的金属,在R的盐溶液中只有+2价R的盐溶液呈蓝色,常温下铝的表面会形成一层致密的氧化膜;硫酸铝、氯化铝、硝酸铝的溶液均为无色.
【实验探究】为了探究哪一种猜想成立,甲、乙、丙三位同学分别针对猜想一、猜想二、猜想三设计实验方案并展开实验探究.
| 猜想 | 主要操作 | 主要现象 | 实验结论 |
| 猜想一 | 打磨R丝,并将其插入到硫酸铜溶液中 | R丝表面覆盖了一层红色的物质 | 猜想一不成立(填“成立”或“不成立”) |
| 猜想二 | 打磨粗细相同的R丝、铝丝、铜丝,分别将它们插入到体积相同、溶质质量分数也相同的稀硫酸中 | ①R丝表面产生气泡缓慢,溶液由无色逐渐变成蓝色 ②铝丝表面产生气泡较快 ③铜丝表面没有气泡产生 | 猜想二成立. R与稀硫酸反应的化学方程式为 R+H2SO4=RSO4+H2↑ |
| 猜想三 | 将打磨过的铝丝,插入到RSO4溶液中 | 无明显现象 | 猜想三成立 |
究竟哪种猜想成立?三位同学经讨论交流,发现丙同学在实验前没有打磨铝丝,这可能会导致实验结论错误.于是他们先打磨铝丝,再将其插入到丙同学做实验用过的溶液中,一段时间后,溶液的颜色由蓝色变成无色;进而确认猜想三不成立,猜想二成立.
【归纳总结】探究结束后,他们总结得出:通过金属与酸反应或金属与盐溶液反应可以比较金属活动性强弱.
8.我国2008年举办第29届夏季奥运会,主题是“绿色奥运、科技奥运、人文奥运”;口号是“同一个世界,同一个梦想”.自第十一届奥运会以来,历届奥运会开幕式都要进行颇为隆重的“火炬接力”.火炬的燃料是丁烷(化学式C4H10),它燃烧时,火苗高且亮.下列关于丁烷的叙述正确的是( )
①丁烷是由碳、氢两种元素组成的 ②丁烷由碳和氢两种原子构成的
③丁烷分子是由碳、氢两种元素构成的 ④丁烷中碳、氢元素的质量比为2:5
⑤丁烷分子是由碳原子和氢原子构成的 ⑥丁烷是由4个碳原子和10个氢原子组成的
⑦丁烷氢元素的质量分数约为17.2% ⑧丁烷由丁烷分子构成.
①丁烷是由碳、氢两种元素组成的 ②丁烷由碳和氢两种原子构成的
③丁烷分子是由碳、氢两种元素构成的 ④丁烷中碳、氢元素的质量比为2:5
⑤丁烷分子是由碳原子和氢原子构成的 ⑥丁烷是由4个碳原子和10个氢原子组成的
⑦丁烷氢元素的质量分数约为17.2% ⑧丁烷由丁烷分子构成.
| A. | ①②③④⑤⑥⑦⑧ | B. | ①⑤⑦⑧ | C. | ②③④⑤⑦⑧ | D. | ①②④⑤⑦⑧ |
15.下列物质的用途主要利用其化学性质的是( )
| A. | 用铝制做铝锅 | B. | 酒精做溶剂 | ||
| C. | 用l 6%的食盐水选种 | D. | 氧气供给呼吸 |
12.下列物质中,前者为单质.后者为氧化物的是( )
| A. | 液氧 冰 | B. | 冰 高锰酸钾 | C. | 白磷 空气 | D. | 过氧化氢 氧化镁 |
13.把一定质量的a,b,c,d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应前后各物质的质量如下表所示,下列说法中正确的是( )
| 物质 | a | b | c | d |
| 反应前的质量(g) | 6.4 | 3.2 | 4.0 | 2.8 |
| 反应后的质量(g) | 5.2 | X | 7.2 | 2.8 |
| A. | a和c是反应物 | B. | d一定是催化剂 | ||
| C. | X=2.0g | D. | 参加反应的a和b的质量比为3:5 |
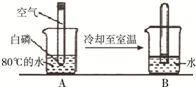 如图装置可用来测定空气中氧气的含量.针对该实验描述不正确的是B.
如图装置可用来测定空气中氧气的含量.针对该实验描述不正确的是B.