12.人体中某些化学元素含量会直接影响人体健康.下列人体所缺元素与引起的健康问题关系错误的是( )
| A. | 缺碘会引起高血压 | B. | 缺铁会引起贫血 | ||
| C. | 缺钙会引起骨质疏松 | D. | 缺锌会引起发育停滞、智力低下 |
11.生活中一些常见物质的pH如图,下列四种物质中酸碱性与众不同的是( )
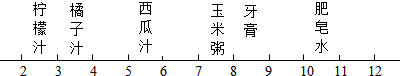

| A. | 肥皂水 | B. | 牙膏 | C. | 西瓜汁 | D. | 玉米粥 |
10.柴静《雾霾调查:穹顶之下》提到雾霾天气,其主要成因是空气中的烟、灰尘等物质,对人体健康有伤害.下列做法不会加剧雾霾天气形成的是( )
| A. | 燃放鞭炮 | B. | 城市绿化 | C. | 露天焚烧垃圾 | D. | 工厂排放烟尘 |
8.“海水晒盐”所获得的粗盐中,除含有泥沙等难溶性杂质外,还含有氯化镁、氯化钙等可溶性杂质,某化学小组为得到较纯净的食盐,进行了下列实验探究活动,请参与他们的探究活动:

【提出问题】如何获得较纯的食盐晶体?
【查阅资料】20℃时,部分物质的溶解性情况如表所示:
【实验方案】按如图方案进行提纯粗盐.
【解释与结论】
(1)操作X的名称是过滤.
(2)沉淀D是碳酸钙.
(3)实验步骤③的主要目的是MgCl2+2NaOH=Mg(OH)2↓+2NaCl (用化学方程式回答);判断氢氧化钠溶液已过量的方法是取溶液B少量于试管中,滴加无色酚酞试液,酚酞试液变红色.
【反思与评价】
(4)有同学认为该实验方案并不完善,其理由及需补充的实验操作是溶液C中还有过量的碳酸钠和氢氧化钠,应该加入适量的稀盐酸反应后再蒸发.

【提出问题】如何获得较纯的食盐晶体?
【查阅资料】20℃时,部分物质的溶解性情况如表所示:
| OH- | CO32- | |
| Na+ | 溶 | 溶 |
| Ca2+ | 微 | 不 |
| Mg2+ | 不 | 微 |
【解释与结论】
(1)操作X的名称是过滤.
(2)沉淀D是碳酸钙.
(3)实验步骤③的主要目的是MgCl2+2NaOH=Mg(OH)2↓+2NaCl (用化学方程式回答);判断氢氧化钠溶液已过量的方法是取溶液B少量于试管中,滴加无色酚酞试液,酚酞试液变红色.
【反思与评价】
(4)有同学认为该实验方案并不完善,其理由及需补充的实验操作是溶液C中还有过量的碳酸钠和氢氧化钠,应该加入适量的稀盐酸反应后再蒸发.
5.甲乙是某同学设计的两套制取二氧化碳的发生装置,对两套装置分析不正确的是( )
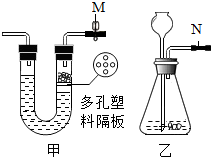

| A. | 此时甲装置中的止水夹M处于关闭状态 | |
| B. | 甲装置具有控制反应的开始与结束的功能 | |
| C. | 乙装置的长颈漏斗下端一定要伸入液体中起液封作用 | |
| D. | 乙装置N处添加止水夹可以与甲装置具有相同功能 |
4.日常生活中有很多问题都涉及化学知识,下列说法正确的是( )
0 163741 163749 163755 163759 163765 163767 163771 163777 163779 163785 163791 163795 163797 163801 163807 163809 163815 163819 163821 163825 163827 163831 163833 163835 163836 163837 163839 163840 163841 163843 163845 163849 163851 163855 163857 163861 163867 163869 163875 163879 163881 163885 163891 163897 163899 163905 163909 163911 163917 163921 163927 163935 211419
| A. | 将废弃塑料切成碎片,混在垃圾中填埋于土壤中以减少对环境的污染 | |
| B. | 青少年长期饮用纯净水有益于身体健康 | |
| C. | 为了降低生产成本,可用工业酒精勾兑饮用酒 | |
| D. | 导致骨质疏松的主要原因是人体骨中缺少钙 |
 随着生活水平的提高,人们对水的质量提出了更高的要求.
随着生活水平的提高,人们对水的质量提出了更高的要求.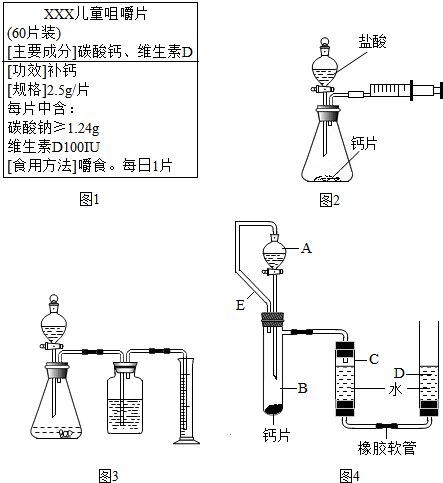

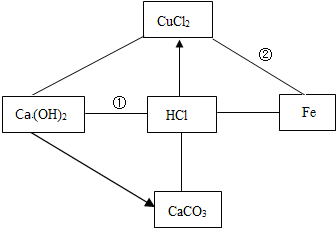 构建知识网络是一种重要的学习方法.如图是关于盐酸化学性质的相关知识,“-”表示相连的两种物质(或溶液)间能发生反应,“→”表示一种物质转化成另一种物质.请回答下面的问题:
构建知识网络是一种重要的学习方法.如图是关于盐酸化学性质的相关知识,“-”表示相连的两种物质(或溶液)间能发生反应,“→”表示一种物质转化成另一种物质.请回答下面的问题: