题目内容
9.如图1为“хх”钙片商品标签图,请根据标签的有关信息完成下列各题.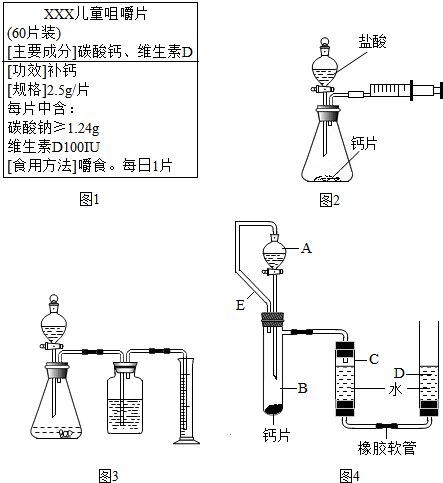
该钙片主要成分碳酸钙,碳酸钙的相对分子质量为 ①100.
某校化学兴趣小组为了确认标签中碳酸钙的含量是否真实,决定通过实验进行探究.
实验目标:测定该钙片主要成分碳酸钙的含量.
实验原理:取一定质量的钙片与足量的稀盐酸反应,测量生成的CO2的质量(已知该状态下CO2的密度),然后计算其中碳元素的质量,利用反应前后碳元素的质量不变,再计算出碳酸钙的质量.
实验方案:兴趣小组的同学们经过思考提出了以下几种实验方案,请你参与他们对实验方案的讨论、取舍.
方案一:甲同学设计了如图2所示的装置,通过反应后右侧注射器(注射器最大量程为20mL)内收集到气体的量来进行计算.
(1)同学们观看了他的设计后,都认为该方案中样品的取用的量需要一定的控制,这是因为样品过多水,产生的气体过多会导致注射器活塞被顶出;取样过少时,产生气体太少会导致误差过大.
(2)同学们讨论后,一致认为注射器的摩擦会影响生成的CO2的完全收集.
方案二:乙同学设计了如图3所示的装置,与甲同学的相比,仅仅在收集方法上不同.
(1)同学们观看了他的设计后,都认为所测得CO2气体的体积将会①偏小(填偏大或偏小),你认为他们的理由是②会有部分二氧化碳溶解在水中,你的改进方案是③在水面上滴一层植物油;广口瓶内原有的空气对实验结果④没有(填“有”或“没有”)影响.
(2)同学们讨论后,一致认为把装置改进后测得生成的CO2气体体积会偏大,你认为他们的最主要理由是滴入的盐酸有一定的体积,导致测定的气体体积偏大.
方案三:丙同学设计了如图4所示的装置.同学们观看后一致认可他的设计,并按照他的思路设计了以下实验步骤.
实验步骤:
①连接装置并检查装置气密性;
②加入10片钙片和水;
③记录C中液面刻度(C为带有刻度的玻璃管);
④由A向B中滴加稀盐酸至过量;
⑤待B中不再有气体产生并恢复至室温后,记录C中液面刻度,计算得到气体的体积为V mL(经查,该气体密度为ρg/L);
⑥计算气体的质量.
实验反思:
(1)丙同学在实验前将钙片全磨成粉末状,你认为他的目的是:使样品中的碳酸钙完全反应,同时能够加快反应速率;
(2)检查该装置的气密性时,如图准备好装置,在C、D两管中装好水且液面相平,提高D管,液面静止后,C、D液面存在高度差,则气密性良好;
(3)实验结论:经多次实验(钙片都是10片),所得CO2气体的平均质量是6.82g,请你最后计算确认标签中碳酸钙的含量是真实(填“真实”或“不真实”)的.(最后一空不需要写计算过程)
分析 根据碳酸钙的化学式可以计算碳酸钙的相对分子质量;
生成二氧化碳的质量决定于药品的质量;
二氧化碳能够溶于水,不溶于植物油;
反应物接触越充分,反应速率越快;
凡是有气体参加或产生的实验,实验前一定要检查装置的气密性,以防装置漏气影响实验结果;
通过提供的数据减小计算,可以判断标签中碳酸钙的含量是否属实.
解答 解:碳酸钙的化学式是CaCO3,相对分子质量为:40+12+(16×3)=100;
方案一:
(1)因为样品过多水,产生的气体过多会导致注射器活塞被顶出;取样过少时,产生气体太少会导致误差过大,因此样品的取用的量需要一定的控制;
方案二:
(1)因为二氧化碳能够溶于水,因此会有部分二氧化碳溶解在水中,导致所测得CO2气体的体积偏小;
改进方案是:在水面上滴一层植物油;
因为有多少体积的二氧化碳进入盛有水和植物油的试剂瓶中时,就会有多少体积的水排出试剂瓶进入量筒中,因此植物油上方原有的空气对测量结果无明显影响;
(2)滴入的盐酸有一定的体积,导致测定的气体体积偏大;
实验反思:
(1)丙同学在实验前将钙片全磨成粉末状,目的是使样品中的碳酸钙完全反应,同时能够加快反应速率;
(2)检查该装置的气密性时,如图准备好装置,在C、D两管中装好水且液面相平,提高D管,液面静止后,C、D液面存在高度差,则气密性良好;
(3)设1片钙片中碳酸钙的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 44
x 0.682g
$\frac{100}{x}$=$\frac{44}{0.682g}$,
x=1.55g,
标签中碳酸钙的含量是真实的.
故填:100;样品过多水,产生的气体过多会导致注射器活塞被顶出;取样过少时,产生气体太少会导致误差过大;偏小;会有部分二氧化碳溶解在水中;在水面上滴一层植物油;没有;滴入的盐酸有一定的体积,导致测定的气体体积偏大;使样品中的碳酸钙完全反应,同时能够加快反应速率;液面静止后,C、D液面存在高度差;真实.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

 阅读快车系列答案
阅读快车系列答案| A. | 将废弃塑料切成碎片,混在垃圾中填埋于土壤中以减少对环境的污染 | |
| B. | 青少年长期饮用纯净水有益于身体健康 | |
| C. | 为了降低生产成本,可用工业酒精勾兑饮用酒 | |
| D. | 导致骨质疏松的主要原因是人体骨中缺少钙 |
| A. | 啤酒 | B. | 碳酸钙 | C. | 加碘食盐 | D. | 食醋 |
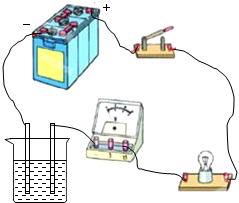 为了研究溶液的导电能力与什么因素有关,某同学设计了如图的一个实验方案,并实验得到了如下表的数据:(已知纯水和沉淀物不导电)
为了研究溶液的导电能力与什么因素有关,某同学设计了如图的一个实验方案,并实验得到了如下表的数据:(已知纯水和沉淀物不导电)  | 2% | 3% | 4% |
| Ca(NO3)2溶液 | 0.09A | 0.14A | 0.18A |
| Ba(OH)2溶液 | 0.06A | 0.09A | 0.11A |
(2)你从实验数据分析可以得出,溶液的导电能力与溶质的种类、溶质质量分数的大小有关;
(3)用胶头滴管不断往氢氧化钡溶液中滴加硫酸溶液,实验中可以观察到灯泡亮度如何改变呢?逐渐变暗,然后熄灭,最后又逐渐变亮.

 水是最常见的物质之一.
水是最常见的物质之一.