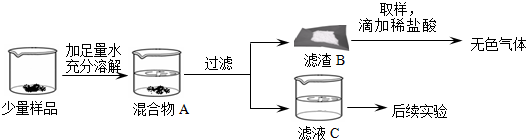
题目内容
6.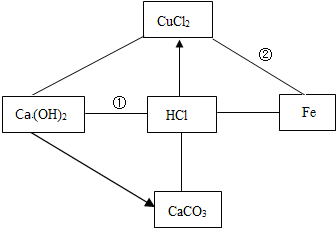 构建知识网络是一种重要的学习方法.如图是关于盐酸化学性质的相关知识,“-”表示相连的两种物质(或溶液)间能发生反应,“→”表示一种物质转化成另一种物质.请回答下面的问题:
构建知识网络是一种重要的学习方法.如图是关于盐酸化学性质的相关知识,“-”表示相连的两种物质(或溶液)间能发生反应,“→”表示一种物质转化成另一种物质.请回答下面的问题:(1)请写出反应①的化学方程式Ca(OH)2+2HCl═CaCl2+2H2O,基本反应类型复分解反应.
(2)反应②的化学方程式Fe+CuCl2=FeCl2+Cu.基本反应类型置换反应.
(3)Ca(OH)2变成CaCO3的化学方程式CO2+Ca(OH)2═CaCO3↓+H2O或Ca(OH)2+Na2CO3═CaCO3↓+2NaOH等合理即可.
分析 (1)根据酸碱的化学性质写出Ca(OH)2和HCl反应的化学方程式,判断反应类型;
(2)根据铁和氯化铜反应产生氯化亚铁和铜,写出反应的方程式并判断反应类型;
(3)根据复分解反应发生的条件结合氢氧化钙的化学性质写出反应的方程式.
解答 解:(1)Ca(OH)2和HCl反应产生氯化钙和水,反应的化学方程式为:Ca(OH)2+2HCl═CaCl2+2H2O,此反应是两种化合物相互交换成分生成两种化合物的复分解反应;故答案为:Ca(OH)2+2HCl═CaCl2+2H2O;复分解反应;
(2)反应②是铁和氯化铜反应产生氯化亚铁和铜,反应的方程式为:Fe+CuCl2=FeCl2+Cu;,该反应是单质和化合物反应产生单质和化合物的置换反应;故答案为:Fe+CuCl2=FeCl2+Cu;置换反应;
(3)Ca(OH)2变成CaCO3可以是氢氧化钙和二氧化碳或碳酸钠的反应,故反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O或Ca(OH)2+Na2CO3═CaCO3↓+2NaOH等合理即可.
点评 本题考查了有关酸、碱、盐的化学性质,解答此类题要求同学们在平时的学习过程中,要学会知识的综合应用,才能准确的写出符合题意的答案.

练习册系列答案
相关题目
14.以下关于物质构成的说法中不正确的是( )
| A. | 氯化钠是由钠离子和氯离子构成的 | B. | 汞是由汞原子构成的 | ||
| C. | 干冰是由碳原子和氧原子构成的 | D. | 金刚石是由碳原子构成的 |
11.生活中一些常见物质的pH如图,下列四种物质中酸碱性与众不同的是( )
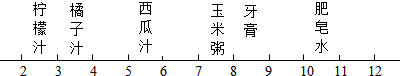

| A. | 肥皂水 | B. | 牙膏 | C. | 西瓜汁 | D. | 玉米粥 |
18.某密闭容器中含有氢气和氧气的混合气体共10g,燃烧后充分反应,冷却到室温,气体质量减少了9g,则原混合气体中氢气和氧气的质量为( )
| A. | 1g和9g | B. | 3g和7g | C. | 2g和8g | D. | 4g和6g |
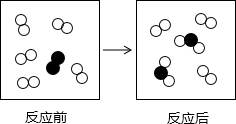 如图是某个化学反应前、后的微观模拟图,请根据图示回答:
如图是某个化学反应前、后的微观模拟图,请根据图示回答: 和
和 与反应后生成的
与反应后生成的 各粒子间的个数比为2:1:2;
各粒子间的个数比为2:1:2;