6.一包由CuSO4、CaCO3、BaCl2、Na2SO4、NaOH中的两种或两种以上的物质混合而成.取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液X.在滤出的白色沉淀中加入足量的盐酸,沉淀全部溶解,并产生无色气体.下列判断错误的是( )
| A. | 原白色粉末的组成有3组可能 | |
| B. | 原白色粉末中一定含有CaCO3 | |
| C. | 原白色粉末中一定不含有CuSO4 | |
| D. | 若向无色滤液X中通入二氧化碳,产生白色沉淀,则可推断原白色粉末中一定还含有BaCl2、NaOH |
4.某溶液中存在Mg2+、Ag+、Ba2+三种阳离子,现用NaOH,Na2CO3和NaCl三种溶液使它们转化为沉淀并分离出来,要求每次只加一种溶液,滤出一种沉淀,则所加溶液的顺序正确的是( )
| A. | NaCl、NaOH、Na2CO3 | B. | Na2CO3、NaCl、NaOH | ||
| C. | NaOH、NaCl、Na2CO3 | D. | NaCl、Na2CO3、NaOH |
3.除去铜粉中混有的少量氧化铜,其主要操作过程是( )
| A. | 加入过量浓H2SO4微热后,过滤,洗涤 | |
| B. | 加强热或在空气中灼热 | |
| C. | 加适量水,加热,过滤,洗涤 | |
| D. | 加适量稀H2SO4,微热,过滤,洗涤 |
2.四位同学检验某瓶无色溶液中所含的离子得出四种不同的结论,其中可能正确的是( )
| A. | K+、Na+、CO32-、H+ | B. | Ba2+、Na+、NO3-、SO42- | ||
| C. | H+、Ba2+、NO3-、Cl- | D. | OH-、K+、H+、Cl- |
1.过氧化氢溶液长期保存会自然分解,使得溶质质量分数减小.小佑从家中拿来一瓶久置的医用过氧化氢溶液,和同学们一起测定其中过氧化氢的质量分数.他们取出该溶液100g,加入适量二氧化锰,生成气体的质量与反应时间的关系如表所示.
(1)完全反应后生成氧气的质量为3.2 g.
(2)计算小佑家的过氧化氢溶液的质量分数.
| 时间 | t1 | t2 | t3 | t4 | t5 |
| 生成气体的质量/g | 0.9 | 1.8 | 2.7 | 3.2 | 3.2 |
(2)计算小佑家的过氧化氢溶液的质量分数.
19.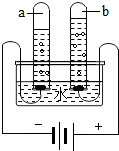 小左做完电解水后的装置情况如图所示.关于本次实验,以下说法不正确的是( )
小左做完电解水后的装置情况如图所示.关于本次实验,以下说法不正确的是( )
0 162951 162959 162965 162969 162975 162977 162981 162987 162989 162995 163001 163005 163007 163011 163017 163019 163025 163029 163031 163035 163037 163041 163043 163045 163046 163047 163049 163050 163051 163053 163055 163059 163061 163065 163067 163071 163077 163079 163085 163089 163091 163095 163101 163107 163109 163115 163119 163121 163127 163131 163137 163145 211419
 小左做完电解水后的装置情况如图所示.关于本次实验,以下说法不正确的是( )
小左做完电解水后的装置情况如图所示.关于本次实验,以下说法不正确的是( )| A. | a试管中收集到的气体是氢气 | |
| B. | 可以用带火星的木条检验b试管中收集的气体 | |
| C. | a、b两支试管中所收集气体的质量比为2:1 | |
| D. | 该实验可以证明水中含有氢氧两种元素 |

 有一不纯的白色固体氯化镁中含有少量氯化钠.化学兴趣小组的同学为了测定该固体氯化镁中氯化钠的质量分数.进行了以下实验:称量10g样品置于烧杯中,向其中加入90g水,搅拌,使其完全溶解为止.然后取该溶液一半,往其中滴加10%的氢氧化钠溶液,产生沉淀的质量与所滴入氢氧化钠溶液的质量关系曲线如图所示.
有一不纯的白色固体氯化镁中含有少量氯化钠.化学兴趣小组的同学为了测定该固体氯化镁中氯化钠的质量分数.进行了以下实验:称量10g样品置于烧杯中,向其中加入90g水,搅拌,使其完全溶解为止.然后取该溶液一半,往其中滴加10%的氢氧化钠溶液,产生沉淀的质量与所滴入氢氧化钠溶液的质量关系曲线如图所示. 如图是A、B、C三种物质的溶解度曲线,根据图回答下列问题:
如图是A、B、C三种物质的溶解度曲线,根据图回答下列问题: