题目内容
8.实验室中的试剂一般要密封保存,否则可能会与空气接触而变质.某研究性学习小组发现一瓶未密闭的KOH固体,对其成分提出以下假设,并完成了实验探究.假设1:只含KOH; 假设2:含KOH和K2CO3; 假设3:只含K2CO3
(1)成分中可能含有K2CO3的原因是(用化学方程式回答)2KOH+CO2═K2CO3+H2O.
(2)取少量样品于试管中,加入足量稀盐酸,观察到有气泡产生,说明假设2
或假设3成立.
(3)进一步探究的过程如下:

①操作1”的名称是过滤,固体A的成份是CaCO3(填化学式).
②加入足量CaCl2溶液的作用是使碳酸钾完全反应,防止对接下来的实验产生干扰.
③溶液B中滴加酚酞试液,若观察到酚酞试液变红色现象,假设2成立.
分析 (1)氢氧化钾能够吸收空气中的二氧化碳,并且能够反应生成碳酸钾和水;
(2)碳酸钾能和稀盐酸反应生成氯化钠、水和二氧化碳;
(3)①过滤可以把不溶于水的物质除去;
②氯化钙和碳酸钾反应能生成碳酸钙沉淀和氯化钾;
③氢氧化钾水溶液显碱性,能够使酚酞试液变红色.
解答 解:(1)成分中可能含有K2CO3的原因是:氢氧化钾和二氧化碳发生反应生成碳酸钾和水,化学方程式为:2KOH+CO2═K2CO3+H2O.
故填:2KOH+CO2═K2CO3+H2O.
(2)取少量样品于试管中,加入足量稀盐酸,如果观察到有气泡产生,说明样品中含有碳酸钾,说明假设2或假设3成立.
故填:有气泡产生.
(3)①操作1的名称是过滤,可以把反应生成的碳酸钙分离出来.由于碳酸钾和绿环该反应生成了碳酸钙沉淀和氢氧化钾,所以固体A是碳酸钙,碳酸钙的化学式是CaCO3.故填:过滤;CaCO3.
②为了排除碳酸钾对实验结果的影响,应该加入足量CaCl2溶液把碳酸钾除去;故填:使碳酸钾完全反应,防止对接下来的实验产生干扰.
③如果向溶液B中滴加酚酞试液时,酚酞试液变红色,说明样品中含有氢氧化钾.故填:酚酞试液变红色.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
18.为区别稀盐酸和稀硫酸,最好选用下列哪种试剂( )
| A. | 石蕊试液 | B. | 碳酸钠溶液 | C. | 氯化钡溶液 | D. | 酚酞试液 |
19. 暖宝宝中的发热剂是铁粉、水和食盐等,发热剂能代替红磷测定空气中氧气含量(装置见图).以下对此改进实验的叙述,错误的是( )
暖宝宝中的发热剂是铁粉、水和食盐等,发热剂能代替红磷测定空气中氧气含量(装置见图).以下对此改进实验的叙述,错误的是( )
 暖宝宝中的发热剂是铁粉、水和食盐等,发热剂能代替红磷测定空气中氧气含量(装置见图).以下对此改进实验的叙述,错误的是( )
暖宝宝中的发热剂是铁粉、水和食盐等,发热剂能代替红磷测定空气中氧气含量(装置见图).以下对此改进实验的叙述,错误的是( )| A. | 此实验的原理是利用铁生锈消耗氧气 | |
| B. | 实验前一定要检查装置的气密性 | |
| C. | 此实验中发热剂的量可能取少了 | |
| D. | 此实验测出氧气的质量分数约是18.3% |
3.除去铜粉中混有的少量氧化铜,其主要操作过程是( )
| A. | 加入过量浓H2SO4微热后,过滤,洗涤 | |
| B. | 加强热或在空气中灼热 | |
| C. | 加适量水,加热,过滤,洗涤 | |
| D. | 加适量稀H2SO4,微热,过滤,洗涤 |
17.如图是治理汽车尾气反应的微观过程,从中获得的信息正确的是( )
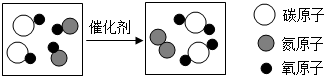

| A. | 该反应方程式为:CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$N2+CO2 | |
| B. | 该反应前后分子的种类没有改变 | |
| C. | 该反应前后原子的数目发生改变 | |
| D. | 该反应体现了一氧化碳的还原性 |
18.现代客机外壳主要材料是铝锂合金.锂的原子结构示意图为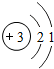 ,下列关于锂的说法错误的是( )
,下列关于锂的说法错误的是( )
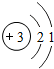 ,下列关于锂的说法错误的是( )
,下列关于锂的说法错误的是( )| A. | 锂元素属于金属元素 | B. | 锂原子的质子数为3 | ||
| C. | 锂元素在化合物中通常显+2价 | D. | 锂原子在化学反应中容易失去电子 |