题目内容
19.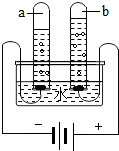 小左做完电解水后的装置情况如图所示.关于本次实验,以下说法不正确的是( )
小左做完电解水后的装置情况如图所示.关于本次实验,以下说法不正确的是( )| A. | a试管中收集到的气体是氢气 | |
| B. | 可以用带火星的木条检验b试管中收集的气体 | |
| C. | a、b两支试管中所收集气体的质量比为2:1 | |
| D. | 该实验可以证明水中含有氢氧两种元素 |
分析 根据电解水的实验现象和结论:电解水时正极生成的是氧气,负极生成的是氢气,氧气和氢气的体积比是1:2,质量比是1:8;据此结合氢气的氧气的化学性质进行分析判断即可.
解答 解:A.a管内气体体积较大,是氢气,故正确;
B.b管内的气体体积较小,是氧气,具有助燃性,能使带火星的木条复燃,故正确;
C.电解水时,可观察到的现象有:与电源正极相连的试管内产生的气体体积少,与电源负极相连的试管内的气体体积多,且两者的体积之比大约是1:2;a、b两试管内分别与电源的负极、正极相连,收集到的气体的体积比约为2:1,而不是质量比,故错误;
D.水电解生成氢气和氧气,化学反应前后元素种类不变,故水是由氢元素和氧元素组成的,故正确.
故选C.
点评 本题难度不大,掌握电解水的实验现象和结论并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
10.下面有关物质的区分方法中,不合理的是( )
| 被区分的物质 | 区分方法 | |
| A | 铁粉-石墨 | 各取少量于试管中,分别滴加稀盐酸,观察有无气泡产生 |
| B | 硬水-软水 | 各取适量于试管中,分别滴加等量肥皂水,振荡,观察产生泡沫多少 |
| C | 羊毛-合成纤维 | 各取少量用酒精灯点燃,闻气味 |
| D | 烧碱-纯碱 | 各取少 量溶液于试管中,分别滴加酚酞试夜,观察颜色变化 |
| A. | A | B. | B | C. | C | D. | D |
7.下列各组物质按单质、化合物和混合物序号排列正确的是( )
| A. | 冰 生石灰 蔗糖 水 | B. | 碘酒 纯水 空气 | ||
| C. | 液氧 盐酸 冰水混合物 | D. | 金刚石 干冰 食盐水 |
14.下列物质中,属于纯净物的是( )
| A. | 大理石 | B. | 糖水 | C. | 黄铜 | D. | 氢气 |
4.某溶液中存在Mg2+、Ag+、Ba2+三种阳离子,现用NaOH,Na2CO3和NaCl三种溶液使它们转化为沉淀并分离出来,要求每次只加一种溶液,滤出一种沉淀,则所加溶液的顺序正确的是( )
| A. | NaCl、NaOH、Na2CO3 | B. | Na2CO3、NaCl、NaOH | ||
| C. | NaOH、NaCl、Na2CO3 | D. | NaCl、Na2CO3、NaOH |
8.化学兴趣小组的同学做中和反应实验时,将稀盐酸滴入氢氧化钠溶液中,看到有气泡产生.同学们认为可能是氢氧化钠溶液变质了.
(分析)氢氧化钠在空气中变质是它能与空气中的二氧化碳反应,化学方程式为:2NaOH+CO2═Na2CO3+H2O.气体是盐酸与碳酸钠反应的结果.
(提出问题)该氢氧化钠溶液是全部变质还是部分变质?
根据实验现象推断相应实验结论.
(实验结论)结论是:氢氧化钠溶液全部(填“部分”或“全部”)变质.
写出实验步骤①中产生白色沉淀的反应的化学方程式CaCl2+Na2CO3═CaCO3↓+2NaCl.
(分析)氢氧化钠在空气中变质是它能与空气中的二氧化碳反应,化学方程式为:2NaOH+CO2═Na2CO3+H2O.气体是盐酸与碳酸钠反应的结果.
(提出问题)该氢氧化钠溶液是全部变质还是部分变质?
根据实验现象推断相应实验结论.
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量该溶液于试管中, 向溶液中滴加过量氯化钙 溶液,振荡. | 有白色沉淀产生. | 说明原溶液中 一定含有碳酸钠. |
| ②取①试管中的上层清液 滴加酚酞试液 | 溶液不变色 | 则溶液中不 含有氢氧化钠. |
写出实验步骤①中产生白色沉淀的反应的化学方程式CaCl2+Na2CO3═CaCO3↓+2NaCl.
