3.根据如图四个化学实验,回答问题:(提示:Cu与Zn的合金称为黄铜)
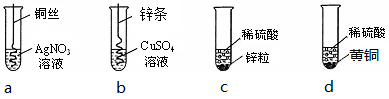
(1)描述实验a中的实验现象铜丝表面附着一层银白色固体,溶液由无色变成蓝色.
(2)要证明Cu、Zn、Ag的活动性顺序,必须要做的实验是ab(填实验序号).
(3)在c实验后的剩余溶液中,一定有的溶质是硫酸锌,可能有的溶质是硫酸,为了确定可能有的溶质,可加入Ⅱ、Ⅳ(填选项序号)
Ⅰ.氯化钡溶液Ⅱ.氢氧化铜Ⅲ.氢氧化钠溶液Ⅳ.锌粒
(4)为了测定d中稀硫酸的溶质质量分数,取20g该黄铜样品于烧杯中,向其中分4次加入该稀硫酸,充分反应.每次所用稀硫酸的质量及剩余固体的质量记录于下表:
试回答下列问题:
Ⅰ.上述表格中m的值为12.0;
Ⅱ.该稀硫酸的溶质质量分数是多少?19.6%(根据化学方程式计算)
0 159450 159458 159464 159468 159474 159476 159480 159486 159488 159494 159500 159504 159506 159510 159516 159518 159524 159528 159530 159534 159536 159540 159542 159544 159545 159546 159548 159549 159550 159552 159554 159558 159560 159564 159566 159570 159576 159578 159584 159588 159590 159594 159600 159606 159608 159614 159618 159620 159626 159630 159636 159644 211419

(1)描述实验a中的实验现象铜丝表面附着一层银白色固体,溶液由无色变成蓝色.
(2)要证明Cu、Zn、Ag的活动性顺序,必须要做的实验是ab(填实验序号).
(3)在c实验后的剩余溶液中,一定有的溶质是硫酸锌,可能有的溶质是硫酸,为了确定可能有的溶质,可加入Ⅱ、Ⅳ(填选项序号)
Ⅰ.氯化钡溶液Ⅱ.氢氧化铜Ⅲ.氢氧化钠溶液Ⅳ.锌粒
(4)为了测定d中稀硫酸的溶质质量分数,取20g该黄铜样品于烧杯中,向其中分4次加入该稀硫酸,充分反应.每次所用稀硫酸的质量及剩余固体的质量记录于下表:
| 加入稀硫酸的质量(g) | 充分反应后剩余固体的质量(g) | |
| 第1次 | 25 | 16.75 |
| 第2次 | 25 | 13.5 |
| 第3次 | 25 | m |
| 第4次 | 25 | 12.0 |
Ⅰ.上述表格中m的值为12.0;
Ⅱ.该稀硫酸的溶质质量分数是多少?19.6%(根据化学方程式计算)


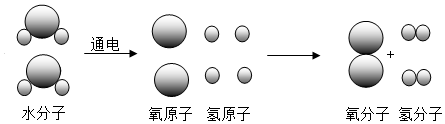
 ①水在天然循环过程中实现了水的自身净化
①水在天然循环过程中实现了水的自身净化