10.汽车用铅蓄电池中需要质量分数为28%的稀硫酸.若在实验室中用10cm3质量分数为98%的浓硫酸(密度为1.84g/cm3)与质量分数为10%的稀硫酸(密度为1.07g/cm3)配制28%的稀硫酸,则量取质量分数为10%的稀硫酸的体积约是( )
| A. | 66.87 cm3 | B. | 88cm3 | C. | 36.34cm3 | D. | 38.9 cm3 |
8.某科技小组的同学,为了比较绍兴与嵊州两地的酸雨污染程度,收集到的证据有:①年降酸雨的次数 ②年降酸雨的平均PH值③煤中含硫的质量分数④年石油的消耗量⑤石油中的含硫量,现将上述证据列成如表进行比较:
(1)根据上述证据:你认为绍兴(绍兴、嵊州)的酸雨严重.
(2)得出上述结果的直接证据是②.(填编号)
(3)酸雨与空气中的飘尘、硫的氧化物等有着密切的关系.空气中的SO2和O2在飘尘作用下转化为SO3.在这一化学反应中,飘尘所起的作用可能是C.(只有一个选项)
A.氧化剂 B.还原剂 C.催化剂
(4)根据自己知识,请你提出一项措施来减少酸雨的形成:将煤脱硫后再使用.
| ① | ② | ③ | ④ | ⑤ | |
| 绍兴 | 18 | 4.85 | 0.023% | 6700吨 | 0.003% |
| 嵊州 | 13 | 5.23 | 0.018% | 4300吨 | 0.002% |
(2)得出上述结果的直接证据是②.(填编号)
(3)酸雨与空气中的飘尘、硫的氧化物等有着密切的关系.空气中的SO2和O2在飘尘作用下转化为SO3.在这一化学反应中,飘尘所起的作用可能是C.(只有一个选项)
A.氧化剂 B.还原剂 C.催化剂
(4)根据自己知识,请你提出一项措施来减少酸雨的形成:将煤脱硫后再使用.
7.铬(Cr)为不锈钢主要的添加元素,含量一般在12%以上.铬的表面生成一薄层致密的钝态氧化物保护膜是不锈钢具有耐蚀性主要原因.请回答下列问题:
(1)不锈钢是一种合金(填“合金”或“金属”).
(2)相同温度下,取大小相同、表面光亮的Cr、Mg、Cu三种金属薄片,分别投入等体积等溶质质量分数的足量稀盐酸中(反应中Cr显+2价),现象如下:
①上述三种金属的活动性由强到弱的顺序是Mg>Cr>Cu.
②从上述探究实验可知,Cr能(填“能”或“不能”)跟CuSO4溶液反应.若反应,请写出反应的化学方程式Cr+CuSO4=CrSO4+Cu.
(1)不锈钢是一种合金(填“合金”或“金属”).
(2)相同温度下,取大小相同、表面光亮的Cr、Mg、Cu三种金属薄片,分别投入等体积等溶质质量分数的足量稀盐酸中(反应中Cr显+2价),现象如下:
| 金属 | Cr | Mg | Cu |
| 与盐酸反应现象 | 放出气泡速率缓慢 | 放出气泡速率较快 | 无明显现象 |
②从上述探究实验可知,Cr能(填“能”或“不能”)跟CuSO4溶液反应.若反应,请写出反应的化学方程式Cr+CuSO4=CrSO4+Cu.
4.下列实验装置合理的是( )
| A. |  分离KNO3和NaCl | B. |  H2还原CuO | ||
| C. |  测定空气中O2含量 | D. |  收集CO2气体 |
3.下列各组中名称、化学式、物质类别相一致的是 ( )
| A. | 干冰、CO2、氧化物 | B. | 氯化铁、FeCl2、盐 | C. | 生石灰、CaCO3、盐 | D. | 纯碱、NaOH、碱 |
2.生活中处处有化学,以下做法不合理的是( )
0 158927 158935 158941 158945 158951 158953 158957 158963 158965 158971 158977 158981 158983 158987 158993 158995 159001 159005 159007 159011 159013 159017 159019 159021 159022 159023 159025 159026 159027 159029 159031 159035 159037 159041 159043 159047 159053 159055 159061 159065 159067 159071 159077 159083 159085 159091 159095 159097 159103 159107 159113 159121 211419
| A. | 用食醋清除水壶中的水垢 | B. | 用汽油擦洗衣服上的油污 | ||
| C. | 用碘酒给伤口消毒 | D. | 用亚硝酸钠替代食盐腌制肉类食品 |
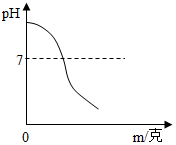 如图所示是稀硫酸与50克质量分数为5%的氢氧化钠溶液反应时,溶液的pH随加入溶液的质量m的变化关系图.请回答下列问题:
如图所示是稀硫酸与50克质量分数为5%的氢氧化钠溶液反应时,溶液的pH随加入溶液的质量m的变化关系图.请回答下列问题:
 归纳是学习的重要方法,小红在复习硫酸和盐酸的性质时归纳出)硫酸和盐酸的五条化学性质(如图所示,连线表示相互反应).
归纳是学习的重要方法,小红在复习硫酸和盐酸的性质时归纳出)硫酸和盐酸的五条化学性质(如图所示,连线表示相互反应).