题目内容
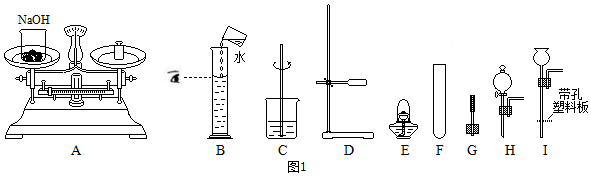
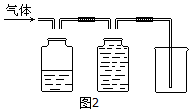
9.由于大量使用一次性塑料方便袋造成的“白色污染”,已成为一个严重的社会问题.小悦同学欲对某种塑料袋的组成进行分析探究(资料显示该塑料只含C、H两种元素),他们设计了如图所示的实验装置,使该塑料试样在纯氧中燃烧,观察实验现象,分析有关数据,推算元素含量.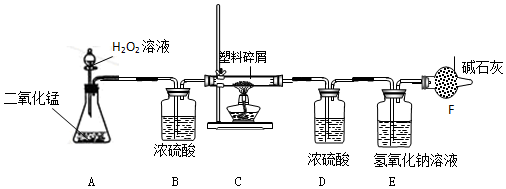
(1)仪器A中所发生的反应化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)若仪器C的玻璃管中放入的塑料试样质量为W克,塑料试样充分燃烧后,若仪器D增重a 克,仪器E增重b克,则W克该塑料试样中含氢元素的质量为$\frac{a}{9}$克(计算结果可为分数形式).
(3)若装置中没有连接仪器B,将使该塑料试样中氢元素的质量测算结果偏大(填“偏小”、“偏大”、“无影响”中之一).
(4)装置F的作用是吸收空气中的二氧化碳和水,防止对实验结果造成干扰.
分析 本题是利用双氧水的分解产生O2,再根据塑料燃烧产物来验证其组成的.
(1)双氧水在二氧化锰的催化作用下分解得到氧气;
(2)可根据元素守恒,水是塑料的燃烧产物,水中的H元素和塑料中H元素质量相同;
(3)若装置中没有连接仪器B,在A装置中的水会在D中和反应生成的水一起被吸收,使水质量增大;
(4)碱石灰能吸收空气中的水和二氧化碳.
解答 解:(1)双氧水在二氧化锰的催化作用下分解得到氧气和水,故答案为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)由元素守恒,塑料中H元素的质量为:a×$\frac{2}{18}$×100%=$\frac{a}{9}$,故答案为:$\frac{a}{9}$;
(3)若装置中没有连接仪器B,没有干燥氧气,使水在D中吸收,质量增大,故答案为:偏大;
(4)装置F中的碱石灰能吸收空气中的二氧化碳和水,防止对实验结果造成干扰,故答案为:吸收空气中的二氧化碳和水,防止对实验结果造成干扰.
点评 本实验题要利用元素守恒的思想,还要特别注意在验证生成物水时要排除从溶液中携带的水的干扰.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
10.蒸馒头时,面碱(主要含Na2CO3 )放多了会发黄,为了除去过多的面碱,做馒头时可加入适量的( )
| A. | 食盐 | B. | 食醋 | C. | 黄酒 | D. | 白糖 |
17.某校化学兴趣小组的同学对一瓶存放已久的氢氧化钠溶液产生浓厚的兴趣,他们探究该溶液是否变质的过程如下:
【提出问题】该氢氧化钠溶液是否变质?
【猜想与假设】
猜想①:氢氧化钠溶液可能全部变质,其溶质是Na2CO3(填化学式,下同)
猜想②:氢氧化钠溶液可能部分变质,其溶质是NaOH、Na2CO3.
猜想③:氢氧化钠溶液没有变质,其溶质是NaOH
【实验探究】
【实验结论】综合上述实验(1)、(2),你得出的结论是猜想②成立.
【反思拓展】(1)氢氧化钠露置于空气中容易变质,原因是2NaOH+CO2═Na2CO3+H2O(用化学方程式表示).
(2)在分析化学反应的物质成分时,除了考虑生成物外,还需考虑的是反应物是否过量.
【提出问题】该氢氧化钠溶液是否变质?
【猜想与假设】
猜想①:氢氧化钠溶液可能全部变质,其溶质是Na2CO3(填化学式,下同)
猜想②:氢氧化钠溶液可能部分变质,其溶质是NaOH、Na2CO3.
猜想③:氢氧化钠溶液没有变质,其溶质是NaOH
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取样于试管中,滴加足量的氯化钡溶液 | 产生白色沉淀 | 原溶液中一定有碳酸钠 |
| (2)取(1)反应后的上层清液于试管中,滴加无色酚酞试液 | 溶液成红色 | 原溶液中一定有氢氧化钠 |
【反思拓展】(1)氢氧化钠露置于空气中容易变质,原因是2NaOH+CO2═Na2CO3+H2O(用化学方程式表示).
(2)在分析化学反应的物质成分时,除了考虑生成物外,还需考虑的是反应物是否过量.
4.下列实验装置合理的是( )
| A. |  分离KNO3和NaCl | B. |  H2还原CuO | ||
| C. |  测定空气中O2含量 | D. |  收集CO2气体 |
14.下列物质能溶于水的是( )
| A. | AgCl | B. | BaSO4 | C. | Ca(NO3)2 | D. | Fe(OH)3 |
1.CaCl2溶液中含有少量的盐酸,欲除去盐酸并使溶液呈中性,在没有指示剂的条件下可选用的试剂是( )
| A. | 石灰水 | B. | 石灰石 | C. | 纯碱 | D. | 硝酸银 |
18.在稀硫酸中加入一定量的下列固体,反应后溶液酸性不会显著减弱的是( )
| A. | 氧化镁 | B. | 碳酸钠 | C. | 氯化钡 | D. | 锌粉 |
19.将一杯质量分数为13%的盐水倒去一半后,剩下的盐水质量分数为( )
| A. | 13% | B. | 26% | C. | 52% | D. | 不一定 |