15.某混合气体可能有COH2中的一种或几种,某学习小组的同学为了探究气体的组成,设计了如下装置进行实验(夹持装置已省略).实验后发现A装置中 溶液变浑浊,C中的固体由黑色变红色,D中的固体由白色变蓝色,F装置中有水流入烧杯.在反应前后对C、D装置进行了质量的测量(各步反应均完全),测量结果如下表:

请分析回答下列问题;
(1)请写出A装置中反应的化学方程式CO2+Ba(OH)2═BaCO3↓+H2O.
(2)一定能证明原混合气体中有氢气存在的实验现象是D中固体由白色变为蓝色.
(3)证明原混合气体中有CO存在的定量关系式是(a-c)>$\frac{8(d-b)}{9}$(用字母a、b、c、d表示)
| 反应前后 | 反应前 | 反应后 |
| C装置中的试管与固体的总质量(克) | a | c |
| D装置的中U形管与固体的总质量 | b | d |

请分析回答下列问题;
(1)请写出A装置中反应的化学方程式CO2+Ba(OH)2═BaCO3↓+H2O.
(2)一定能证明原混合气体中有氢气存在的实验现象是D中固体由白色变为蓝色.
(3)证明原混合气体中有CO存在的定量关系式是(a-c)>$\frac{8(d-b)}{9}$(用字母a、b、c、d表示)
14.某未知溶液可能含Cl-、CO32-、Na+、SO42-、H+.取少量试液,向其中加入紫色石蕊试液,溶液显红色.另取少量试液,滴加硝酸酸化的氯化钡溶液,有白色沉淀生成;在上层清液中滴加硝酸银溶液,产生白色沉淀.下列判断合理的是( )
| A. | 一定有H+、SO42-、Cl- | B. | 一定没有CO32-和Cl- | ||
| C. | 可能有CO32-和SO32- | D. | 一定有H+、SO42-,可能有Cl- |
13.镍粉常用于各种高光泽装饰漆和塑料生产,也常用作催化剂.
I、【镍粉制备】:工业用电解镍新液(主要含NiSO4、NiCl2)制备碱式碳酸镍晶体 xNiCO3•yNi(OH)2•zH2O,并利用其制备镍粉的流程如下:
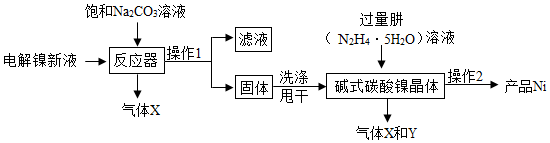
(1)反应器中一个重要反应为 3NiSO4+3Na2CO3+2H2O=NiCO3•2Ni(OH)2+3Na2SO4+2X,X的化学式为CO2.
(2)物料在反应器中反应时需要控制反应条件.分析下图,反应器中最适合的温度及pH分别为55℃、8.3.
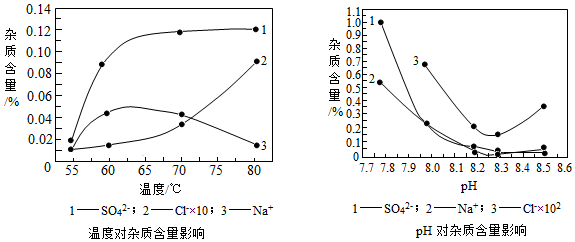
(3)生产中,pH逐渐增加,生成Ni(OH)2含量也相对增加,则生成的碱式碳酸镍晶体 中,镍的含量将升高(填“升高”、“降低”或“不变”).
Ⅱ.【测定碱式碳酸镍晶体的组成】:为测定碱式碳酸镍晶体(xNiCO3•Ni(OH)2•zH2O)组成,某小组设计了如下实验方案及装置:
【资料卡片】
1、碱式碳酸镍晶体受热会完全分解生成NiO、CO2及H2O.
2、400℃左右,NiO会氧化生成Ni2O3.
3、碱石灰是NaOH及CaO的混合物,可以吸收CO2和H2O.
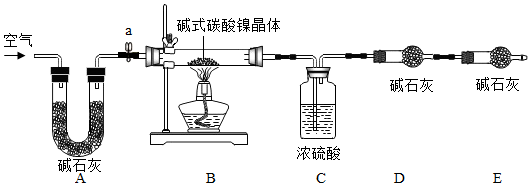
【实验步骤】:
①检查装置的气密性;②准确称取3.77gxNiCO3•yNi(OH)2•zH2O放在B装置中,连接仪器;③打开弹簧夹a,鼓入一段时间空气,称量装置C、D的质量;④关闭弹簧夹a,加热装置B至装置C中导管末端无气泡冒出;⑤打开弹簧夹a,鼓入空气;⑥准确称量装置C、D的质量;⑦根据数据进行计算(相关数据如下表).
【实验分析及数据处理】:
(4)完善实验步骤中的填空:①检查装置的气密性;⑤鼓入空气.
(5)装置E的作用是装置右侧的空气进入装置内造成干扰;
(6)计算 xNiCO3•yNi(OH)2•zH2O中x:y:z 的值1:1:4.
【实验反思】:
(7)实验结束后,称得装置B中残留固体质量为2.33g.请通过计算确定残留固体的组成及各成分的质量(精确到小数点后两位)NiO和Ni2O3混合物,其中NiO的质量为1.50g而Ni2O3的质量为0.83g.
I、【镍粉制备】:工业用电解镍新液(主要含NiSO4、NiCl2)制备碱式碳酸镍晶体 xNiCO3•yNi(OH)2•zH2O,并利用其制备镍粉的流程如下:

(1)反应器中一个重要反应为 3NiSO4+3Na2CO3+2H2O=NiCO3•2Ni(OH)2+3Na2SO4+2X,X的化学式为CO2.
(2)物料在反应器中反应时需要控制反应条件.分析下图,反应器中最适合的温度及pH分别为55℃、8.3.

(3)生产中,pH逐渐增加,生成Ni(OH)2含量也相对增加,则生成的碱式碳酸镍晶体 中,镍的含量将升高(填“升高”、“降低”或“不变”).
Ⅱ.【测定碱式碳酸镍晶体的组成】:为测定碱式碳酸镍晶体(xNiCO3•Ni(OH)2•zH2O)组成,某小组设计了如下实验方案及装置:
【资料卡片】
1、碱式碳酸镍晶体受热会完全分解生成NiO、CO2及H2O.
2、400℃左右,NiO会氧化生成Ni2O3.
3、碱石灰是NaOH及CaO的混合物,可以吸收CO2和H2O.

【实验步骤】:
①检查装置的气密性;②准确称取3.77gxNiCO3•yNi(OH)2•zH2O放在B装置中,连接仪器;③打开弹簧夹a,鼓入一段时间空气,称量装置C、D的质量;④关闭弹簧夹a,加热装置B至装置C中导管末端无气泡冒出;⑤打开弹簧夹a,鼓入空气;⑥准确称量装置C、D的质量;⑦根据数据进行计算(相关数据如下表).
| 装置C/g | 装置D/g | 装置E/g | |
| 加热前 | 200.00 | 180.00 | 180.00 |
| 加热后 | 201.08 | 180.44 | 180.00 |
(4)完善实验步骤中的填空:①检查装置的气密性;⑤鼓入空气.
(5)装置E的作用是装置右侧的空气进入装置内造成干扰;
(6)计算 xNiCO3•yNi(OH)2•zH2O中x:y:z 的值1:1:4.
【实验反思】:
(7)实验结束后,称得装置B中残留固体质量为2.33g.请通过计算确定残留固体的组成及各成分的质量(精确到小数点后两位)NiO和Ni2O3混合物,其中NiO的质量为1.50g而Ni2O3的质量为0.83g.
10.有关溶液的下列说法中不正确的是( )
①溶液都是透明、均一、稳定的混合物.
②同种溶质的饱和溶液一定比它的不饱和溶液浓.
③把不饱和溶液转变成饱和溶液,溶质质量分数一定变大.
①溶液都是透明、均一、稳定的混合物.
②同种溶质的饱和溶液一定比它的不饱和溶液浓.
③把不饱和溶液转变成饱和溶液,溶质质量分数一定变大.
| A. | ①② | B. | ①③ | C. | ①②③ | D. | ②③ |
9.下列关于原子的叙述正确的是( )
①一切原子都是由质子、中子和电子构成
②原子的质量几乎都集中在原子核中
③原子是在化学变化中不可再分的粒子
④原子由原子核和核外电子构成
⑤生活中常接触到的“高钙牛奶”、“加碘食盐”中的“钙”、“碘”指的是原子.
0 158193 158201 158207 158211 158217 158219 158223 158229 158231 158237 158243 158247 158249 158253 158259 158261 158267 158271 158273 158277 158279 158283 158285 158287 158288 158289 158291 158292 158293 158295 158297 158301 158303 158307 158309 158313 158319 158321 158327 158331 158333 158337 158343 158349 158351 158357 158361 158363 158369 158373 158379 158387 211419
①一切原子都是由质子、中子和电子构成
②原子的质量几乎都集中在原子核中
③原子是在化学变化中不可再分的粒子
④原子由原子核和核外电子构成
⑤生活中常接触到的“高钙牛奶”、“加碘食盐”中的“钙”、“碘”指的是原子.
| A. | ②③④ | B. | ②④ | C. | ②③④⑤ | D. | ①②③④⑤ |


 氯化钠是一种重要的化工原料,电解氯化钠溶液可制得氯气、氢氧化钠等物质,发生的化学反应如下:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$ Cl2↑+H2↑+2NaOH.现取一定质量的溶质质量分数为10%的氯化钠溶液进行电解,当氯化钠完全反应时,停止通电.生成氯气的质量与反应时间的关系如图所示.
氯化钠是一种重要的化工原料,电解氯化钠溶液可制得氯气、氢氧化钠等物质,发生的化学反应如下:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$ Cl2↑+H2↑+2NaOH.现取一定质量的溶质质量分数为10%的氯化钠溶液进行电解,当氯化钠完全反应时,停止通电.生成氯气的质量与反应时间的关系如图所示.