4.下列物质长期暴露在空气中不会变质的是( )
| A. | 浓盐酸 | B. | 熟石灰 | C. | 生石灰 | D. | 烧碱 |
3.设计实验方案是科学探究的重要环节,以下化学实验设计中不能达到实验目的是( )
| A. | 厨房中用淀粉鉴别食中是否含有碘单质 | |
| B. | 用湿润的pH试纸区别氨气和氯化氢气体 | |
| C. | 厨房中用食醋鉴别纯碱与食盐 | |
| D. | 用AgNO3溶液鉴别实验室制取二氧化碳的剩余废液中是否存在过量的盐酸 |
2.现有含氯化钠的碳酸钠样品,为测定样品中氯化钠的含量.课外活动小组的同学称取20g该样品于烧杯中,并将80g稀盐酸评价分成四份,依次加入烧杯中,实验数据如表:
计算:
(1)产生CO2气体的总质量;
(2)样品中氯化钠的百分含量;
(3)使用的稀盐酸的溶质质量分数.
| 实验序号 | 第一次 | 第二次 | 第三次 | 第四次 |
| 加入稀盐酸的质量/g | 20 | 20 | 20 | 20 |
| 反应后烧杯中剩余物质的质量/g | 37.8 | 55.6 | 74.5 | 94.5 |
(1)产生CO2气体的总质量;
(2)样品中氯化钠的百分含量;
(3)使用的稀盐酸的溶质质量分数.
20.以下说法正确的是( )
| A. | 三种物质CuSO4、Mg(NO3)2、CaO可以共存于同一溶液中 | |
| B. | 盐都是由金属阳离子和酸根阴离子构成 | |
| C. | 只用水就能区分CaCO3、NaOH、NaCl、NH4NO3四种白色固体 | |
| D. | 某可燃物燃烧后生成的产物中有CO2、CO和SO2,则该物质一定含有碳、硫、氧元素 |
19.有关下列叙述正确的是( )
| A. | 在KMnO4→K2MnO4这一变化前后,酸根不变 | |
| B. | 根据图 可以确定钙元素原子的核外电子数为20 可以确定钙元素原子的核外电子数为20 | |
| C. | 水通电分解过程中,不改变的粒子是水分子 | |
| D. | H2S表示硫化氢分子是2个氢原子和1个硫原子构成的 |
18.分类是化学学习和研究常用的方法,下列分类中正确的是( )
| A. | 人体必须的微量元素:锌、铁、氟 | B. | 合金:不锈钢、生铁、金刚石 | ||
| C. | 碱:纯碱、小苏打、消石灰 | D. | 混合物:生理盐水、硫酸、煤 |
17.如图所示的实验,发生化学变化的是( )
| A. |  品红加入水中,整个液体变红 | B. |  用自制净水器净水 | ||
| C. |  二氧化碳溶于水 | D. |  比较硬度 |
16.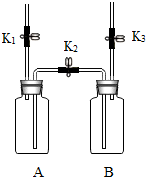 某同学利用如图所示装置进行实验.实验前止水夹K1、K2、K3均都已关闭.请回答下列问题.
某同学利用如图所示装置进行实验.实验前止水夹K1、K2、K3均都已关闭.请回答下列问题.
(1)检查装置的气密性:保持K1关闭,打开K2、K3,向B中加水浸没下端导管口,用手捂住A瓶外壁,若B中导管口处有气泡产生,说明A装置的气密性良好.同样原理检查装置另一侧的气密性良好.
【实验一】制备气体
Ⅰ.打开K1,用注射器向盛有锌粒的A中注入稀硫酸,至液面浸没下端导管口.
Ⅱ.在K1上方导管口收集气体.
(2)A中发生反应的化学方程式Zn+H2SO4═ZnSO4+H2↑;气体收集完毕,在不拆卸装置的情况下,将A中未反应稀硫酸大部分转移到B中的操作是打开k2,k3,关闭k1.
【实验二】测定气体含量
Ⅰ.先将B重装满水,然后再用注射器扎入胶塞向A(容积为300mL,里面是乐乐同学用排空气法收集的二氧化碳气体)中注入15mLNaOH溶液,充分振荡.
Ⅱ.完全反应后,打开止水夹K2、K3.
(3)当B中的液面不再发生变化时,测得B中的水减少了135mL,则A中所收集的二氧化碳气体的体积分数为50%.
【拓展研究】用不同的方法各收集一瓶(相同体积)二氧化碳,实验抽样数据记录如表:
说明:
①实验一、二用时相同;实验三是待到集气瓶口火柴棒熄灭视为二氧化碳集满瓶.
②二氧化碳的体积分数(纯度)是根据相应反应、测试并进行计算而得出的数据.
(4)分析上面的数据,你的一点新思考是可否用排水法收集二氧化碳.
0 157651 157659 157665 157669 157675 157677 157681 157687 157689 157695 157701 157705 157707 157711 157717 157719 157725 157729 157731 157735 157737 157741 157743 157745 157746 157747 157749 157750 157751 157753 157755 157759 157761 157765 157767 157771 157777 157779 157785 157789 157791 157795 157801 157807 157809 157815 157819 157821 157827 157831 157837 157845 211419
 某同学利用如图所示装置进行实验.实验前止水夹K1、K2、K3均都已关闭.请回答下列问题.
某同学利用如图所示装置进行实验.实验前止水夹K1、K2、K3均都已关闭.请回答下列问题.(1)检查装置的气密性:保持K1关闭,打开K2、K3,向B中加水浸没下端导管口,用手捂住A瓶外壁,若B中导管口处有气泡产生,说明A装置的气密性良好.同样原理检查装置另一侧的气密性良好.
【实验一】制备气体
Ⅰ.打开K1,用注射器向盛有锌粒的A中注入稀硫酸,至液面浸没下端导管口.
Ⅱ.在K1上方导管口收集气体.
(2)A中发生反应的化学方程式Zn+H2SO4═ZnSO4+H2↑;气体收集完毕,在不拆卸装置的情况下,将A中未反应稀硫酸大部分转移到B中的操作是打开k2,k3,关闭k1.
【实验二】测定气体含量
Ⅰ.先将B重装满水,然后再用注射器扎入胶塞向A(容积为300mL,里面是乐乐同学用排空气法收集的二氧化碳气体)中注入15mLNaOH溶液,充分振荡.
Ⅱ.完全反应后,打开止水夹K2、K3.
(3)当B中的液面不再发生变化时,测得B中的水减少了135mL,则A中所收集的二氧化碳气体的体积分数为50%.
【拓展研究】用不同的方法各收集一瓶(相同体积)二氧化碳,实验抽样数据记录如表:
| 实验序号 | 实验一 | 实验二 | 实验三 |
| 实验方法 | 排水法收集二氧化碳 | 排空气法集二氧化碳 | 排空气法集二氧化碳 |
| CO2体积分数(%) | 91.1 | 69.5 | 61.9 |
①实验一、二用时相同;实验三是待到集气瓶口火柴棒熄灭视为二氧化碳集满瓶.
②二氧化碳的体积分数(纯度)是根据相应反应、测试并进行计算而得出的数据.
(4)分析上面的数据,你的一点新思考是可否用排水法收集二氧化碳.
