1.化学反应的基本特征是有新物质生成,常表现出能量的变化和颜色的变化,下列物质在发生化学反应的同时,也有能量变化和“蓝色”产生,你认为违背了化学反应原理的是( )
| 物质间的反应与反应条件 | 颜色变化 | 化学反应原理 |
| A.硫在空气中燃烧 | 淡蓝色火焰 | S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 |
| B.一氧化碳在空气中点燃 | 蓝色火焰 | 2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 |
| C.氧化铜与盐酸反应 | 蓝色 | CuO+2HCl═CuCl2+H2O |
| D.将铜放入稀硫酸中 | 蓝色 | Cu+H2SO4═CuSO4+H2↑ |
| A. | A | B. | B | C. | C | D. | D |
20.珍惜生命,远离毒品.每年6.26是国际禁毒日.凉山州公安局公开销毁缴获的毒品,其中毒品冰毒的化学式为C10H15N,下列关于冰毒的说法错误的是( )
| A. | 该物质中碳、氢、氮元素的质量比为10:15:1 | |
| B. | 该物质由碳、氢、氮三种元素组成 | |
| C. | 该物质一个分子由10个碳原子,15个氢原子和1个氮原子构成 | |
| D. | 该物质的相对分子质量为12×10+1×15+14=149 |
19.概括和归纳是学习化学的重要方法,把需要掌握和记忆的知识用简洁的语言,精炼的文字表述出来也是一种能力表现,下列是初中化学中的“三”,你认为不符合化学原理的是( )
| A. | 三多$\left\{\begin{array}{l}{地壳中含量最多的元素是氧}\\{地壳中含量最多的金属元素是铝}\\{空气中含量最多的元素是氮}\end{array}\right.$ | |
| B. | 三少$\left\{\begin{array}{l}{人体中含量最少的金属元素是钙}\\{人体中含量最少的非金属元素是氧}\\{人体中供给能量最少的是油脂}\end{array}\right.$ | |
| C. | 三红$\left\{\begin{array}{l}{赤铁矿--Fe2O3--红色}\\{氧化汞--HgO--红色}\\{铜粉--Cu--红色}\end{array}\right.$ | |
| D. | 三黑$\left\{\begin{array}{l}{四氧化三铁--Fe3O4--黑色}\\{碳粉--C--黑色}\\{二氧化锰--MnO2--黑色}\end{array}\right.$ |
18. 实验室有一变质的氢氧化钠样品(样品中只含碳酸钠杂质,且成分均匀),为测量样品中Na2CO3的质量分数,小明进行了如下实验.
实验室有一变质的氢氧化钠样品(样品中只含碳酸钠杂质,且成分均匀),为测量样品中Na2CO3的质量分数,小明进行了如下实验.
①取质量、大小相同的3个烧杯,分别加入一定质量分数的稀盐酸100克;
②向上述3个烧杯中分别加入3份质量不同的样品;
③充分反应后,再用电子天平称量烧杯及烧杯内物质的总质量(假设产生的气体完全逸出).实验数据如下:
已知实验中发生的化学反应:NaOH+HCl═NaCl+H2O
Na2CO3+2HCl═2NaCl+H2O+CO2↑
(1)分析表中数据,写出判断实验二中的样品已完全反应的理由:实验三产生的气体的质量为150g+12g-158.7g=3.3g,实验二产生的气体的质量为150g+8g-155.8g=2.2g,实验三产生的气体的质量大于实验二,所以实验二中稀盐酸有剩余,8g样品已完全反应..
(2)表中的m值为152.9.
(3)根据实验二中的数据计算样品中Na2CO3的质量分数.
0 157539 157547 157553 157557 157563 157565 157569 157575 157577 157583 157589 157593 157595 157599 157605 157607 157613 157617 157619 157623 157625 157629 157631 157633 157634 157635 157637 157638 157639 157641 157643 157647 157649 157653 157655 157659 157665 157667 157673 157677 157679 157683 157689 157695 157697 157703 157707 157709 157715 157719 157725 157733 211419
 实验室有一变质的氢氧化钠样品(样品中只含碳酸钠杂质,且成分均匀),为测量样品中Na2CO3的质量分数,小明进行了如下实验.
实验室有一变质的氢氧化钠样品(样品中只含碳酸钠杂质,且成分均匀),为测量样品中Na2CO3的质量分数,小明进行了如下实验.①取质量、大小相同的3个烧杯,分别加入一定质量分数的稀盐酸100克;
②向上述3个烧杯中分别加入3份质量不同的样品;
③充分反应后,再用电子天平称量烧杯及烧杯内物质的总质量(假设产生的气体完全逸出).实验数据如下:
| 实验一 | 实验二 | 实验三 | |
| 反应前稀盐酸+烧杯质量(克) | 150 | 150 | 150 |
| 反应前固体样品质量(克) | 4 | 8 | 12 |
| 反应后烧杯内物质+烧杯质量(克) | m | 155.8 | 158.7 |
Na2CO3+2HCl═2NaCl+H2O+CO2↑
(1)分析表中数据,写出判断实验二中的样品已完全反应的理由:实验三产生的气体的质量为150g+12g-158.7g=3.3g,实验二产生的气体的质量为150g+8g-155.8g=2.2g,实验三产生的气体的质量大于实验二,所以实验二中稀盐酸有剩余,8g样品已完全反应..
(2)表中的m值为152.9.
(3)根据实验二中的数据计算样品中Na2CO3的质量分数.
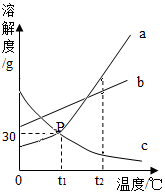 如图是a、b、c三种物质(不含结晶水)的溶解度曲线,a与c的溶解度曲线交于P点,请据图回答
如图是a、b、c三种物质(不含结晶水)的溶解度曲线,a与c的溶解度曲线交于P点,请据图回答 某校举行科学实验操作考查,由学生抽签确定考察的实验内容,要求根据提供的实验器材完成相关实验.
某校举行科学实验操作考查,由学生抽签确定考察的实验内容,要求根据提供的实验器材完成相关实验. 为了研究可燃物的燃烧条件,某兴趣小组同学用如图所示装置进行实验(白磷、红磷均不超过绿豆大小,锥形瓶中的白磷A与红磷C尽量拉开距离),白磷的着火点为40℃,红磷的着火点为240℃.
为了研究可燃物的燃烧条件,某兴趣小组同学用如图所示装置进行实验(白磷、红磷均不超过绿豆大小,锥形瓶中的白磷A与红磷C尽量拉开距离),白磷的着火点为40℃,红磷的着火点为240℃.