题目内容
18. 实验室有一变质的氢氧化钠样品(样品中只含碳酸钠杂质,且成分均匀),为测量样品中Na2CO3的质量分数,小明进行了如下实验.
实验室有一变质的氢氧化钠样品(样品中只含碳酸钠杂质,且成分均匀),为测量样品中Na2CO3的质量分数,小明进行了如下实验.①取质量、大小相同的3个烧杯,分别加入一定质量分数的稀盐酸100克;
②向上述3个烧杯中分别加入3份质量不同的样品;
③充分反应后,再用电子天平称量烧杯及烧杯内物质的总质量(假设产生的气体完全逸出).实验数据如下:
| 实验一 | 实验二 | 实验三 | |
| 反应前稀盐酸+烧杯质量(克) | 150 | 150 | 150 |
| 反应前固体样品质量(克) | 4 | 8 | 12 |
| 反应后烧杯内物质+烧杯质量(克) | m | 155.8 | 158.7 |
Na2CO3+2HCl═2NaCl+H2O+CO2↑
(1)分析表中数据,写出判断实验二中的样品已完全反应的理由:实验三产生的气体的质量为150g+12g-158.7g=3.3g,实验二产生的气体的质量为150g+8g-155.8g=2.2g,实验三产生的气体的质量大于实验二,所以实验二中稀盐酸有剩余,8g样品已完全反应..
(2)表中的m值为152.9.
(3)根据实验二中的数据计算样品中Na2CO3的质量分数.
分析 根据质量守恒定律可知,过程中质量的减少是因为生成了二氧化碳,所以可以求算二氧化碳的质量,根据二氧化碳的质量和对应的化学方程式求算碳酸钠的质量,进而求算对应的质量分数.
解答 解:
(1)分析表中数据,写出判断实验二中的样品已完全反应的理由:实验三产生的气体的质量为150g+12g-158.7g=3.3g,实验二产生的气体的质量为150g+8g-155.8g=2.2g,实验三产生的气体的质量大于实验二,所以实验二中稀盐酸有剩余,8g样品已完全反应..
(2)表中的m值为 152.9.
(3)根据实验二中的数据计算样品中Na2CO3的质量分数.根据质量守恒定律可得,生成的二氧化碳的质量为150g+8g-155.8g=2.2g
设参加反应的碳酸钠的质量为x
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 44
x 2.2g
$\frac{106}{44}$=$\frac{x}{2.2g}$
x=5.3
样品中Na2CO3的质量分数为$\frac{5.3g}{8g}$×100%≈66.25%
答:
(1)实验三产生的气体的质量为150g+12g-158.7g=3.3g,实验二产生的气体的质量为150g+8g-155.8g=2.2g,实验三产生的气体的质量大于实验二,所以实验二中稀盐酸有剩余,8g样品已完全反应..
(2)152.9.
(3)样品中Na2CO3的质量分数为66.25%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.下列图象能正确反映其对应操作的是( )
| A. | 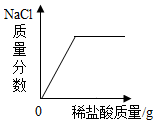 一定量的NaOH溶液中逐滴加入稀盐酸 | |
| B. | 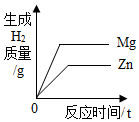 等质量、等质量分数的稀硫酸中分别加入足量的镁粉和锌粉 | |
| C. | 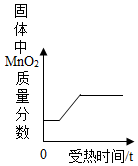 用适量KClO3和MnO2的混合物加热制取O2 | |
| D. | 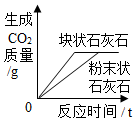 等质量、不同形状的石灰石中分別加入足量相同的稀盐酸 |
6.在一定条件下,一个密闭容器内发生某反应,测得反应过程中各物质的质量部分数据如表所示:下列说法正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前的质量/g | 12 | 26 | 3 | 0 |
| 反应中的质量/g | 9 | 22 | 3 | b |
| 反应后的质量/g | 0 | a | 3 | 28 |
| A. | a等于10 | B. | 该化学反应为复分解反应 | ||
| C. | 丙一定为催化剂 | D. | b等于12 |
10.化学与生产、生活密切相关.下列说法错误的是( )
| A. | 用活性炭吸附室内甲醛,降低甲醛对人体的危害 | |
| B. | 施用大量农药减少病虫害 | |
| C. | 用氯化钠作融雪剂,消除公路上的积雪 | |
| D. | 医疗上用乙醇体积分数为75%的酒精杀菌消毒 |
7.下列关于空气的说法中,不正确的是( )
| A. | 工业上采用分离液态空气法获得氧气 | |
| B. | 二氧化硫是空气污染物之一 | |
| C. | 空气中氧气质量占空气质量的21% | |
| D. | 空气中的氧气来源于绿色植物的光合作用 |
5. 在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的研究.
在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的研究.
探究一 M溶液中的溶质是什么?
(1)【提出猜想】该组同学认为M溶液的溶质有两种可能:
①是Ca(OH)2,②是CaCl2.
【收集资料】CaCl2水溶液呈中性.
(2)【设计实验】同学们设计了如下方案并进行实验:
探究二 过滤后澄清滤液中会有哪些溶质?
【提出猜想】猜想一:NaOH和Na2CO3;猜想二:NaOH和Ca(OH)2;猜想三:NaOH
(3)【实验验证】同学们针对“猜想一”进行了如下实验:
他们的实验结论是否正确?不正确,理由是溶液中氢氧化钠能与加入的少量盐酸反应,即使溶液中有Na2CO3溶液也可能不产生气体.
 在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的研究.
在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的研究.探究一 M溶液中的溶质是什么?
(1)【提出猜想】该组同学认为M溶液的溶质有两种可能:
①是Ca(OH)2,②是CaCl2.
【收集资料】CaCl2水溶液呈中性.
(2)【设计实验】同学们设计了如下方案并进行实验:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量M溶液于 试管中,向其中滴加酚酞溶液. | 酚酞溶液变红色. | 猜想①正确,碳酸钠与其反应的化学 方程为Na2CO3+Ca(OH)2=CaCO3↓+2NaOH. |
【提出猜想】猜想一:NaOH和Na2CO3;猜想二:NaOH和Ca(OH)2;猜想三:NaOH
(3)【实验验证】同学们针对“猜想一”进行了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,滴入几滴稀盐酸 | 没有气体产生. | “猜想一”不成立 |
 )和118号(Og
)和118号(Og )为化学新元素.其中,“115号(Mc 镆)”中115表示原子的原子序数,Mc表示的微观意义是一个镆原子.
)为化学新元素.其中,“115号(Mc 镆)”中115表示原子的原子序数,Mc表示的微观意义是一个镆原子.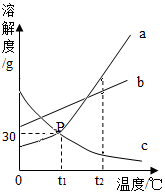 如图是a、b、c三种物质(不含结晶水)的溶解度曲线,a与c的溶解度曲线交于P点,请据图回答
如图是a、b、c三种物质(不含结晶水)的溶解度曲线,a与c的溶解度曲线交于P点,请据图回答