7.下列各项中,前者一定大于后者的是( )
| A. | 1g H2与9g O2完全燃烧生成水的质量、1g H2与8g O2完全燃烧生成水的质量 | |
| B. | 甲的饱和溶液的质量分数、甲的不饱和溶质的质量分数 | |
| C. | 50g NaOH溶液吸收少量CO2后溶液的质量、50g Ca(OH)2溶液吸收少量CO2后溶液的质量 | |
| D. | 10%的盐酸的pH、10%的烧碱溶液的pH |
5.小亮在实验室发现一瓶盛有无色溶液的试剂瓶,其标签破损,从残余部分只能看出溶质的质量分数为10%,具体是什么物质无法辨认.老师告诉他,这瓶溶液可能是氢氧化钠、氯化钠、氢氧化钙、氯化钠、氢氧化钙或是碳酸钠中的一种.
(1)小亮查阅氢氧化钙常温下的溶解度为0.18g后,认为该溶液不可能是氢氧化钙,理由是常温下不可能得到质量分数为10%的氢氧化钙溶液.
(2)小亮取少量样品于试管中,滴加无色酚酞溶液(填“紫色石蕊溶液”或“无色酚酞溶液”),试液边红色,该溶液不可能是氯化钠.
(3)为了确定该溶液的成分,小亮同学继续进行下列实验,请一起参与,并填写下列实验报告.
【设计实验方案】方案甲:选择BaCl2溶液来确定该溶液的成份;
方案乙:选择稀盐酸来确定该溶液的成份.
【进行实验】小亮选择了方案甲进行实验:
(4)【实验反思】①有同学认为还可以用一种常见的碱溶液来确定,那么它可能是Ca(OH)2溶液;
②小亮经过反思,向同学们提出如下建议,你认为合理的是A
A.倾倒液体时,应注意保护标签不被腐蚀 B.无法辨认的药品,直接倒掉,无需保留.
(1)小亮查阅氢氧化钙常温下的溶解度为0.18g后,认为该溶液不可能是氢氧化钙,理由是常温下不可能得到质量分数为10%的氢氧化钙溶液.
(2)小亮取少量样品于试管中,滴加无色酚酞溶液(填“紫色石蕊溶液”或“无色酚酞溶液”),试液边红色,该溶液不可能是氯化钠.
(3)为了确定该溶液的成分,小亮同学继续进行下列实验,请一起参与,并填写下列实验报告.
【设计实验方案】方案甲:选择BaCl2溶液来确定该溶液的成份;
方案乙:选择稀盐酸来确定该溶液的成份.
【进行实验】小亮选择了方案甲进行实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量溶液于试管中,滴加BaCl2溶液. | 该溶液是碳酸钠溶液. 有关反应方程式为:BaCl2+Na2CO3═BaCO3↓+2NaCl |
②小亮经过反思,向同学们提出如下建议,你认为合理的是A
A.倾倒液体时,应注意保护标签不被腐蚀 B.无法辨认的药品,直接倒掉,无需保留.
3.设计方案是实验探究的保证,感悟方法是探究的根本目的.某化学学习小组欲对实验室失去标签的三瓶无色溶液A、B、C的成分进行探究,它们可能是NH4Cl溶液、NaOH溶液、Na2CO3溶液中的一种,探究过程如下:
【分析】从组成上看,NH4Cl属于铵盐,含有NH4+,与强碱溶液反应会有氨气产生,NaOH溶液和Na2CO3溶液中因为含有不同阴离子,所以性质不同,据此可鉴别.
【设计方案并实验】
【反思与评价】小组同学讨论后一致认为小贝的结论不正确,理由是碳酸钠溶液也显碱性.
【方法感悟】在检验物质时,要分析物质的组成和性质(或化学性质),据此选择加入适当的试剂,最后根据不同现象得出结论.
【问题处理】几天后,小明才发现取完C后忘了及时盖上瓶塞,若要除去其中杂质,可向其中加入适量的氢氧化钙(或氢氧化钡)溶液.
【分析】从组成上看,NH4Cl属于铵盐,含有NH4+,与强碱溶液反应会有氨气产生,NaOH溶液和Na2CO3溶液中因为含有不同阴离子,所以性质不同,据此可鉴别.
【设计方案并实验】
| 实验操作 | 现象 | 结论 |
| (1)小红分别取适量A、B、C三种溶液于三只试管中,再分别加入氢氧化钠溶液微热 | A中产生有刺激性气味的气体,B、C中无气味 | A是NH4Cl溶液. A与氢氧化钠溶液反应的化学方程式:NH4Cl+NaOH$\frac{\underline{\;\;△\;\;}}{\;}$NaCl+H2O+NH3↑. |
| (2)小贝分别取适量B、C两种溶液于两只试管中,再分别滴加酚酞溶液 | 酚酞溶液变红 | B、C都是NaOH溶液 |
| (3)小明也分别取适量B、C两种溶液于两只试管中,再分别滴加稀盐酸(或氢氧化钙溶液、氯化钙溶液). | B中有气泡产生(或有白色沉淀产生) | B是Na2CO3溶液 C是NaOH溶液 |
【方法感悟】在检验物质时,要分析物质的组成和性质(或化学性质),据此选择加入适当的试剂,最后根据不同现象得出结论.
【问题处理】几天后,小明才发现取完C后忘了及时盖上瓶塞,若要除去其中杂质,可向其中加入适量的氢氧化钙(或氢氧化钡)溶液.
3. 全国各地进行新农村建设,宽敞的马路两旁都装上了太阳能路灯.太阳能路灯是利用太阳能进行照明的装置.太阳能路灯由太阳能电池板、蓄电池、LED路灯灯头、灯柱、微电脑控制器这五大部分组成.
全国各地进行新农村建设,宽敞的马路两旁都装上了太阳能路灯.太阳能路灯是利用太阳能进行照明的装置.太阳能路灯由太阳能电池板、蓄电池、LED路灯灯头、灯柱、微电脑控制器这五大部分组成.
(1)太阳能电池板的主要材料是硅,硅单质与金刚石结构相似,则构成硅单质的粒子是①(填序号).
①原子 ②分子 ③离子
(2)蓄电池白天将太阳能转化为化学能储存,晚上把化学能转化成光能.
(3)在太阳能路灯各组件中,其主要材料属于有机合成材料的是C(填序号).
A.硅电池板 B.铝合金灯柱 C.塑料灯罩 D.钢质防盗螺丝
(4)灯柱材料用铝合金制成,欲探究铝与铜盐溶液的反应,小华同学设计了两种铜盐溶液分别与金属铝片(经打磨后)的反应.
I、实验一中铝与硫酸铜溶液反应的化学方程式为2Al+3CuSO4═3Cu+Al2(SO4)3.
II、实验二中产生的气体经检验有爆鸣声,该气体为氢气,还在铝片表面观察到蓝色絮状沉淀物,该物质的化学式为Cu(OH)2.
0 157301 157309 157315 157319 157325 157327 157331 157337 157339 157345 157351 157355 157357 157361 157367 157369 157375 157379 157381 157385 157387 157391 157393 157395 157396 157397 157399 157400 157401 157403 157405 157409 157411 157415 157417 157421 157427 157429 157435 157439 157441 157445 157451 157457 157459 157465 157469 157471 157477 157481 157487 157495 211419
 全国各地进行新农村建设,宽敞的马路两旁都装上了太阳能路灯.太阳能路灯是利用太阳能进行照明的装置.太阳能路灯由太阳能电池板、蓄电池、LED路灯灯头、灯柱、微电脑控制器这五大部分组成.
全国各地进行新农村建设,宽敞的马路两旁都装上了太阳能路灯.太阳能路灯是利用太阳能进行照明的装置.太阳能路灯由太阳能电池板、蓄电池、LED路灯灯头、灯柱、微电脑控制器这五大部分组成.(1)太阳能电池板的主要材料是硅,硅单质与金刚石结构相似,则构成硅单质的粒子是①(填序号).
①原子 ②分子 ③离子
(2)蓄电池白天将太阳能转化为化学能储存,晚上把化学能转化成光能.
(3)在太阳能路灯各组件中,其主要材料属于有机合成材料的是C(填序号).
A.硅电池板 B.铝合金灯柱 C.塑料灯罩 D.钢质防盗螺丝
(4)灯柱材料用铝合金制成,欲探究铝与铜盐溶液的反应,小华同学设计了两种铜盐溶液分别与金属铝片(经打磨后)的反应.
| 实验一:4mL 8%的CuSO4溶液 | 实验二:4mL 8%的CuCl2溶液 | |
| 实验现象 | 短时间无变化,数小时后铝片上仅有少量红色斑点出现 | 立即产生大量气泡,铝片上迅速有一层暗红色物质出现 |
II、实验二中产生的气体经检验有爆鸣声,该气体为氢气,还在铝片表面观察到蓝色絮状沉淀物,该物质的化学式为Cu(OH)2.
 利用如图装置进行实验.实验前K1、K2均已关闭,装置气密性良好.
利用如图装置进行实验.实验前K1、K2均已关闭,装置气密性良好.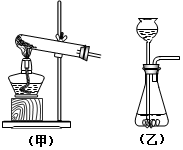 探究实验室制取气体的方法
探究实验室制取气体的方法


 同学们在实验室看到有一瓶没有盖瓶塞的硫酸,欲测量这瓶硫酸的质量分数,现取50g该硫酸溶液倒入烧杯中,再向该烧杯中滴加17.1%的Ba(OH)2溶液,测量的pH与滴加Ba(OH)2溶液之间的关系如图所示:
同学们在实验室看到有一瓶没有盖瓶塞的硫酸,欲测量这瓶硫酸的质量分数,现取50g该硫酸溶液倒入烧杯中,再向该烧杯中滴加17.1%的Ba(OH)2溶液,测量的pH与滴加Ba(OH)2溶液之间的关系如图所示: