题目内容
6. 探究实验室制取气体的方法
探究实验室制取气体的方法实验室中进行实验需要制取少量的乙炔气体,小婷同学对制取乙炔的方法进行了探究.请你参与她探究过程并回答有关问题.
小婷同学首先查阅了相关资料,获得了如下信息:
①乙炔(C2H2)是一种无色、无味、无嗅的气体,比空气轻,微溶于水,易燃烧.
②(A)天然气在电炉中高温下反应可生成乙炔:2CH4$\frac{\underline{\;高温\;}}{\;}$C2H2+3H2
(B)固体碳化钙(CaC2)与水反应可生成乙炔:CaC2+2H2O=Ca(OH)2+C2H2↑
(1)实验室应选择制取乙炔气体的反应是B(填“A”或“B”),选择该反应的理由是反应在室温下发生,容易控制
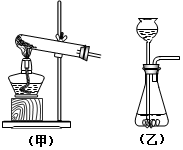
(2)实验室中有以下两套气体的发生装置.
制取乙炔应选择的装置是乙(填“甲”或“乙”).
你选择此装置的理由是反应为固体与液体反应不需要加热制取气体的反应.
(3)实验室中收集乙炔气体可采用的方法是向下排空气法(或排水法),选择此方法的理由是乙炔密度比空气小(乙炔微溶于水)..
(4)实验室用大理石和稀盐酸反应制取二氧化碳,应选择的发生装置是乙(填“甲”或“乙”),发生反应的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑.收集满气体的集气瓶应该正放在桌面上.写出用澄清的石灰水检验二氧化碳的化学方程式CO2+Ca(OH)2=CaCO3↓+H2O.
分析 制取装置包括加热和不需加热两种,固体碳化钙(CaC2)与水反应可生成乙炔,反应在室温下发生,容易控制,因此不用加热;乙炔(C2H2)是一种无色、无味、无嗅的气体,比空气轻,微溶于水,因此可以用向下排空气法和排水法收集;实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.收集满气体的集气瓶应该正放在桌面上,二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳.
解答 解:(1)天然气在电炉中高温下反应可生成乙炔,还有杂质氢气,固体碳化钙(CaC2)与水反应可生成乙炔,反应在室温下发生,容易控制,因此不用加热;故答案为:B;反应在室温下发生,容易控制;
(2)固体碳化钙(CaC2)与水反应,反应为固体与液体反应不需要加热制取气体的反应,因此不需要加热;故答案为:乙; 反应为固体与液体反应不需要加热制取气体的反应;
(3)乙炔(C2H2)是一种无色、无味、无嗅的气体,比空气轻,微溶于水,因此可以用向下排空气法和排水法收集;故答案为:向下排空气法(或排水法); 乙炔密度比空气小(乙炔微溶于水).
(4)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;收集满气体的集气瓶应该正放在桌面上,因为二氧化碳的密度比空气的密度大;二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳;故答案为:乙; CaCO3+2HCl=CaCl2+H2O+CO2↑,正;CO2+Ca(OH)2=CaCO3↓+H2O;
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的检验等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案| A. | 铜常用作导线 | B. | 干冰用于人工降雨 | ||
| C. | 氮气用作食品保护气 | D. | 金刚石用于切割大理石 |
| A. | 洗剂精可以溶解食用油 | |
| B. | 均一、稳定的液体都是溶液 | |
| C. | 溶质都以分子形式溶解在溶剂里 | |
| D. | 氢氧化钠溶于水,使溶液的温度升高 |
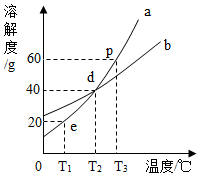
| A. | d点是表示在T2℃时,a、b的质量分数相等 | |
| B. | p点表示是在T3℃时,在100g水中最多溶解60g的a物质 | |
| C. | 在T1℃时,在60g水中加入15ga物质,得到溶液75g | |
| D. | a的溶解度大于b的溶解度 |
| A. | 火烧连营 | B. | 刻舟求剑 | C. | 大海捞针 | D. | 滴水成冰 |
| A. | 乙硫醇的相对分子质量为 62 | |
| B. | 硫元素的质量分数的计算式是$\frac{32}{12×2+1×6+32}$×100% | |
| C. | 乙硫醇中 C、H、S 三种元素的质量比为 2:6:1 | |
| D. | 在管道煤气中添加微量乙硫醇,目的是及时发现煤气泄漏 |

