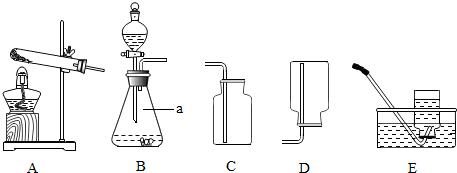
14.用盐酸和碳酸钙固体反应,将得到的气体X通入澄清石灰水中,始终没有发现石灰水变浑浊.针对此现象,同学们提出了自己的想法.
[假设]小明的假设:澄清石灰水已变质. 小白的假设:气体X中除了有CO2外,还有HCl.
[实验探究](1)小明的探究:
(2)小白的探究
[实验反思]盐酸有很强的挥发性,用它制取气体往往不纯.
[假设]小明的假设:澄清石灰水已变质. 小白的假设:气体X中除了有CO2外,还有HCl.
[实验探究](1)小明的探究:
| 实验目的 | 实验步骤 | 可能的实验现象 | 化学方程式和实验结沦 |
| 探究所用 澄清石灰 水是否变 质 | ①用一支试管另取少量原澄清石灰水 ②取稀硫酸与碳酸钠反应制取CO2 ③把二氧化碳通入澄清石灰水中 | 步骤③中现象为: 澄清石灰水变浑浊 | 步骤②中反应方程式为: Na2CO3+H2SO4═Na2SO4+H2O+CO2↑ 实验结论:所用的澄清石灰水没有变质. |
| 实验目的 | 实验步骤 | 实验现象 | 化学方程式和实验结论 |
| 探究小白的假设是否成立 | 将气体X通入AgNO3溶液 | 产生白色沉淀 | 反应方程式为:HCl+AgNO3═AgCl↓+HNO3 实验结论:小白的假设成立 |
13.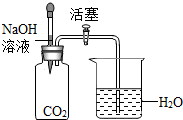 C02与NaOH溶液能发生反应,但看不到明显现象.某化学兴趣小组为验证CO2与NaOH溶液发生了反应,进行如下探究活动.
C02与NaOH溶液能发生反应,但看不到明显现象.某化学兴趣小组为验证CO2与NaOH溶液发生了反应,进行如下探究活动.
【查阅资料】
(1)CO2与NaOH反应的化学方程式为2NaOH+CO2═Na2CO3+H2O.
【设计实验】
(2)方案一:
(3)方案二:接如图所示装置进行实验.
【反思与评价】
(4)有同学认为方案二根据实验现象不能得出“CO2与NaOH溶液发生了反应”的结论,还应再做对比实验,理由是二氧化碳可以溶于水.
 C02与NaOH溶液能发生反应,但看不到明显现象.某化学兴趣小组为验证CO2与NaOH溶液发生了反应,进行如下探究活动.
C02与NaOH溶液能发生反应,但看不到明显现象.某化学兴趣小组为验证CO2与NaOH溶液发生了反应,进行如下探究活动.【查阅资料】
(1)CO2与NaOH反应的化学方程式为2NaOH+CO2═Na2CO3+H2O.
【设计实验】
(2)方案一:
| 实验操作 | 实验现象 | 结论 |
| 往盛有NaOH溶液的试管中通人CO2,然后滴人足量的氯化钙溶液 | 产生了沉淀 | CO2与NaOH溶液发生了反应 |
| 1实验操作 | 实验现象 | 结论 |
| 将氢氧化钠溶液滴入广口瓶中,然后打开活塞 | 烧杯中的水吸入集气瓶中 | CO2与NaOH溶液发生了反应 |
(4)有同学认为方案二根据实验现象不能得出“CO2与NaOH溶液发生了反应”的结论,还应再做对比实验,理由是二氧化碳可以溶于水.
12.某同学在学习了燃烧与燃料的有关知识后,注意到一张纸容易燃烧,而卷成纸团却不易燃烧,联想到细铁丝受热后,在空气中一般只产生红热现象,而在氧气中能剧烈燃烧,于是引发思考,并进行了实验探究.请你协助回答下面有关问题:
【发现问题】:可燃物燃烧的剧烈程度与哪些因素有关呢?
【提出猜想】:
猜想①:燃烧的剧烈程度可能与氧气的接触面积有关;
猜想②:燃烧的剧烈程度可能与氧气的浓度有关.
【验证猜想】:实验报告如下:
【结论应用】:请你结合工业生产或生活中的实例,就如何使燃料得到充分燃烧,而达到节约能源的目的,提出一条具体建议:增大可燃物和氧气的接触面积,或增大氧气的浓度.
【发现问题】:可燃物燃烧的剧烈程度与哪些因素有关呢?
【提出猜想】:
猜想①:燃烧的剧烈程度可能与氧气的接触面积有关;
猜想②:燃烧的剧烈程度可能与氧气的浓度有关.
【验证猜想】:实验报告如下:
| 验证猜想 | 实验操作 | 实验现象 | 实验结论 |
| 猜想① | 取两张相同的纸,其中一张卷成纸团,点燃 | 卷成纸团的纸燃烧不如没有卷成纸团的纸燃烧剧烈 | 与氧气接触面积大的纸燃烧更剧烈 |
| 猜想② | 点燃相同的两份红磷,其中一份放入盛有氧气的集气瓶中 | 放入盛有氧气的集气瓶中的红磷燃烧比空气中的红磷燃烧更剧烈 | 氧气浓度大的红磷燃烧更剧烈 |
11.某化学兴趣小组同学用大理石和盐酸反应制取CO2,将制得的气体通入澄清石灰水时,未变浑浊,便产生了好奇.对此展开了探究活动,请你参与探究并填写空格.
【提出问题】澄清石灰水未变浑浊的原因是什么?
【假设猜想】假设一:石灰水变质 假设二:制得气体中无CO2
【探究实验】为探究假设是否成立,小组同学取原试剂瓶中澄清石灰水进行如下实验:
【分析推理】通过上述探究,否定了两个假设,小组同学确定澄清石灰水未变浑浊是其他原因造成的.于是他们对反应物进行了分析,根据盐酸的挥发性,推测制得气体中有较多的HCl气体.
写出上述实验中AgNO3溶液中发生的化学反应方程式HCl+AgNO3═AgCl↓+HNO3.
【得出结论】澄清石灰水未变浑浊的原因是制得的CO2中有一定量HCl气体.有一定量HCI气体存在时,澄清石灰水为什么不变浑浊?请解释氯化氢先和氢氧化钙反应生成氯化钙和水.
【评价反思】小组中有一位同学认为【验证实验】中不能用紫色石蕊溶液证明HCI气体的存在,原因是二氧化碳能和水反应生成碳酸,碳酸能使石蕊试液变红色.
【提出问题】澄清石灰水未变浑浊的原因是什么?
【假设猜想】假设一:石灰水变质 假设二:制得气体中无CO2
【探究实验】为探究假设是否成立,小组同学取原试剂瓶中澄清石灰水进行如下实验:
| 实验操作 | 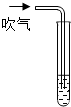 | 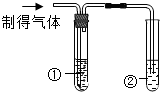 |
| 实验现象 | 澄清石灰水变浑浊 | 试管①澄清石灰水未变浑浊;试管②澄清石灰水变浑浊 |
| 实验结论 | 说明石灰水未变质 | 说明值得气体中有二氧化碳气体 |
| 实验操作 | 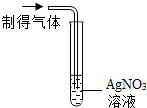 | 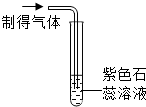 |
| 实验现象 | 出现白色沉淀 | 紫色石蕊试液变红 |
| 实验结论 | 有HCl气体 | 有HCl气体 |
【得出结论】澄清石灰水未变浑浊的原因是制得的CO2中有一定量HCl气体.有一定量HCI气体存在时,澄清石灰水为什么不变浑浊?请解释氯化氢先和氢氧化钙反应生成氯化钙和水.
【评价反思】小组中有一位同学认为【验证实验】中不能用紫色石蕊溶液证明HCI气体的存在,原因是二氧化碳能和水反应生成碳酸,碳酸能使石蕊试液变红色.
5.我国著名的闽籍制碱专家侯德榜,在纯碱制造方面做出了重大贡献.用“侯氏制碱法”制得的纯碱中常含有氯化钠等杂质,化学兴趣小组欲对某品牌纯碱样品中碳酸钠的质量分数进行实验探究,在老师的指导下,他们设计了下列两种实验方案进行试验.
资料摘要:
Ⅰ.碳酸钠和氯化钙能发生复分解反应.
Ⅱ.浓硫酸具有很强的吸水性;碱石灰常用于吸收水蒸气和二氧化碳.
[方案一]样品与氯化钙溶液反应,测定Na2CO3的质量分数
(1)样品与氯化钙溶液的反应实验(杂质不与氯化钙溶液反应):
(2)分析滴加的CaCl2溶液要过量的原因:与碳酸钠充分反应;
(3)将反应后的混合物进行过滤,把获得的沉淀物进行洗涤、干燥、称量.利用沉淀物质量计算Na2CO3的质量分数为91%.如果不洗涤沉淀物会造成测定结果大于91%,这是因为不洗涤碳酸钙,表面可能会附着一层可溶性物质使沉淀物质量增加,所以使得计算出的碳酸钠的质量增大.
[方案二]样品与稀盐酸反应,测定Na2CO3的质量分数
利用下图所示实验装置(铁架台略去)和试剂,通过测定样品和稀盐酸反应产生的CO2气体的质量,计算Na2CO3的质量分数(装置气密性良好,忽略盐酸的挥发性且每步反应或作用都是完全的).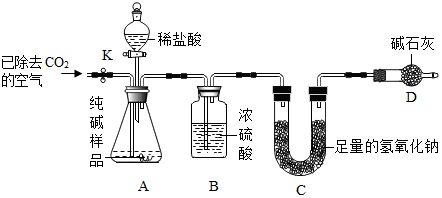
(4)打开止水夹K,先对装置A和B(已连接)通入已除去CO2的空气一会儿,以排尽装置A和B中含有的二氧化碳,再接上装置C和D.
(5)关闭止水夹K,加入足量的稀盐酸(杂质不与盐酸反应),装置A中样品产生气体的化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(6)待装置A中的反应结束后,再一次打开止水夹K,继续往装置通入已除去CO2的空气一会儿.根据质量守恒 定律,装置质量守恒(填标号)在反应前后的质量差就是产生CO2的质量,由此计算出该样品中Na2CO3的质量分数.若没有装置D,将会使测定结果偏大(选填“偏大”或“偏小”).
0 150587 150595 150601 150605 150611 150613 150617 150623 150625 150631 150637 150641 150643 150647 150653 150655 150661 150665 150667 150671 150673 150677 150679 150681 150682 150683 150685 150686 150687 150689 150691 150695 150697 150701 150703 150707 150713 150715 150721 150725 150727 150731 150737 150743 150745 150751 150755 150757 150763 150767 150773 150781 211419
资料摘要:
Ⅰ.碳酸钠和氯化钙能发生复分解反应.
Ⅱ.浓硫酸具有很强的吸水性;碱石灰常用于吸收水蒸气和二氧化碳.
[方案一]样品与氯化钙溶液反应,测定Na2CO3的质量分数
(1)样品与氯化钙溶液的反应实验(杂质不与氯化钙溶液反应):
| 实验操作 | 实验现象 | 实验结论 |
| 取一定量纯碱样品配成溶液后,滴加过量的CaCl2溶液. | 产生白色沉淀 | 反应的化学方程式: Na2CO3+CaCl2═CaCO3↓+2NaCl |
(3)将反应后的混合物进行过滤,把获得的沉淀物进行洗涤、干燥、称量.利用沉淀物质量计算Na2CO3的质量分数为91%.如果不洗涤沉淀物会造成测定结果大于91%,这是因为不洗涤碳酸钙,表面可能会附着一层可溶性物质使沉淀物质量增加,所以使得计算出的碳酸钠的质量增大.
[方案二]样品与稀盐酸反应,测定Na2CO3的质量分数
利用下图所示实验装置(铁架台略去)和试剂,通过测定样品和稀盐酸反应产生的CO2气体的质量,计算Na2CO3的质量分数(装置气密性良好,忽略盐酸的挥发性且每步反应或作用都是完全的).

(4)打开止水夹K,先对装置A和B(已连接)通入已除去CO2的空气一会儿,以排尽装置A和B中含有的二氧化碳,再接上装置C和D.
(5)关闭止水夹K,加入足量的稀盐酸(杂质不与盐酸反应),装置A中样品产生气体的化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(6)待装置A中的反应结束后,再一次打开止水夹K,继续往装置通入已除去CO2的空气一会儿.根据质量守恒 定律,装置质量守恒(填标号)在反应前后的质量差就是产生CO2的质量,由此计算出该样品中Na2CO3的质量分数.若没有装置D,将会使测定结果偏大(选填“偏大”或“偏小”).
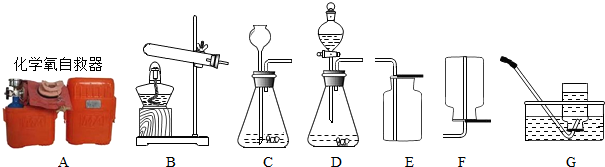
 阅读材料,回答问题:
阅读材料,回答问题: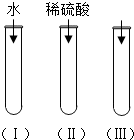 氧化铜(CuO)是一种黑色固体,可溶于稀硫酸中.某同学想知道是稀硫酸中的H2O、H+和SO42-中的哪种粒子能使氧化铜溶解.请你和他一起通过如图所示三个实验来完成这次探究活动
氧化铜(CuO)是一种黑色固体,可溶于稀硫酸中.某同学想知道是稀硫酸中的H2O、H+和SO42-中的哪种粒子能使氧化铜溶解.请你和他一起通过如图所示三个实验来完成这次探究活动