题目内容
7.化学反应方程式“4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5”表示( )| A. | 磷加氧气生成五氧化二磷 | |
| B. | 磷和氧气混合后生成五氧化二磷 | |
| C. | 4个磷原子加10个氧原子等于2个五氧化二磷分子 | |
| D. | 4个磷原子与5个氧分子在点燃条件下反应生成2个五氧化二磷分子 |
分析 化学方程式可表示:反应物和生成物的种类;反应的条件;反应物和生成物的微观粒子个数比;反应物和生成物的质量比等.但要注意读化学方程式时,“+”应读作“和”,“═”应读作“生成”..
解答 解:A.在化学方程式中的“+”读作“和”而不是“加”,故错误;
B.该反应表示磷和氧气在点燃的条件下反应生成五氧化二磷,而不是简单地混合,故错误;
C.该反应表示从微观上,在点燃条件下,每4个磷原子与5个氧分子反应生成2个五氧化二磷,故错误;
D.4个磷原子与5个氧分子在点燃条件下反应生成2个五氧化二磷分子,故正确.
故选D.
点评 本题难度不大,化学方程式是最重要的化学用语之一,掌握化学方程式的含义、了解方化学程式的读法是正确解答此类题的关键.

练习册系列答案
相关题目
17.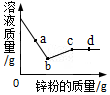 向一定量硝酸银和硝酸铜的混合溶液中加入锌粉,所得溶液的质量与加入锌粉的质量关系如图所示.下列说法正确的是( )
向一定量硝酸银和硝酸铜的混合溶液中加入锌粉,所得溶液的质量与加入锌粉的质量关系如图所示.下列说法正确的是( )
 向一定量硝酸银和硝酸铜的混合溶液中加入锌粉,所得溶液的质量与加入锌粉的质量关系如图所示.下列说法正确的是( )
向一定量硝酸银和硝酸铜的混合溶液中加入锌粉,所得溶液的质量与加入锌粉的质量关系如图所示.下列说法正确的是( )| A. | a点所得溶液中的溶质是硝酸铜、硝酸锌 | |
| B. | 向b点所得固体中加入盐酸有气泡产生 | |
| C. | c点所得固体为银和铜 | |
| D. | d点所得溶液中溶质一定有硝酸锌,可能有硝酸铜 |
15.下列化学方程式符合题意且书写正确的是( )
| A. | 正常的雨水略呈酸性的原因:CO2+H2O═H2CO3 | |
| B. | 生活中用天然气作燃料:C2H5OH+3O2 $\frac{\underline{\;点燃\;}}{\;}$ 2CO2+3H2O | |
| C. | 胃舒平(含氢氧化铝)治疗胃酸过多症:Al(OH)3+HCl═AlCl3+H2O | |
| D. | 用大理石和盐酸制取二氧化碳:CaCO3+2HCl═CaCl2+H2O+CO2 |
12.利用沉淀法可测定某粗盐样品的纯度(假定粗盐中的杂质全部是MgCl2).每次取1000g样品配制成溶液,向其中加10%的氢氧化钠溶液,测得生成沉淀的质量与所加氢氧化钠溶液的质量关系如下表所示:
(1)可求得粗盐的纯度是90.5%.
(2)在第三次实验中所得溶液的溶质有NaOH和NaCl.
(3)当加入800克10%的氢氧化钠溶液时恰好和1000克样品中的杂质MgCl2完全反应,此时溶液中氯化钠的质量为1022g.
| 测定次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 样品质量(g) | 1000 | 1000 | 1000 | 1000 |
| 氢氧化钠溶液质量(g) | 320 | 640 | 820 | 900 |
| 沉淀质量(g) | 23.2 | 46.4 | 58 | 58 |
(2)在第三次实验中所得溶液的溶质有NaOH和NaCl.
(3)当加入800克10%的氢氧化钠溶液时恰好和1000克样品中的杂质MgCl2完全反应,此时溶液中氯化钠的质量为1022g.
19.下列认识或说法中正确的是( )
| A. | 向某固体中加入稀盐酸有气泡产生,可证明该物质中一定含有CO32- | |
| B. | 可用过量的Cu(OH)2除去CuSO4溶液中少量的H2SO4 | |
| C. | 常温下可用Fe与AgCl反应制取Ag | |
| D. | 将Fe、Cu、Ag放入稀盐酸中,可确定它们的活动性顺序 |
16.金属Ti(钛)是一种具有许多优良性能的较为昂贵的金属,钛和钛合金被认为是21世纪的重要金属材料.某科学兴趣小组在实验室探究Ti、Mg、Cu的活泼性顺序.他们在相同温度下,取大小相同的三种金属薄片,分别投入等体积等浓度足量稀盐酸中,观察现象如下:
下列有关三种金属的说法正确的是( )
| 金 属 | Ti | Mg | Cu |
| 金属表面现象 | 放出气泡速度缓慢 | 放出气泡速度快 | 无变化 |
| A. | 三种金属的活泼性由强到弱的顺序是:Ti、Mg、Cu | |
| B. | 温度、金属表面积、盐酸浓度等因素都会影响反应速率 | |
| C. | 用Ti从CuSO4溶液中置换出Cu是工业制取Cu的很好途径 | |
| D. | 若Ti粉中混有Mg,提纯Ti时可用稀盐酸除去Mg |

 碳酸氢钠(NaHCO3)俗称小苏打,常用于食品和医药工业.某科学兴趣小组的同学对碳酸氢钠的性质进行探究:碳酸氢钠的热稳定性.
碳酸氢钠(NaHCO3)俗称小苏打,常用于食品和医药工业.某科学兴趣小组的同学对碳酸氢钠的性质进行探究:碳酸氢钠的热稳定性.