题目内容
17.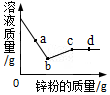 向一定量硝酸银和硝酸铜的混合溶液中加入锌粉,所得溶液的质量与加入锌粉的质量关系如图所示.下列说法正确的是( )
向一定量硝酸银和硝酸铜的混合溶液中加入锌粉,所得溶液的质量与加入锌粉的质量关系如图所示.下列说法正确的是( )| A. | a点所得溶液中的溶质是硝酸铜、硝酸锌 | |
| B. | 向b点所得固体中加入盐酸有气泡产生 | |
| C. | c点所得固体为银和铜 | |
| D. | d点所得溶液中溶质一定有硝酸锌,可能有硝酸铜 |
分析 锌比铜活泼,铜比银活泼,向一定质量AgNO3和Cu(NO3)2的混合溶液中加入锌粉,锌先和硝酸银反应,如果反应后锌过量,则再和硝酸铜反应;
锌和硝酸银、硝酸铜反应的化学方程式及其质量关系为:
Zn+2AgNO3=Zn(NO3)2+2Ag,
65 216
Zn+Cu(NO3)2=Zn(NO3)2+Cu,
65 64
由以上质量关系可知,锌和硝酸银反应后溶液质量减小,和硝酸铜反应后溶液质量增大,即从开始反应至b点时,是锌和硝酸银反应,b-c点时是锌和硝酸铜反应.
解答 解:A、a点时锌和部分硝酸银反应,溶液中的溶质有:反应生成的硝酸锌、剩余的硝酸银和没有反应的硝酸铜,故错误;
B、b点时锌和硝酸银恰好反应,固体中只有银一种物质,加入盐酸没有气泡产生,故错误;
C、b~c段是锌和硝酸铜反应,c点表示锌和硝酸铜恰好反应,所得固体为银和铜,故正确;
D、d点表示锌过量,所得溶液中溶质只有硝酸锌,故错误.
故选:C.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案
相关题目
8.下列物质的化学式与名称表示一致并且书写正确的是( )
| A. | NH4HCO3--碳酸氢氧 | B. | CaO--熟石灰 | ||
| C. | NaOH--纯碱 | D. | CO(NH2)2--尿素 |
5.2017年我国在可燃冰开采技术上取得了世界性的突破.可燃冰分解出的甲烷属于( )
| A. | 混合物 | B. | 单质 | C. | 氧化物 | D. | 有机物 |
12.下列实验现象的描述正确的是( )
| A. | 碳在氧气中燃烧发出白光,产生白烟 | |
| B. | 铁丝在氧气中燃烧火星四射,生成黑色固体 | |
| C. | 将铁丝伸入稀盐酸中,溶液变成黄色 | |
| D. | 铝丝伸入硫酸铜溶液中,铝的表面有铜析出 |
9.兴趣活动小组设计并完成了如下实验(装置气密性良好,药品足量):
| 操作 | 现象 | 结论 | 装置 |
| 实验一: 同时将Ⅰ中5mL5%的过氧化氢溶液和Ⅱ中5mL15%的过氧化氢溶液注入各盛有0.5g二氧化锰的甲、乙中,关闭弹簧夹. | 发现烧杯中右侧导管口产生气泡的速率比左侧快. | 化学反应速率与 反应物浓度有关; 该反应的化学方程式为 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑. | 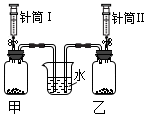 |
| 操作 | 现象 | 现象分析 | 装置 |
| 实验二: 先将稀盐酸注入甲,关闭弹簧夹;再将水注入乙,关闭弹簧夹. 注意:注入液体后,甲、乙导管口均处于液面以下. | 甲中液体先流入烧杯,乙中液体后流入烧杯,然后观察到烧杯中先无明显现象,后有白色沉淀产生. | 乙中液体流入烧杯的原因是 氢氧化钠溶于水,放出热量,使得瓶内压强大于外界压强; 甲中流入烧杯的液体溶质的化学式是 MgCl2HCl. | 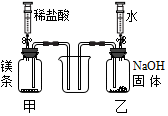 |
6.氯化钠的下列用途中,主要反映其具有杀菌防腐作用的是( )
| A. | 制生理盐水 | B. | 作调味剂 | C. | 腌制鱼肉 | D. | 制取氢氧化钠 |
7.化学反应方程式“4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5”表示( )
| A. | 磷加氧气生成五氧化二磷 | |
| B. | 磷和氧气混合后生成五氧化二磷 | |
| C. | 4个磷原子加10个氧原子等于2个五氧化二磷分子 | |
| D. | 4个磷原子与5个氧分子在点燃条件下反应生成2个五氧化二磷分子 |