题目内容
11.氯化钙在生活中常用作干燥剂、融雪剂,在工业上可用于制造防冻液等.某工厂以石灰石为原料生产二水合氯化钙(CaCl2•2H2O)的流程如下.原料石灰石中含有的杂质主要是MgCO3、SiO2和Fe2O3.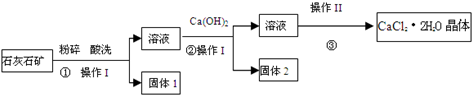
(1)第①步酸洗所用的酸是A(填编号).
A.稀盐酸 B.稀硫酸 C.浓硫酸 D.稀硝酸
(2)酸洗时酸与Fe2O3反应的化学方程式是Fe2O3+6HCl═2FeCl3+3H2O.
(3)固体2中一定含有的物质的名称是氢氧化镁和氢氧化铁.
(4)实验室中操作I所用到的玻璃仪器有:玻璃棒、烧杯、漏斗.
(5)操作Ⅱ的名称是:蒸发浓缩、降温结晶.
分析 (1)根据反应前后元素种类不变,结合生成物判断反应物;
(2)根据氧化铁和盐酸反应生成氯化铁和水进行分析;
(3)根据二氧化硅与盐酸不反应进行分析;
(4)根据过滤用到的仪器进行分析;
(5)根据从溶液中结晶的过程分析.
解答 解:(1)整个流程是用石灰石制取二水合氯化钙(CaCl2•2H2O),生成物中含有氯元素,反应物中也应有氯元素,因此用的酸为盐酸,故选:A;
(2)盐酸与氧化铁反应生成氯化铁和水,化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O;
(3)二氧化硅与盐酸不反应,过滤可得到二氧化硅固体;
(4)操作Ⅰ将固体与液体分离,方法为过滤,过滤用到的玻璃仪器有玻璃棒、烧杯和漏斗;
(5)操作Ⅱ是将液体蒸发浓缩,后降温结晶,即得二水合氯化钙固体.
故答案为:(1)A;
(2)Fe2O3+6HCl═2FeCl3+3H2O;
(3)氢氧化镁和氢氧化铁;
(4)漏斗;
(5)降温结晶.
点评 紧扣生产目的分析生产流程图,明确流程图中各操作在生产过程中的作用,整体把握生产过程,这是解答所提出的问题的基础.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案
相关题目
1.某化学兴趣小组进行以下实验:
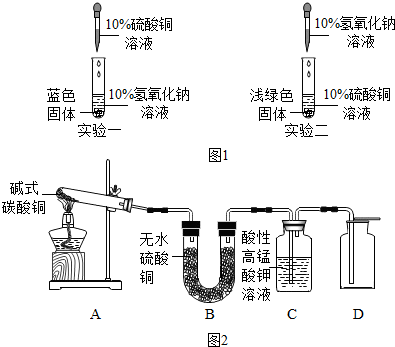
【提出问题】实验一和实验二中,现象为何不同?
【查阅资料】氢氧化钠溶液和硫酸铜溶液反应会生成蓝色的氢氧化铜,但当硫酸铜溶液过量时,也会生成浅绿色的碱式硫酸铜.
【分析讨论】下列说法正确的是ABC(填字母).
A.加热实验一反应后生成的物质,出现黑色固体
B.实验二中生成了碱式硫酸铜
C.根据实验一和实验二可知,反应物相同时,反应物的量不同,产物可能不同
D.根据实验一和实验二可知,反应物相同时,反应条件不同,产物可能不同
【继续探究】该小组同学对碱式硫酸铜产生了兴趣,通过以下实验探究碱式硫酸铜受热分解的产物.(已知:无水硫酸铜遇H2O变蓝;SO2能使酸性高锰酸钾溶液褪色.)
【拓展延伸】
(1)若实验二中得到的碱式硫酸铜化学式为CuSO4•3Cu(OH)2,将该碱式硫酸铜浸泡在过量的氢氧化钠溶液中,密封放置一天后,固体全部变为蓝色.写出此反应的化学方程式:CuSO4•3Cu(OH)2+2NaOH=4Cu(OH)2+Na2SO4.
(2)取12.9g某种碱式硫酸铜[化学式可表示为xCuSO4•yCu(OH)2],加热完全分解后生成0.9g水,则x:y=1:1.
(30取2份等质量的某种碱式硫酸铜[化学式可表示为xCuSO4•yCu(OH)2],一份加热完全分解后生成4.8g氧化铜,另一份可与20g质量分数为19.6%的稀硫酸恰好完全反应,则该碱式硫酸铜的化学式为CuSO4•2Cu(OH)2.

【提出问题】实验一和实验二中,现象为何不同?
【查阅资料】氢氧化钠溶液和硫酸铜溶液反应会生成蓝色的氢氧化铜,但当硫酸铜溶液过量时,也会生成浅绿色的碱式硫酸铜.
【分析讨论】下列说法正确的是ABC(填字母).
A.加热实验一反应后生成的物质,出现黑色固体
B.实验二中生成了碱式硫酸铜
C.根据实验一和实验二可知,反应物相同时,反应物的量不同,产物可能不同
D.根据实验一和实验二可知,反应物相同时,反应条件不同,产物可能不同
【继续探究】该小组同学对碱式硫酸铜产生了兴趣,通过以下实验探究碱式硫酸铜受热分解的产物.(已知:无水硫酸铜遇H2O变蓝;SO2能使酸性高锰酸钾溶液褪色.)
| 装置 | 操作及现象 | 分解产物 |
| A | 试管中出现黑色固体,将黑色固体溶于稀硫酸,溶液呈蓝色 | CuO |
| B | U形管中出现蓝色固体 | H2O |
| C | 溶液颜色褪去 | SO2 |
| D | 将带火星的木条伸入集气瓶中,木条复燃 | O2 |
(1)若实验二中得到的碱式硫酸铜化学式为CuSO4•3Cu(OH)2,将该碱式硫酸铜浸泡在过量的氢氧化钠溶液中,密封放置一天后,固体全部变为蓝色.写出此反应的化学方程式:CuSO4•3Cu(OH)2+2NaOH=4Cu(OH)2+Na2SO4.
(2)取12.9g某种碱式硫酸铜[化学式可表示为xCuSO4•yCu(OH)2],加热完全分解后生成0.9g水,则x:y=1:1.
(30取2份等质量的某种碱式硫酸铜[化学式可表示为xCuSO4•yCu(OH)2],一份加热完全分解后生成4.8g氧化铜,另一份可与20g质量分数为19.6%的稀硫酸恰好完全反应,则该碱式硫酸铜的化学式为CuSO4•2Cu(OH)2.
3.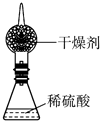 为测定锌铜合金中锌的含量,取该合金放入右图所示盛有稀硫酸的锥形瓶中,发生反应:Zn+H2SO4═ZnSO4+H2↑.多次实验后,取平均值所得数据如下表:
为测定锌铜合金中锌的含量,取该合金放入右图所示盛有稀硫酸的锥形瓶中,发生反应:Zn+H2SO4═ZnSO4+H2↑.多次实验后,取平均值所得数据如下表:
若不考虑干燥剂吸收空气中的水蒸气,计算:
(1)若不用干燥剂,则测得锌的质量分数会偏大;
(2)该合金中锌的质量分数.
 为测定锌铜合金中锌的含量,取该合金放入右图所示盛有稀硫酸的锥形瓶中,发生反应:Zn+H2SO4═ZnSO4+H2↑.多次实验后,取平均值所得数据如下表:
为测定锌铜合金中锌的含量,取该合金放入右图所示盛有稀硫酸的锥形瓶中,发生反应:Zn+H2SO4═ZnSO4+H2↑.多次实验后,取平均值所得数据如下表:| 反应前 | 充分反应后装置及 反应剩余物质质量 | |
| 装置和足量的稀硫酸质量 | 锌铜合金质量 | |
| 342.10g | 16.00g | 357.70g |
(1)若不用干燥剂,则测得锌的质量分数会偏大;
(2)该合金中锌的质量分数.
 化学与生产、生活息息相关,请你用所学知识回答下列问题:
化学与生产、生活息息相关,请你用所学知识回答下列问题: