题目内容
20.发酵粉是糕点的常见蓬松剂,成分一般是NH4HCO3、NaHCO3.某同学将发酵粉加入到一定量的氢氧化钙饱和溶液中,产生大量气泡和白色固体,溶液呈无色.(一)为确定气体和固体及溶液的成分,该同学进行了如下的探究:
(1)将气体通入紫色石蕊试液中,石蕊试液变蓝色.则该气体为NH3(写化学式),生成该气体的化学方程式是NH4HCO3+Ca(OH)2=CaCO3↓+2H2O+NH3↑.
(2)对白色固体做出如下猜测并进行实验:
【猜测】
①白色固体是CaCO3;②白色固体是Ca (OH)2;③白色固体是CaCO3和Ca (OH)2.
【实验】
取洗净后的白色固体,加入足量的水,滴入酚酞,无明显变化,则白色固体一定是CaCO3.
(3)将所得溶液分为两份:
①一份中加足量的稀盐酸,无气体;
②在另一份中通入足量的CO2后,滴入酚酞.生成白色沉淀且溶液呈红色.则原
溶液中有溶质Ca(OH)2、NaOH(写化学式).
(二)为确定发酵粉成分含量,该同学进行了定量实验:
(4)称取干燥的白色固体10g,充分加热至质量不再改变为止,称得残留固体质量为5.3g.则发酵粉中NH4HCO3与NaHCO3的质量比为4:21.
分析 (一)氨气溶于水形成氨水,氨水显碱性,能使石蕊试液变蓝色;
碳酸氢铵和氢氧化钙反应生成碳酸钙、水和氨气;
氢氧化钙和氢氧化钠的水溶液显碱性,能使酚酞试液变红色;
二氧化碳能和氢氧化钙反应生成白色沉淀碳酸钙和水;
(二)碳酸氢铵受热分解生成氨气、水和二氧化碳,碳酸氢钠受热分解生成碳酸钠、水和二氧化碳,根据反应的化学方程式和提供的数据可以进行相关方面的计算.
解答 解:(1)将气体通入紫色石蕊试液中,石蕊试液变蓝色,说明气体是氨气,氨气的化学式是NH3;
生成该气体的化学方程式是:NH4HCO3+Ca(OH)2=CaCO3↓+2H2O+NH3↑.
故填:NH3;NH4HCO3+Ca(OH)2=CaCO3↓+2H2O+NH3↑.
(2)取洗净后的白色固体,加入足量的水,滴入酚酞,无明显变化,则白色固体一定是CaCO3.
故填:CaCO3.
(3)①一份中加足量的稀盐酸,无气体,说明溶液中不含有碳酸钠;
②在另一份中通入足量的CO2后,滴入酚酞,生成白色沉淀且溶液呈红色,说明原溶液中含有Ca (OH)2和NaOH.
故填:Ca (OH)2;NaOH.
(4)设碳酸氢钠的质量为x,
充分加热至质量不再改变为止,称得残留固体质量为5.3g,说明碳酸氢钠分解生成碳酸钠的质量是5.3g,
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,
168 106
x 5.3g
$\frac{168}{x}$=$\frac{106}{5.3g}$,
x=8.4g,
则发酵粉中NH4HCO3与NaHCO3的质量比为:(10g-8.4g):8.4g=4:21.
故填:4:21.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

| A. | 中和反应生成盐和水,生成盐和水的反应不一定是中和反应 | |
| B. | 酸溶液具有酸性,酸性溶液不一定是酸溶液 | |
| C. | 化肥中加熟石灰研磨,没有刺激性气味,一定不是氮肥 | |
| D. | 油脂和淀粉组成元素相同,但分子结构不同 |
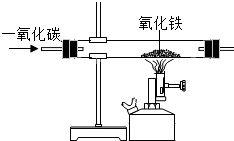 如图是“一氧化碳与氧化铁反应”的部分实验装置,关于该实验说法正确的是( )
如图是“一氧化碳与氧化铁反应”的部分实验装置,关于该实验说法正确的是( )| A. | 该实验的反应原理是FeO+CO$\frac{\underline{\;高温\;}}{\;}$ Fe+CO2 | |
| B. | 在实验过程中,黑色的粉末会逐渐变成红色 | |
| C. | 充分反应后,向固体中加稀盐酸会产生气泡 | |
| D. | 在实验过程中,产生的尾气可以直接排放到空气中 |
①千里冰封,万里雪飘
②白玉为床,金作马
③野火烧不尽,春风吹又生
④粉骨碎身浑不怕,要留清白在人间
⑤夜来风雨声,花落知多少
⑥春蚕到死丝方尽,蜡炬成灰泪始干.
| A. | ①③⑤ | B. | ②④⑥ | C. | ①③④⑤ | D. | ③④⑥ |

| A. | 空气是一种混合物 | B. | 氮气沸点比氧气高 | ||
| C. | 该过程属于物理变化 | D. | 氧气由氧分子构成 |