题目内容
8.小红和小丽在探究碱的化学性质时,将稀盐酸滴入到氢氧化钠溶液中,意外地看到有气泡产生,她认为氢氧化钠溶液 已经变质了.用化学方程式表示氢氧化钠溶液变质的原因:CO2+2NaOH=Na2CO3+H2O.【提出问题】变质后的氢氧化钠溶液中的溶质是什么?
【猜想假设】小丽对变质后的氢氧化钠溶液中的溶质成分做出了两种猜想:
猜想一:碳酸钠;
猜想二:NaOH和Na2CO3.
【实验设计】为验证上述猜想哪个正确,小丽设计了如下方案:取少量氢氧化钠溶液样品于试管中,滴加几滴无色酚酞溶液,观察溶液颜色变化.小红认为小丽的实验方案不合理,理由是:碳酸钠和氢氧化钠溶液都能使酚酞变红色
【实验与结论】小红另外设计并完成了实验,请你帮她填写下面的实验报告:
| 实验步骤 | 实验现象 | 结论 |
| 步骤1:取少量氢氧化钠溶液样品于试管中,向其中滴加过量的氯化钙溶液 | 有白色沉淀生成 | 猜想一 正确 |
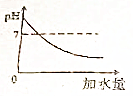
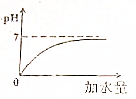
| 步骤2:取步骤1反应后的溶液测定溶液的pH,具体方法是把pH试纸放在洁净的玻璃片上,用玻璃棒蘸 取待测液滴到pH试纸上将试纸显示的颜色与标准比色卡比较 | pH=7 |
分析 氢氧化钠溶液能吸收空气中的二氧化碳并发生反应生成碳酸钠和水,写出反应的方程式;
【猜想假设】根据变质后的氢氧化钠溶液可能是部分变质,也可能是全部变质进行猜想;
【实验设计】根据氢氧化钠和碳酸钠的水溶液都呈碱性进行分析;
【实验与结论】要证明氢氧化钠变质的程度,应该先除去氢氧化钠中的碳酸钠,然后再证明剩余溶液是否碱性;
解答 解:氢氧化钠溶液能吸收空气中的二氧化碳并发生反应生成碳酸钠和水,反应的方程式为:CO2+2NaOH=Na2CO3+H2O;
【猜想假设】变质后的氢氧化钠溶液可能是部分变质,含有碳酸钠和氢氧化钠;也可能是全部变质则含有碳酸钠;
【实验设计】无论氢氧化钠是否变质,酚酞试液都会变成红色,因为氢氧化钠和碳酸钠的水溶液都呈碱性;
【实验与结论】步骤1:取少量氢氧化钠溶液样品于试管中,向其中滴加过量的氯化钙溶液,有白色沉淀生成;
步骤2:取步骤1反应后的溶液测定溶液的pH,具体方法是把pH试纸放在洁净的玻璃片上,用玻璃棒蘸取待测液滴到pH试纸上将试纸显示的颜色与标准比色卡比较,pH=7;猜想一正确.
答案:
2NaOH+CO2═Na2CO3+H2O;
【猜想假设】碳酸钠和氢氧化钠
【实验设计】碳酸钠和氢氧化钠溶液都能使酚酞变红色;
【实验与结论】
| 实验步骤 | 实验现象 | 结论 |
| 步骤1:取少量氢氧化钠溶液样品于试管中,向其中滴加过量的氯化钙溶液 | 有白色沉淀生成 | 猜想一 正确 |
| 步骤2:取步骤1反应后的溶液测定溶液的pH,具体方法是 把pH试纸放在洁净的玻璃片上,用玻璃棒蘸 取待测液滴到pH试纸上将试纸显示的颜色与标准比色卡比较 | pH=7 |
点评 此题是一道关于氢氧化钠变质程度的实验探究题,解题的关键是把握在证明氢氧化钠部分变质时,先除去氢氧化钠中的碳酸钠,然后再证明剩余溶液显碱性,才能说明氢氧化钠部分变质.

练习册系列答案
相关题目
19.下列实验方案中,设计合理的是( )
| A. | 检验氢气中是否含有氧气,用带火星的木条检验 | |
| B. | 除去铜粉中的木炭粉:将混合物在空气中充分灼烧 | |
| C. | 鉴别氢氧化钠和硝酸铵:取样,分别溶于水并测温度变化 | |
| D. | 分离CO2和CO:强混合气体通过足量的氢氧化钠溶液,再通过浓硫酸 |
3.金属钠的化学性质非常活泼它可以与冷水发生反应,下列物质可能是钠与水反应生成物的是( )
| A. | CO2 | B. | Cl2 | C. | Na2CO3 | D. | NaOH |


 如图是a、b、c三种物质(均不含结晶水)的溶解度曲线.
如图是a、b、c三种物质(均不含结晶水)的溶解度曲线. 如图表示某化学反应的微观示意图.(“○”和“●”分别代表不同元素的原子)
如图表示某化学反应的微观示意图.(“○”和“●”分别代表不同元素的原子) 清明时节,春暖花开,同学们相约踏青野炊.活动一:观赏大片油菜花生态旅游区.活动二:就近挑选合适地点野炊.请利用所学化学知识解释下列的问题.
清明时节,春暖花开,同学们相约踏青野炊.活动一:观赏大片油菜花生态旅游区.活动二:就近挑选合适地点野炊.请利用所学化学知识解释下列的问题.