题目内容
19.下列实验方案中,设计合理的是( )| A. | 检验氢气中是否含有氧气,用带火星的木条检验 | |
| B. | 除去铜粉中的木炭粉:将混合物在空气中充分灼烧 | |
| C. | 鉴别氢氧化钠和硝酸铵:取样,分别溶于水并测温度变化 | |
| D. | 分离CO2和CO:强混合气体通过足量的氢氧化钠溶液,再通过浓硫酸 |
分析 氢气和氧气混合达到一定程度时,遇明火或加热会发生爆炸;
加热条件下,铜能和空气中的氧气反应生成氧化铜,炭粉能和空气中的氧气反应生成二氧化碳;
氢氧化钠溶于水放热,硝酸铵溶于水吸热;
氢氧化钠能和二氧化碳反应生成碳酸钠和水.
解答 解:A、氢气和氧气混合达到一定程度时,遇明火或加热会发生爆炸,因此不能用带火星的木条检验氢气中是否含有氧气;
B、加热条件下,铜能和空气中的氧气反应生成氧化铜,炭粉能和空气中的氧气反应生成二氧化碳,因此不能用在空气中充分灼烧的方法除去铜粉中的木炭粉;
C、氢氧化钠溶于水放热,硝酸铵溶于水吸热,因此可以用取样,分别溶于水并测温度变化的方法鉴别氢氧化钠和硝酸铵;
D、氢氧化钠能和二氧化碳反应生成碳酸钠和水,因此不能用将混合气体通过足量的氢氧化钠溶液,再通过浓硫酸的方法分离二氧化碳和一氧化碳.
故选:C.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
10.下列关于实验现象的描述正确的是( )
| A. | 硫在空气中燃烧产生蓝紫色的火焰 | B. | 铁在氧气中燃烧生成四氧化三铁 | ||
| C. | 红磷燃烧产生大量的白色烟雾 | D. | 木炭在氧气中燃烧发出白光 |
14.下列有关湿衣服晾干的说法中,正确的是( )
| A. | 发生了化学变化 | B. | 是水分子不断运动的结果 | ||
| C. | 水分子变成了氢分子和氧分子 | D. | 水分子的体积变小了 |
4.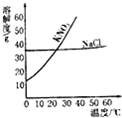 根据给出的KNO3和NaCl两种物质的溶解度表,溶解度曲线,回答问题.
根据给出的KNO3和NaCl两种物质的溶解度表,溶解度曲线,回答问题.
(1)在20℃时,KNO3的溶解度是31.6g.
(2)从海水中提取氯化钠,通常采用蒸发溶剂的方法,而不采用冷却热饱和溶液的方法,主要原因是氯化钠的溶解度受温度影响变化很小.
(3)将180gKNO3跟20gNaCl的混合物放入100g60℃的水中,充分搅拌,在降温到20℃,有大量晶体析出,下列说法中,正确的是AB.
A.析出的晶体只有KNO3 B.60℃时有部分KNO3与溶液共存
C.降温到20℃时溶液中的溶质只有NaCl D.20℃时的溶液是NaCl的饱和溶液.
 根据给出的KNO3和NaCl两种物质的溶解度表,溶解度曲线,回答问题.
根据给出的KNO3和NaCl两种物质的溶解度表,溶解度曲线,回答问题.| 0 | 20 | 40 | 60 | 80 | 100 | |
| KNO3 | 13.3 | 31.6 | 63.6 | 110 | 169 | 246 |
| NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
(2)从海水中提取氯化钠,通常采用蒸发溶剂的方法,而不采用冷却热饱和溶液的方法,主要原因是氯化钠的溶解度受温度影响变化很小.
(3)将180gKNO3跟20gNaCl的混合物放入100g60℃的水中,充分搅拌,在降温到20℃,有大量晶体析出,下列说法中,正确的是AB.
A.析出的晶体只有KNO3 B.60℃时有部分KNO3与溶液共存
C.降温到20℃时溶液中的溶质只有NaCl D.20℃时的溶液是NaCl的饱和溶液.
8.小红和小丽在探究碱的化学性质时,将稀盐酸滴入到氢氧化钠溶液中,意外地看到有气泡产生,她认为氢氧化钠溶液 已经变质了.用化学方程式表示氢氧化钠溶液变质的原因:CO2+2NaOH=Na2CO3+H2O.
【提出问题】变质后的氢氧化钠溶液中的溶质是什么?
【猜想假设】小丽对变质后的氢氧化钠溶液中的溶质成分做出了两种猜想:
猜想一:碳酸钠;
猜想二:NaOH和Na2CO3.
【实验设计】为验证上述猜想哪个正确,小丽设计了如下方案:取少量氢氧化钠溶液样品于试管中,滴加几滴无色酚酞溶液,观察溶液颜色变化.小红认为小丽的实验方案不合理,理由是:碳酸钠和氢氧化钠溶液都能使酚酞变红色
【实验与结论】小红另外设计并完成了实验,请你帮她填写下面的实验报告:
【提出问题】变质后的氢氧化钠溶液中的溶质是什么?
【猜想假设】小丽对变质后的氢氧化钠溶液中的溶质成分做出了两种猜想:
猜想一:碳酸钠;
猜想二:NaOH和Na2CO3.
【实验设计】为验证上述猜想哪个正确,小丽设计了如下方案:取少量氢氧化钠溶液样品于试管中,滴加几滴无色酚酞溶液,观察溶液颜色变化.小红认为小丽的实验方案不合理,理由是:碳酸钠和氢氧化钠溶液都能使酚酞变红色
【实验与结论】小红另外设计并完成了实验,请你帮她填写下面的实验报告:
| 实验步骤 | 实验现象 | 结论 |
| 步骤1:取少量氢氧化钠溶液样品于试管中,向其中滴加过量的氯化钙溶液 | 有白色沉淀生成 | 猜想一 正确 |
| 步骤2:取步骤1反应后的溶液测定溶液的pH,具体方法是把pH试纸放在洁净的玻璃片上,用玻璃棒蘸 取待测液滴到pH试纸上将试纸显示的颜色与标准比色卡比较 | pH=7 |
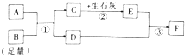 A-F是初中化学常见的物质,其中A为天然气的主要成分,F是大理石的主要成分,这些物质的相互转化关系如图所示,其中部分生成物和反应条件已省略.
A-F是初中化学常见的物质,其中A为天然气的主要成分,F是大理石的主要成分,这些物质的相互转化关系如图所示,其中部分生成物和反应条件已省略.