题目内容
9.将一定浓度的NaOH溶液加水稀释,则其pH与所加水的体积V的关系图正确的是( )| A. | 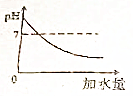 | B. | 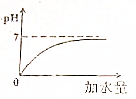 | C. |  | D. |  |
分析 氢氧化钠溶液显碱性,pH大于7;将一定浓度的NaOH溶液加水稀释,结合当溶液的pH大于7时,呈碱性,且pH越大,碱性越强;进行分析判断.
解答 解:氢氧化钠溶液显碱性,pH大于7;将一定浓度的NaOH溶液加水稀释,碱性逐渐变弱;但溶液始终显碱性,所得溶液的pH接近7,但不可能等于7,更不可能小于7.
故选:C.
点评 本题是一道图象坐标与化学知识相结合的综合题,解题的关键是结合所涉及的化学知识,正确分析各变化的过程,注意分析坐标轴表示的意义、曲线的起点、折点及变化趋势,进而确定正确的图象.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.化学物质之间的反应奥妙无穷.在一次化学探宄活动中,同学们从不同角度对稀 盐酸与氢氧化钠溶液的反应进行了探究.请你参与并填写以下空白.
(1)如何用实验验证稀盐酸与氢氧化钠溶液发生了反应
第一组同学设计了实验方案一:
请你分析上述方案中为什么强调只有测得的pH≥7才能证明反应发生了?排除因氢氧化钠溶液的加入,稀释盐酸而引起pH变大(或只有pH≥7才能说明盐酸已经反应掉了)
(2)设计实验.探究稀盐酸与氢氧化钠溶液的反应是否放热
提供的实验仪器与药品的盐酸、10%的氢氧化钠溶液、烧杯、温度计、玻璃棒、胶头滴管.(请填写实验步骤、实验现象)
(3)探究稀盐酸与氢氧化钠溶液是否恰好完全反应.请你完成实验方案设计:
第二组同学在做完稀盐酸与氢氧化钠溶液反应的实验后.为探究稀盐酸与氢氧化钠溶液 是否恰好完全反应,设计了实验方案二:
此时有同学提出方案二不能证明稀盐酸与氢氧化钠溶液恰好完全反应.其原因是若盐酸过量,加入硫酸铜溶液时也无明显现象(或盐酸可能有剩余).为此,还需要选择紫色石蕊试液(或锌粒、碳酸钠、氧化铜、氢氧化铜、pH试纸等)(填一种试剂).再进行实验即可.
(1)如何用实验验证稀盐酸与氢氧化钠溶液发生了反应
第一组同学设计了实验方案一:
| 实验步骤 | 实验现象 | 结论 |
| 先用pH试纸测定稀盐酸的 pH.再逐渐滴加氢氧化钠溶 液.并不断振荡,同时测定 混合液的pH | pH逐渐变大,最后PH≥7 | 稀盐酸与氢氧化钠溶液能发 生反应 |
(2)设计实验.探究稀盐酸与氢氧化钠溶液的反应是否放热
提供的实验仪器与药品的盐酸、10%的氢氧化钠溶液、烧杯、温度计、玻璃棒、胶头滴管.(请填写实验步骤、实验现象)
| 实验步骤 | 实验现象 | 结论 |
| 稀盐酸与氢氧化钠溶液反应 放热. |
第二组同学在做完稀盐酸与氢氧化钠溶液反应的实验后.为探究稀盐酸与氢氧化钠溶液 是否恰好完全反应,设计了实验方案二:
| 实验步骤 | 实验现象 | 结论 |
| 取少受上述反应后的溶液子 试管中.滴加硫酸铜溶液. | 若生成蓝色沉淀 | 氢氧化钠溶液过量 |
| 若没有明显现象 | 稀盐酸与氢氧化钠溶液恰好 完全反应 |
4.探究一学习氢氧化钠的性质之后,知道氢氧化钠溶液中含有H2O、Na+、OH-,能使无色酚酞试液变红色,某科技小组想进一步探究是哪一种粒子使无色酚酞试液变红色.
【提出猜想】猜想①:可能是H2O;猜想②:可能是Na+; 猜想③:可能是OH-.
【实验验证】
【讨论反思】有同学认为猜想①不需要实验验证就可以排除,你认为该同学的理由是无色酚酞试液中有大量水分子,已经证明水分子不能使酚酞变红色.
探究二
某化学兴趣小组的同学对碳酸钙高温加热一段时间剩余固体的成分进行探究.
【提出问题】剩余固体成分是什么?
【猜想与假设】剩余固体成分为:
A.全部是碳酸钙 B.既有碳酸钙,也有氧化钙 C.全部是氧化钙
【设计并完成实验】
实验结论】该化学兴趣小组同学得出的结论:
【剩余固体成分】与【猜想与假设】中的B(填“A”或“B”或“C”).
【交流与反思】实验操作产生的气体是二氧化碳,如何检验是该气体把气体通入澄清石灰水中,如果澄清石灰水变浑浊,说明是二氧化碳;剩余固体的成分若与C相符,则两步操作的实验现象②(填“①”或“②”或“①②”)不同.
【提出猜想】猜想①:可能是H2O;猜想②:可能是Na+; 猜想③:可能是OH-.
【实验验证】
| 实 验 操 作 | 实 验 现 象 | 结 论 |
| ①用试管取少量蒸馏水,滴入1-2滴无色酚酞试液,振荡 | 试管内溶液仍为无色 | 水分子不能使无色酚酞试液变红色 |
| ②用试管取少量氯化钠溶液,滴入1-2滴无色酚酞试液,振荡 | 试管内溶液仍为无色 | 钠离子不能使无色酚酞试液变红色 |
| ③用试管取少量氢氧化钠溶液,滴入1-2滴无色酚酞试液,振荡 | 溶液变红色 | 氢氧根离子能使酚酞试液变红色 |
探究二
某化学兴趣小组的同学对碳酸钙高温加热一段时间剩余固体的成分进行探究.
【提出问题】剩余固体成分是什么?
【猜想与假设】剩余固体成分为:
A.全部是碳酸钙 B.既有碳酸钙,也有氧化钙 C.全部是氧化钙
【设计并完成实验】
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量固体于试管中,加适量水振荡后静置,再滴几滴无色酚酞试液 | 溶液变红 | 说明固体成分中一定 含有氧化钙. |
| ②再取少量固体于另一试管中滴加过量稀盐酸 | 有气泡生成 | 说明固体成分中一定 含有碳酸钙. |
【剩余固体成分】与【猜想与假设】中的B(填“A”或“B”或“C”).
【交流与反思】实验操作产生的气体是二氧化碳,如何检验是该气体把气体通入澄清石灰水中,如果澄清石灰水变浑浊,说明是二氧化碳;剩余固体的成分若与C相符,则两步操作的实验现象②(填“①”或“②”或“①②”)不同.
3.推理是化学学习中常用的思维方法,下列推理正确的是( )
| A. | 酸溶液能使紫色石蕊试液变红,能使紫色石蕊试液变红的一定是酸 | |
| B. | 氢氧化钠能与二氧化碳反应生成盐和水,所以属于中和反应 | |
| C. | 氧化物有两种元素组成,其中一种元素为氧元素,所以水属于氧化物 | |
| D. | 碱溶液的pH>7,碳酸钠溶液的pH也大于7,所以它属于碱 |
10.下列关于实验现象的描述正确的是( )
| A. | 硫在空气中燃烧产生蓝紫色的火焰 | B. | 铁在氧气中燃烧生成四氧化三铁 | ||
| C. | 红磷燃烧产生大量的白色烟雾 | D. | 木炭在氧气中燃烧发出白光 |
8.小红和小丽在探究碱的化学性质时,将稀盐酸滴入到氢氧化钠溶液中,意外地看到有气泡产生,她认为氢氧化钠溶液 已经变质了.用化学方程式表示氢氧化钠溶液变质的原因:CO2+2NaOH=Na2CO3+H2O.
【提出问题】变质后的氢氧化钠溶液中的溶质是什么?
【猜想假设】小丽对变质后的氢氧化钠溶液中的溶质成分做出了两种猜想:
猜想一:碳酸钠;
猜想二:NaOH和Na2CO3.
【实验设计】为验证上述猜想哪个正确,小丽设计了如下方案:取少量氢氧化钠溶液样品于试管中,滴加几滴无色酚酞溶液,观察溶液颜色变化.小红认为小丽的实验方案不合理,理由是:碳酸钠和氢氧化钠溶液都能使酚酞变红色
【实验与结论】小红另外设计并完成了实验,请你帮她填写下面的实验报告:
【提出问题】变质后的氢氧化钠溶液中的溶质是什么?
【猜想假设】小丽对变质后的氢氧化钠溶液中的溶质成分做出了两种猜想:
猜想一:碳酸钠;
猜想二:NaOH和Na2CO3.
【实验设计】为验证上述猜想哪个正确,小丽设计了如下方案:取少量氢氧化钠溶液样品于试管中,滴加几滴无色酚酞溶液,观察溶液颜色变化.小红认为小丽的实验方案不合理,理由是:碳酸钠和氢氧化钠溶液都能使酚酞变红色
【实验与结论】小红另外设计并完成了实验,请你帮她填写下面的实验报告:
| 实验步骤 | 实验现象 | 结论 |
| 步骤1:取少量氢氧化钠溶液样品于试管中,向其中滴加过量的氯化钙溶液 | 有白色沉淀生成 | 猜想一 正确 |
| 步骤2:取步骤1反应后的溶液测定溶液的pH,具体方法是把pH试纸放在洁净的玻璃片上,用玻璃棒蘸 取待测液滴到pH试纸上将试纸显示的颜色与标准比色卡比较 | pH=7 |
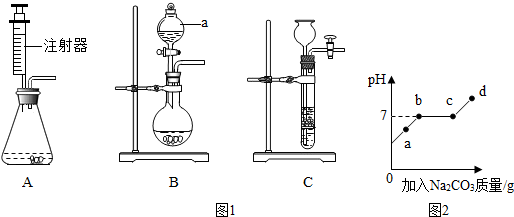
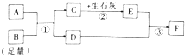 A-F是初中化学常见的物质,其中A为天然气的主要成分,F是大理石的主要成分,这些物质的相互转化关系如图所示,其中部分生成物和反应条件已省略.
A-F是初中化学常见的物质,其中A为天然气的主要成分,F是大理石的主要成分,这些物质的相互转化关系如图所示,其中部分生成物和反应条件已省略.