题目内容
12.向盛有氯化亚铁和氯化铜混合溶液的烧杯中加入一定量的锌粉,充分反应后,得到固体M和溶液N.下列叙述错误的是( )| A. | 锌有剩余时,M中一定有Fe、Cu和Zn | |
| B. | 锌有剩余时,N中一定没有FeCl2和CuCl2 | |
| C. | 锌无剩余时,M中一定有Cu、可能有Fe | |
| D. | 锌无剩余时,N中一定有ZnCl2和FeCl2 |
分析 根据在金属活动性顺序中,排在前面的金属可以将排在后面的金属从其盐溶液中置换出来,三种金属的活动性顺序为:锌>铁>铜进行分析.
解答 解:在金属活动性顺序中,排在前面的金属可以将排在后面的金属从其盐溶液中置换出来,三种金属的活动性顺序为:锌>铁>铜,所以向盛有氯化亚铁和氯化铜混合溶液的烧杯中加入一定量的锌粉,锌会先与氯化铜反应,再与氯化亚铁反应,所以
A、锌有剩余时,M中一定有Fe、Cu和Zn,故A正确;
B、锌有剩余时,锌和氯化铜、氯化亚铁完全反应,所以N中一定没有FeCl2和CuCl2,故B正确;
C、锌无剩余时,锌先与氯化铜反应,可能与氯化亚铁反应,所以M中一定有Cu、可能有Fe,故C正确;
D、锌无剩余时,N中一定有ZnCl2,可能FeCl2、CuCl2,故D错误.
故选:D.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
3.钛具有硬度大、密度小、熔点高、抗腐蚀性强等优良性能,被誉为“未来金属”.钛铁矿石的主要成分是钛酸亚铁(FeTiO3).冶炼金属钛时,主要发生以下两个反应:①2FeTiO3+6C+7Cl2=2X+2TiCl4+6CO,②TiCl4+2Mg=Ti+2MgCl2,则下列说法正确的是( )
| A. | X的化学式为FeCl2 | |
| B. | 钛合金属于合成材料 | |
| C. | Ti的活动性比Mg强 | |
| D. | 钛元素的化合价在反应中出现的化合物中都是+4价 |
20.下列过程属于物理变化的是( )
| A. | 铁锅生锈 | B. | 粮食酿酒 | C. | 食物腐败 | D. | 白醋挥发 |
7.化学与社会、科技、生产和生活等密切相关,下列做法不合理的是( )
| A. | 少开私家车,以减轻雾霾 | |
| B. | 多用熟石灰吸收CO2,以防止温室效应 | |
| C. | 在钢铁表面镀锌,以防止钢铁生锈 | |
| D. | 开发新能源,以减少对化石燃料的依赖 |
4.在氧化铜和铁的混合物中加入一定量的稀硫酸,微热,使其充分反应.反应停止后滤出不溶物,再往滤液中放入一根光亮的铁钉,铁钉表面有气泡产生,未见其它变化.则( )
| A. | 滤出的不溶物只有铜 | B. | 滤出的不溶物只有铁 | ||
| C. | 滤出的不溶物是铁和铜的混合物 | D. | 滤液中没有Fe2+ |
15.区别下列各组物质,选择的试剂或方法均能达到目的是( )
| 选项 | 区别的物质 | 试剂或方法 |
| A | 二氧化碳和一氧化碳 | ①闻气味;②紫色石蕊溶液 |
| B | 浓盐酸和浓硫酸 | ①小木棍;②打开试剂瓶,观察是否有白雾 |
| C | 氢氧化钠和碳酸钠 | ①酚酞溶液;②澄清石灰水 |
| D | 碳粉和氧化铜 | ①稀盐酸;②氧气 |
| A. | A | B. | B | C. | C | D. | D |
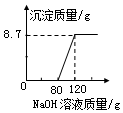 向盛有100g稀硫酸的烧杯中加入一定质量的镁粉,固体完全反应后,再向所得溶液中加入NaOH溶 液,所得沉淀的质量与加入NaOH溶液的质量关系如图所示.请计算:
向盛有100g稀硫酸的烧杯中加入一定质量的镁粉,固体完全反应后,再向所得溶液中加入NaOH溶 液,所得沉淀的质量与加入NaOH溶液的质量关系如图所示.请计算: 如图是测定空气中氧气含量的实验装置图.实验如下:用注射器抽取30mL空气(活塞拉至30mL刻度处),硬质玻璃管中空气的体积为50mL;在硬质玻璃管中放入过量铜粉,在右侧导管口套上瘪的气球;点燃酒精灯,反复推拉注射器和挤压气球,待充分反应后,冷却至室温;将气球中气体全部挤入硬质玻璃管,注射器中气体的体积为14mL.
如图是测定空气中氧气含量的实验装置图.实验如下:用注射器抽取30mL空气(活塞拉至30mL刻度处),硬质玻璃管中空气的体积为50mL;在硬质玻璃管中放入过量铜粉,在右侧导管口套上瘪的气球;点燃酒精灯,反复推拉注射器和挤压气球,待充分反应后,冷却至室温;将气球中气体全部挤入硬质玻璃管,注射器中气体的体积为14mL.