题目内容
17. 如图是测定空气中氧气含量的实验装置图.实验如下:用注射器抽取30mL空气(活塞拉至30mL刻度处),硬质玻璃管中空气的体积为50mL;在硬质玻璃管中放入过量铜粉,在右侧导管口套上瘪的气球;点燃酒精灯,反复推拉注射器和挤压气球,待充分反应后,冷却至室温;将气球中气体全部挤入硬质玻璃管,注射器中气体的体积为14mL.
如图是测定空气中氧气含量的实验装置图.实验如下:用注射器抽取30mL空气(活塞拉至30mL刻度处),硬质玻璃管中空气的体积为50mL;在硬质玻璃管中放入过量铜粉,在右侧导管口套上瘪的气球;点燃酒精灯,反复推拉注射器和挤压气球,待充分反应后,冷却至室温;将气球中气体全部挤入硬质玻璃管,注射器中气体的体积为14mL.(1)写出铜粉与氧气反应的化学方程式2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO.
(2)实验时,铜粉过量的目的是除去空气中所有的氧气;不能(填“能”或“不能”)用木炭代替铜粉进行相同实验.
(3)实验测得空气中氧气的含量为20%.
分析 (1)根据铜粉与氧气反应生成氧化铜解答;
(2)根据实验时,铜粉过量的目的是除去空气中所有的氧气解答;根据木炭燃烧生成二氧化碳气体解答;
(3)根据反应消耗氧气的体积为30ml-14ml=16ml,从而计算出空气中氧气的体积分数解答.
解答 解:
(1)该实验的原理是:铜粉与氧气反应生成氧化铜;发生反应的化学方程式为 2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO.
(2)实验时,为了完全除去空气中的氧气,铜粉必须是过量的,否则得出的结果不准确,铜粉与氧气反应生成固体氧化铜,而木条与氧气反应生成二氧化碳气体,瓶内气压基本不变,无法测量氧气的含量,故不能用木炭代替铜粉进行相同实验.
(3)原装置内气体气体为30ml+50ml=80ml;待充分反应后,冷却至室温;将气球中气体全部挤入硬质玻璃管,注射器中气体的体积为14mL.则反应消耗氧气的体积为30ml-14ml=16ml;实验测得空气中氧气的含量为:$\frac{16mL}{80mL}$×100%=20%
答案:
(1)2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO.
(2)除去空气中所有的氧气;不能;
(3)20%
点评 本考点考查了空气中氧气的含量的探究,并且注重了实验方案的评价,对实验方案进行评价是近几年中考的一个重点.评价包括对实验方案的评价、实验过程的评价、实验结论的评价等,要认真把握.

练习册系列答案
相关题目
7. 为测定某氮肥中氮元素的质量分数是否与标签说明相符,小玲取一定量该氮肥样品于烧杯中配成溶液与足量氯化钡溶液恰好反应,(杂质成分不含有氮元素,能溶于水但不参加反应)记录有关数据如表:请通过计算回答:
为测定某氮肥中氮元素的质量分数是否与标签说明相符,小玲取一定量该氮肥样品于烧杯中配成溶液与足量氯化钡溶液恰好反应,(杂质成分不含有氮元素,能溶于水但不参加反应)记录有关数据如表:请通过计算回答:
(1)反应共生成BaSO4的质量为23.3g.
(2)反应前后,溶液中硫元素的质量是减小(填“不变”、“增大”或“减小”).
(3)若所取氮肥样品的质量为15g,试通过计算确定该氮肥中氮元素的含量是否与标签相符.(请写出计算过程)
 为测定某氮肥中氮元素的质量分数是否与标签说明相符,小玲取一定量该氮肥样品于烧杯中配成溶液与足量氯化钡溶液恰好反应,(杂质成分不含有氮元素,能溶于水但不参加反应)记录有关数据如表:请通过计算回答:
为测定某氮肥中氮元素的质量分数是否与标签说明相符,小玲取一定量该氮肥样品于烧杯中配成溶液与足量氯化钡溶液恰好反应,(杂质成分不含有氮元素,能溶于水但不参加反应)记录有关数据如表:请通过计算回答:| 反 应 前 | 反 应 后 | |
| 烧杯和样品溶液总质量 | 氯化钡溶液质量 | 过滤后烧杯和溶液质量(滤液的损失忽略不计) |
| 45g | 85g | 106.7g |
(2)反应前后,溶液中硫元素的质量是减小(填“不变”、“增大”或“减小”).
(3)若所取氮肥样品的质量为15g,试通过计算确定该氮肥中氮元素的含量是否与标签相符.(请写出计算过程)
5.实验室配制溶质质量分数为5%的氯化钠溶液50g,下列操作正确的是( )
| A. | 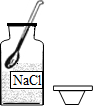 取氯化钠 取氯化钠 | B. | 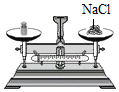 称氯化钠 称氯化钠 | C. | 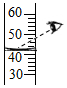 量取水 量取水 | D. | 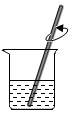 溶解 溶解 |
12.向盛有氯化亚铁和氯化铜混合溶液的烧杯中加入一定量的锌粉,充分反应后,得到固体M和溶液N.下列叙述错误的是( )
| A. | 锌有剩余时,M中一定有Fe、Cu和Zn | |
| B. | 锌有剩余时,N中一定没有FeCl2和CuCl2 | |
| C. | 锌无剩余时,M中一定有Cu、可能有Fe | |
| D. | 锌无剩余时,N中一定有ZnCl2和FeCl2 |
2.下列化学用语与所表述的意义相符合的是( )
| A. | H2O--1个水分子 | B. | Na+1--1个钠离子 | ||
| C. | 3Fe2+--3个铁离子 | D. | H2--2个氢原子 |