题目内容
2.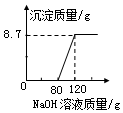 向盛有100g稀硫酸的烧杯中加入一定质量的镁粉,固体完全反应后,再向所得溶液中加入NaOH溶 液,所得沉淀的质量与加入NaOH溶液的质量关系如图所示.请计算:
向盛有100g稀硫酸的烧杯中加入一定质量的镁粉,固体完全反应后,再向所得溶液中加入NaOH溶 液,所得沉淀的质量与加入NaOH溶液的质量关系如图所示.请计算:(1)NaOH溶液中溶质的质量分数.
(2)与NaOH溶液反应所消耗硫酸溶质的质量.
分析 根据稀硫酸和镁反应生成硫酸镁和氢气,硫酸镁和氢氧化钠反应生成氢氧化镁沉淀和硫酸钠,稀硫酸和氢氧化钠反应生成硫酸钠和水,结合题中提供的数据可以进行相关方面的计算.
解答 解:(1)设生成8.7gMg(OH)2消耗的NaOH的质量为x,氢氧化钠溶液反应所消耗硫酸溶质的质量为y,
MgSO4+2NaOH=Mg(OH)2↓+Na2SO4,
80 58
x 8.7g
$\frac{80}{x}$=$\frac{58}{8.7g}$
x=12g
氢氧化钠溶液中溶质质量分数为:$\frac{12g}{120g-80g}$×100%=30%;
(2)H2SO4消耗的NaOH的质量为:80g×30%=24g
H2SO4+2NaOH=Na2SO4+2H2O,
98 80
y 24g
$\frac{98}{y}$=$\frac{80}{24g}$
y=29.4g
故答案为:(1)30%;
(2)29.4.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
12.小金根据生活经验推测,可燃物燃烧可能与氧气和温度有关,并设计完成了下列实验.对比各组实验,哪些组合能够达到研究影响可燃物燃烧因素的目的( )
| 实验① | 实验② | 实验③ | 实验④ |
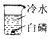 |  | 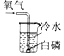 | 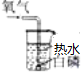 |
| 白磷不燃烧 | 白磷不燃烧 | 白磷不燃烧 | 白磷燃烧 |
| A. | ①和②,与温度有关 | B. | ②和③,与氧气有关 | ||
| C. | ②和④,与氧气有关 | D. | ①和④,与氧气和温度有关 |
13.下列实验现象的描述,错误的是( )
| A. | 铁丝在空气中燃烧时生成一种黑色固体 | |
| B. | 硫粉在氧气中燃烧时发出明亮的蓝紫色火焰 | |
| C. | 硫粉在空气中燃烧时发出淡蓝色火焰 | |
| D. | 燃着的火柴放入装满O2的瓶内,木条燃的更旺 |
10.甲原子与乙原子的质量比为a:b,而乙原子与碳12原子的质量比为c:d,则甲原子的相对原子质量为( )
| A. | 12ac/bd | B. | bc/12ac | C. | 12bd/ac | D. | ab/12bc |
7. 为测定某氮肥中氮元素的质量分数是否与标签说明相符,小玲取一定量该氮肥样品于烧杯中配成溶液与足量氯化钡溶液恰好反应,(杂质成分不含有氮元素,能溶于水但不参加反应)记录有关数据如表:请通过计算回答:
为测定某氮肥中氮元素的质量分数是否与标签说明相符,小玲取一定量该氮肥样品于烧杯中配成溶液与足量氯化钡溶液恰好反应,(杂质成分不含有氮元素,能溶于水但不参加反应)记录有关数据如表:请通过计算回答:
(1)反应共生成BaSO4的质量为23.3g.
(2)反应前后,溶液中硫元素的质量是减小(填“不变”、“增大”或“减小”).
(3)若所取氮肥样品的质量为15g,试通过计算确定该氮肥中氮元素的含量是否与标签相符.(请写出计算过程)
 为测定某氮肥中氮元素的质量分数是否与标签说明相符,小玲取一定量该氮肥样品于烧杯中配成溶液与足量氯化钡溶液恰好反应,(杂质成分不含有氮元素,能溶于水但不参加反应)记录有关数据如表:请通过计算回答:
为测定某氮肥中氮元素的质量分数是否与标签说明相符,小玲取一定量该氮肥样品于烧杯中配成溶液与足量氯化钡溶液恰好反应,(杂质成分不含有氮元素,能溶于水但不参加反应)记录有关数据如表:请通过计算回答:| 反 应 前 | 反 应 后 | |
| 烧杯和样品溶液总质量 | 氯化钡溶液质量 | 过滤后烧杯和溶液质量(滤液的损失忽略不计) |
| 45g | 85g | 106.7g |
(2)反应前后,溶液中硫元素的质量是减小(填“不变”、“增大”或“减小”).
(3)若所取氮肥样品的质量为15g,试通过计算确定该氮肥中氮元素的含量是否与标签相符.(请写出计算过程)
11.央视《是真的吗?》栏目播出了电脑浸在液体中也能正常工作的新鲜亊.其实这种液体是被称作“绝缘液”的液态一氟二氯乙烷,其化学式为(CC12FCH3),下列对一氟二氯乙烷的认识错误的是( )
| A. | 一氟二氯乙烷是有机物 | |
| B. | 一氟二氯乙烷由四种元素组成 | |
| C. | 一氟二氯乙烷由2个碳原子、2个氯原子、1个氟原子和3个氧原子构成 | |
| D. | 一氟二氯乙烷中碳元素与氢元素的质量比为8:1 |
12.向盛有氯化亚铁和氯化铜混合溶液的烧杯中加入一定量的锌粉,充分反应后,得到固体M和溶液N.下列叙述错误的是( )
| A. | 锌有剩余时,M中一定有Fe、Cu和Zn | |
| B. | 锌有剩余时,N中一定没有FeCl2和CuCl2 | |
| C. | 锌无剩余时,M中一定有Cu、可能有Fe | |
| D. | 锌无剩余时,N中一定有ZnCl2和FeCl2 |
 向100gCuSO4与H2SO4的混合溶液中加入质量分数为20%的氢氧化钠溶液,产生沉淀的质量与所加氢氧化钠溶液的质量关系如图所示,回答下列问题
向100gCuSO4与H2SO4的混合溶液中加入质量分数为20%的氢氧化钠溶液,产生沉淀的质量与所加氢氧化钠溶液的质量关系如图所示,回答下列问题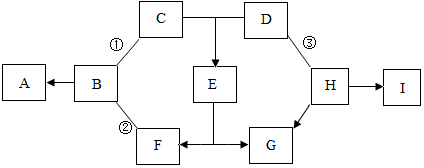 如图中A-I表示几种初中化学常见的物质,其中A、D、I是氧化物,I中两元素质量比为3:4; B元素在地壳中含量位居第三;C有三种元素组成;G为紫红色;H为黑色固体单质.(图中部分反应物、生成物或反应条件已略去)
如图中A-I表示几种初中化学常见的物质,其中A、D、I是氧化物,I中两元素质量比为3:4; B元素在地壳中含量位居第三;C有三种元素组成;G为紫红色;H为黑色固体单质.(图中部分反应物、生成物或反应条件已略去)