题目内容
4.在氧化铜和铁的混合物中加入一定量的稀硫酸,微热,使其充分反应.反应停止后滤出不溶物,再往滤液中放入一根光亮的铁钉,铁钉表面有气泡产生,未见其它变化.则( )| A. | 滤出的不溶物只有铜 | B. | 滤出的不溶物只有铁 | ||
| C. | 滤出的不溶物是铁和铜的混合物 | D. | 滤液中没有Fe2+ |
分析 根据酸的性质以及金属活动性顺序表的应用分析,CuO和Fe的混合物中加入一定量的稀硫酸,微热.硫酸与氧化铜反应生成了硫酸铜和水,硫酸与铁反应生成了硫酸亚铁和氢气,铁又能与生成的硫酸铜反应生成了铜和硫酸亚铁.滤出不溶物后再往滤液里加入一枚铁钉,铁钉表面有气泡产生,未见其它变化,上说明了溶液中有稀硫酸,但没有硫酸铜.
解答 解:由题意可知:CuO和Fe的混合物中加入一定量的稀硫酸,微热.硫酸与氧化铜反应生成了硫酸铜和水,硫酸与铁反应生成了硫酸亚铁和氢气,铁又能与生成的硫酸铜反应生成了铜和硫酸亚铁.滤出不溶物后再往滤液里加入一枚铁钉,铁钉表面有气泡产生,未见其它变化,上说明了溶液中有稀硫酸,但没有硫酸铜.所以:
A、因为滤液中有硫酸,因此滤出的不溶物只有铜,没有铁,故正确;
B、因为滤液中有硫酸,因此滤出的不溶物只有铜,没有铁,故错误;
C、因为滤液中有硫酸,因此滤出的不溶物只有铜,没有铁,故错误;
D、铁和硫酸反应生成硫酸亚铁和氢气,铁和硫酸铜反应生成硫酸亚铁和铜,因此滤液中一定有Fe2+,故错误.
故选:A.
点评 本题是一道推断知识考查题,解题的关键是对最后加入铁后的分析,这是解题的关键.

练习册系列答案
相关题目
15.下列各组物质中都是由分子构成的是( )
| A. | 金刚石 C60 | B. | 氧气 甲烷 | ||
| C. | 氯化钾 硫酸铜 | D. | 氦气 水 |
12.向盛有氯化亚铁和氯化铜混合溶液的烧杯中加入一定量的锌粉,充分反应后,得到固体M和溶液N.下列叙述错误的是( )
| A. | 锌有剩余时,M中一定有Fe、Cu和Zn | |
| B. | 锌有剩余时,N中一定没有FeCl2和CuCl2 | |
| C. | 锌无剩余时,M中一定有Cu、可能有Fe | |
| D. | 锌无剩余时,N中一定有ZnCl2和FeCl2 |
7.下列用途与性质关系的说法正确的是( )
| A. | 石墨制铅笔芯---石墨是黑色固体 | |
| B. | 氧气用于金属切割---氧气具有可燃性 | |
| C. | 食品充氮气防腐---氮气化学性质不活泼 | |
| D. | 熟石灰改良酸性土壤---熟石灰易溶于水 |
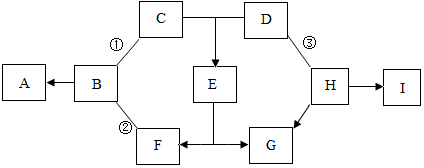 如图中A-I表示几种初中化学常见的物质,其中A、D、I是氧化物,I中两元素质量比为3:4; B元素在地壳中含量位居第三;C有三种元素组成;G为紫红色;H为黑色固体单质.(图中部分反应物、生成物或反应条件已略去)
如图中A-I表示几种初中化学常见的物质,其中A、D、I是氧化物,I中两元素质量比为3:4; B元素在地壳中含量位居第三;C有三种元素组成;G为紫红色;H为黑色固体单质.(图中部分反应物、生成物或反应条件已略去)