题目内容
14. 如图所示,往水电解器中加入96g蒸馏水和2g Na2SO4(Na2SO4不参与反应,仅起增加水的导电性的作用)组成的混合物,然后进行电解,当负极得到2g气体时,停止实验(所需相对原子质量:H-1、O-16).计算:
如图所示,往水电解器中加入96g蒸馏水和2g Na2SO4(Na2SO4不参与反应,仅起增加水的导电性的作用)组成的混合物,然后进行电解,当负极得到2g气体时,停止实验(所需相对原子质量:H-1、O-16).计算:(1)停止实验时,电解消耗水的质量是多少?
(2)停止实验后,剩余溶液中Na2SO4的质量分数是多少?
分析 由于过程中硫酸钠仅起增加水的导电性的作用,相当于是本反应的催化剂,其质量保持不变.根据电解水正氧负氢,氢二氧一可知,负极为氢气也就是得到2g氢气,根据氢气的质量和对应的化学方程式求算消耗的水的质量,进而求算所得溶液中硫酸钠的质量分数.
解答 解:负极得到的是氢气,也就是氢气的质量为2g
设生成2g氢气消耗的水的质量为x
2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑
36 4
x 2g
$\frac{36}{4}$=$\frac{x}{2g}$
x=18g
由于过程中硫酸钠仅起增加水的导电性的作用,相当于是本反应的催化剂,其质量保持不变.
剩余溶液中Na2SO4的质量分数为$\frac{2g}{96g-18g+2g}$×100%=2.5%
答:(1)停止实验时,电解消耗水的质量是18g.
(2)停止实验后,剩余溶液中Na2SO4的质量分数是2.5%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
相关题目
5.对物质的鉴别方法不正确的是( )
| A. | 用燃着的木条区分氮气和二氧化碳 | |
| B. | 用灼烧闻气味的方法区分天然纤维和合成纤维 | |
| C. | 用稀盐酸区分NaOH溶液和Na2CO3溶液 | |
| D. | 用互相刻画的方法比较黄铜和铜的硬度 |
6.小明同学利用一瓶敞口放置已久的NaOH溶液进行了一些实验探究.
[提出问题]这瓶NaOH溶液变质程度如何呢?
[提出猜想]小明的猜想:NaOH溶液部分变质
[实验探究]小明设计了如下实验来验证自己的猜想,请根据表中内容填写实验时的现象.
[实验反思]
(1)下列物质①Ca(OH)2溶液 ②Ba(NO3)2溶液 ③BaCl2溶液,能替代小明实验中CaCl2溶液的是②③
(2)请用化学方程式表示氢氧化钠溶液变质的原因2NaOH+CO2═Na2CO3+H2O
[拓展应用]现向烧杯中加入100g这种已部分变质的NaOH溶液,再滴加溶质质量分数为11.1%的CaCl2溶液100g,产生沉淀质量与所加CaCl2溶液质量的关系如图所示.
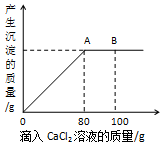
(1)B点处所得溶液中溶质为NaCl和CaCl2 (写化学式)
(2)求反应结束后烧杯中沉淀的质量.
[提出问题]这瓶NaOH溶液变质程度如何呢?
[提出猜想]小明的猜想:NaOH溶液部分变质
[实验探究]小明设计了如下实验来验证自己的猜想,请根据表中内容填写实验时的现象.
| 实验步骤 | 现象 | 结论 |
| 取少量NaOH溶液样品于试管中,先滴加足量CaCl2溶液,然后再滴加酚酞试液 | NaOH部分变质 | |
(1)下列物质①Ca(OH)2溶液 ②Ba(NO3)2溶液 ③BaCl2溶液,能替代小明实验中CaCl2溶液的是②③
(2)请用化学方程式表示氢氧化钠溶液变质的原因2NaOH+CO2═Na2CO3+H2O
[拓展应用]现向烧杯中加入100g这种已部分变质的NaOH溶液,再滴加溶质质量分数为11.1%的CaCl2溶液100g,产生沉淀质量与所加CaCl2溶液质量的关系如图所示.

(1)B点处所得溶液中溶质为NaCl和CaCl2 (写化学式)
(2)求反应结束后烧杯中沉淀的质量.
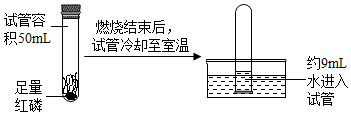 磷的燃烧反应在生产生活中有着广泛的应用价值.
磷的燃烧反应在生产生活中有着广泛的应用价值. A、B、C、D为初中化学常见的物质,它们之间存在一定的关系,请根据下列叙述回答问题.“-”表示两端的物质能反应,“→”表示物质间存在转化关系.(部分生成物和反应条件已略去).
A、B、C、D为初中化学常见的物质,它们之间存在一定的关系,请根据下列叙述回答问题.“-”表示两端的物质能反应,“→”表示物质间存在转化关系.(部分生成物和反应条件已略去).