题目内容
6.小明同学利用一瓶敞口放置已久的NaOH溶液进行了一些实验探究.[提出问题]这瓶NaOH溶液变质程度如何呢?
[提出猜想]小明的猜想:NaOH溶液部分变质
[实验探究]小明设计了如下实验来验证自己的猜想,请根据表中内容填写实验时的现象.
| 实验步骤 | 现象 | 结论 |
| 取少量NaOH溶液样品于试管中,先滴加足量CaCl2溶液,然后再滴加酚酞试液 | NaOH部分变质 | |
(1)下列物质①Ca(OH)2溶液 ②Ba(NO3)2溶液 ③BaCl2溶液,能替代小明实验中CaCl2溶液的是②③
(2)请用化学方程式表示氢氧化钠溶液变质的原因2NaOH+CO2═Na2CO3+H2O
[拓展应用]现向烧杯中加入100g这种已部分变质的NaOH溶液,再滴加溶质质量分数为11.1%的CaCl2溶液100g,产生沉淀质量与所加CaCl2溶液质量的关系如图所示.
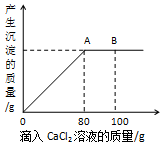
(1)B点处所得溶液中溶质为NaCl和CaCl2 (写化学式)
(2)求反应结束后烧杯中沉淀的质量.
分析 根据已有的知识进行分析解答,氢氧化钠变质生成碳酸钠,碳酸钠能与氯化钙溶液反应生成白色沉淀,氢氧化钠能使酚酞试液变红;要证明碳酸钠和氢氧化钠同时存在,需要除去碳酸钠,但是不能生成氢氧化钠;根据图象提供的数据结合反应的化学方程式计算即可.
解答 解:实验探究:氢氧化钠部分变质,则含有的是氢氧化钠和碳酸钠,除去碳酸钠以后的溶液呈碱性,能使酚酞试液变红;故填;无色酚酞变红色;
实验反思:(1)①Ca(OH)2溶液能除去碳酸钠,但是生成了氢氧化钠,对氢氧化钠的检验造成了干扰,错误;
②Ba(NO3)2溶液能除去碳酸钠,且不会生成碱性物质,对氢氧化钠的检验没有干扰,正确;
③BaCl2溶液能除去碳酸钠,且不会生成碱性物质,对氢氧化钠的检验没有干扰,正确;
故填:②③;
(2)氢氧化钠变质是因为氢氧化钠和二氧化碳反应生成了碳酸钠和水的缘故,故填:2NaOH+CO2═Na2CO3+H2O;
拓展应用:(1)B点处氯化钙溶液过量,碳酸钠和氯化钙完全反应生成碳酸钙沉淀和氯化钠,故含有的溶质是氯化钠和氯化钙,故填:NaCl和CaCl2;
(2)恰好完全反应消耗氯化钙的质量为:80g×11.1%=8.88g
设碳酸钙的质量为x
Na2CO3+CaCl2=CaCO3↓+2NaCl
111 100
8.88g x
$\frac{111}{100}=\frac{8.88g}{x}$
x=8g
答:反应结束后烧杯中沉淀的质量8g.
点评 本题考查的是物质变质成分的实验探究,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
17.李明同学在不同季节的制作过程中,一定发生了化学变化的是( )
| A. | 春天花朵制成标本 | B. | 夏天粮食酿成美酒 | ||
| C. | 秋天水果榨成果汁 | D. | 冬天冰砖凿成冰雕 |
11.甲醛是装修材料中常见的污染物,其分子结构如图所示,下列说法正确的是( )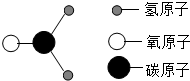

| A. | 甲醛由碳、氢、氧三种元素组成 | |
| B. | 甲醛的相对分子质量为30g | |
| C. | 甲醛由一个碳原子、2个氢原子和1个氧原子构成 | |
| D. | 甲醛中碳、氢、氧三种元素的质量比为1:2:1 |
18.实验室配制100g 10%的NaCl溶液,不需要用到的仪器是( )
| A. | 酒精灯 | B. | 托盘天平 | C. | 胶头滴管 | D. | 烧杯 |
15.下列实验操作正确的是( )
| A. | 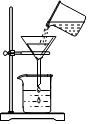 过滤 | B. | 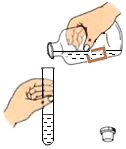 倾倒液体 | C. | 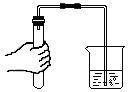 检验装置气密性 | D. | 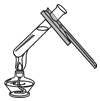 给液体加热 |
16.分类、归纳、分析、推理等是化学学习中常用的思想和方法.下列相关说法不正确的是( )
| A. | 分类:生铁、天然气、冰水混合物都属于混合物 | |
| B. | 归纳:酸和碱中和一定都含有氢元素 | |
| C. | 分析:金刚石和石墨物理性质差异很大,是因为碳原子的排列方式不同 | |
| D. | 推理:碱性溶液能使物色酚酞变红,所以能使酚酞变红的溶液pH一定大于7 |
 构建知识网络是一种重要的学习方法.下面是某同学整理的关于硫酸化学性质的知识网络“-”表示相连的两种物质能发生反应,“→”表示一种物质能转化为另一种物质,A、B、C分别属于不同类别的化合物,D是一种常见的银白色的金属单质.请填写下列空格:
构建知识网络是一种重要的学习方法.下面是某同学整理的关于硫酸化学性质的知识网络“-”表示相连的两种物质能发生反应,“→”表示一种物质能转化为另一种物质,A、B、C分别属于不同类别的化合物,D是一种常见的银白色的金属单质.请填写下列空格: 如图所示,往水电解器中加入96g蒸馏水和2g Na2SO4(Na2SO4不参与反应,仅起增加水的导电性的作用)组成的混合物,然后进行电解,当负极得到2g气体时,停止实验(所需相对原子质量:H-1、O-16).计算:
如图所示,往水电解器中加入96g蒸馏水和2g Na2SO4(Na2SO4不参与反应,仅起增加水的导电性的作用)组成的混合物,然后进行电解,当负极得到2g气体时,停止实验(所需相对原子质量:H-1、O-16).计算: