题目内容
3. 磷的燃烧反应在生产生活中有着广泛的应用价值.
磷的燃烧反应在生产生活中有着广泛的应用价值.(1)红磷在空气中燃烧能冒出浓厚的白烟,军事上常用来制烟幕弹.红磷燃烧的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
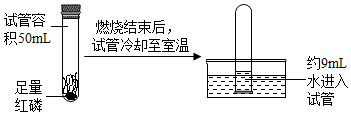
(2)某同学利用燃磷法测量空气中氧气含量,实验过程如图.他测得氧气体积分数约是18%.燃烧结束试管里剩余气体主要是N2(填化学式).
分析 (1)根据化学反应的原理以及化学方程式的写法来分析;
(2)根据进入容器的水的体积即为氧气体积以及空气的组成来分析.
解答 解:(1)磷与氧气在点燃的条件下反应生成五氧化二磷;故填:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(2)进入试管内的水的体积为消耗的氧气体积,也就是50mL空气中含有9mL氧气,所以他测得氧气体积分数约是$\frac{9mL}{50mL}×100%$=18%;空气主要是由氮气与氧气组成的,氧气被消耗后剩余的气体主要是氮气;故填:18;N2.
点评 熟记用红磷测定空气里氧气含量的实验原理、操作步骤、实验现象、实验结论和注意事项是解答这类题目的基础.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.下列物质露置于空气中一段时间后,质量增加的是( )
| A. | 碳酸钙 | B. | 氯化钠 | C. | 氢氧化钠 | D. | 浓盐酸 |
11.甲醛是装修材料中常见的污染物,其分子结构如图所示,下列说法正确的是( )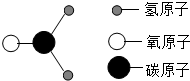

| A. | 甲醛由碳、氢、氧三种元素组成 | |
| B. | 甲醛的相对分子质量为30g | |
| C. | 甲醛由一个碳原子、2个氢原子和1个氧原子构成 | |
| D. | 甲醛中碳、氢、氧三种元素的质量比为1:2:1 |
18.实验室配制100g 10%的NaCl溶液,不需要用到的仪器是( )
| A. | 酒精灯 | B. | 托盘天平 | C. | 胶头滴管 | D. | 烧杯 |
15.下列实验操作正确的是( )
| A. | 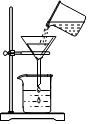 过滤 | B. | 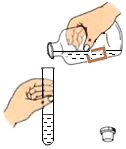 倾倒液体 | C. | 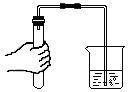 检验装置气密性 | D. | 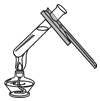 给液体加热 |
12.实验室发现一瓶标签脱落的固体试剂,小王分别取少量的该固体进行了下列实验.根据实验现象,该固体最可能是( )
| 实验步骤 | 实验现象 |
| 检测水中加入固体前后液体的pH | 固体不溶解,液体的pH几乎没变化 |
| 检测盐酸中加入固体前后溶液的pH | 固体溶解,无气体放出,溶液pH增大 |
| 固体灼热状态下,通入纯净CO | 固体质量减轻,尾气中只检测到CO与CO2 |
| A. | 金属单质 | B. | 碱 | C. | 盐 | D. | 金属氧化物 |
13.早期治疗疟疾的原料是奎宁碱(化学式为C20H24N2O2),现在普遍使用的是我国科学家发现的青蒿素(化学式为C15H22O5),下列说法正确的是( )
| A. | 奎宁碱和青蒿素都是有机物 | |
| B. | 奎宁碱中含有20个碳原子 | |
| C. | 青蒿素中碳、氢、氧三种元素的质量比是15:22:5 | |
| D. | 奎宁碱和青蒿素分别在氧气中完全燃烧的产物相同 |
 如图所示,往水电解器中加入96g蒸馏水和2g Na2SO4(Na2SO4不参与反应,仅起增加水的导电性的作用)组成的混合物,然后进行电解,当负极得到2g气体时,停止实验(所需相对原子质量:H-1、O-16).计算:
如图所示,往水电解器中加入96g蒸馏水和2g Na2SO4(Na2SO4不参与反应,仅起增加水的导电性的作用)组成的混合物,然后进行电解,当负极得到2g气体时,停止实验(所需相对原子质量:H-1、O-16).计算: 如图是A、B、C三种固体物质的溶解度曲线,请回答下列问题:
如图是A、B、C三种固体物质的溶解度曲线,请回答下列问题: