题目内容
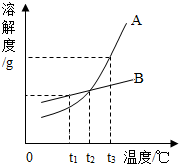 如图是A、B两种物质的溶解度曲线,根据图示回答下列问题:
如图是A、B两种物质的溶解度曲线,根据图示回答下列问题:(1)t1°C时,A、B两种物质的溶解度是A
(2)将t3°C的A、B两种物质的饱和溶液各200g,降温至t1°C,析出晶体的质量关系是A
(3)t2°C时,100g水中溶解50gA刚好饱和,那么50g水中溶解
(4)A溶液中混有少量的B,可以通过
考点:固体溶解度曲线及其作用,结晶的原理、方法及其应用,晶体和结晶的概念与现象
专题:溶液、浊液与溶解度
分析:(1)据溶解度曲线可比较同一温度下不同物质的溶解度大小;
(2)等质量的饱和溶液降低相同的温度,溶解度变化大的析出晶体多;
(3)据该温度下二者的溶解度和溶解度概念、溶质的质量分数计算式分析解答;
(4)据物质的溶解度受温度影响情况分析提纯物质的方法.
(2)等质量的饱和溶液降低相同的温度,溶解度变化大的析出晶体多;
(3)据该温度下二者的溶解度和溶解度概念、溶质的质量分数计算式分析解答;
(4)据物质的溶解度受温度影响情况分析提纯物质的方法.
解答:解(1)由图可知:t1°C时,A、B两种物质的溶解度是A 小于B;
(2)由图可知:t3°C~t1°C,A的溶解度受温度影响比B大,所以将t3°C的A、B两种物质的饱和溶液各200g,降温至t1°C,析出晶体的质量关系是A>B;
(3)t2°C时AB的溶解度曲线交于一点,二者的溶解度在该温度时相等,100g水中溶解50gA刚好饱和,则B也是这样,那么50g水中溶解25gB刚好达饱和,此时溶液的质量分数是
×100%≈33.3%;
(4)A的溶解度受温度影响比B大,所以若A溶液中混有少量的B,可以通过冷却热饱和溶液或降温结晶的方法提纯A;
故答案为:(1)<;(2)>;(3)25;33.3%;(4)冷却热饱和溶液(或降温结晶).
(2)由图可知:t3°C~t1°C,A的溶解度受温度影响比B大,所以将t3°C的A、B两种物质的饱和溶液各200g,降温至t1°C,析出晶体的质量关系是A>B;
(3)t2°C时AB的溶解度曲线交于一点,二者的溶解度在该温度时相等,100g水中溶解50gA刚好饱和,则B也是这样,那么50g水中溶解25gB刚好达饱和,此时溶液的质量分数是
| 25g |
| 75g |
(4)A的溶解度受温度影响比B大,所以若A溶液中混有少量的B,可以通过冷却热饱和溶液或降温结晶的方法提纯A;
故答案为:(1)<;(2)>;(3)25;33.3%;(4)冷却热饱和溶液(或降温结晶).
点评:本题难度不大,掌握溶解度曲线的意义、溶解度概念、溶质质量分数等相关知识即可顺利解答,若溶解度受温度影响变化大的物质中混有溶解度受温度影响变化小的物质,通常采用降温结晶的方法进行提纯.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
“关爱生命,拥抱健康”是人类永恒的主题.下列做法有利于人体健康的是( )
| A、多食水果和蔬菜,给人体补充维生素 |
| B、在牛奶中添加三聚氰胺 |
| C、用亚硝酸钠腌肉 |
| D、在辣椒酱中添加“苏丹红1号” |
下列几种作物无土栽培营养液中的成分中属于复合肥料的是( )
| A、Ca(NO3)2 |
| B、KCl |
| C、KNO3 |
| D、MgSO4?7H2O |
 同学们用Na2CO3溶液和浓HCl来研究简易灭火器的反应原理时,对废液的成分进行探究.
同学们用Na2CO3溶液和浓HCl来研究简易灭火器的反应原理时,对废液的成分进行探究.
 ”、“
”、“ ”、“
”、“ ”、“
”、“ ”代表不同原子,现对四瓶气体进行如下分类,用A、B…序号回答下列问题:
”代表不同原子,现对四瓶气体进行如下分类,用A、B…序号回答下列问题: