题目内容
我们知道,高温煅烧石灰石可制得生石灰和二氧化碳.现在一批石灰石,为了分析它的纯度,某学习小组取样品44g,充分煅烧后称得剩余固体的质量为26.4g(提示:假定杂质不反应).计算:(计算结果保留一位小数)
(1)生成二氧化碳的物质的量是多少?
(2)碳酸钙的质量是多少?石灰石中碳酸钙的纯度是多少?
(1)生成二氧化碳的物质的量是多少?
(2)碳酸钙的质量是多少?石灰石中碳酸钙的纯度是多少?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据化学方程式计算的步骤有:一设、二写、三找、四列、五答、六查.在本题中,首先根据质量守恒定律求出二氧化碳的质量;再根据化学方程式求生石灰的质量,然后求其纯度.
解答:解:(1)根据质量守恒定律,二氧化碳的质量=44g-26.4g=17.6g,则其物质的量为
=0.4mol;
(2)设碳酸钙的质量为x
CaCO3
CaO+CO2↑
100 44
x 17.6g
=
x=40g
石灰石的纯度=
×100%≈90.9%
答:生石灰的质量为:22.4g;碳酸钙的纯度为:90.9%.
答:(1)生成二氧化碳的物质的量是0.4mol;(2)碳酸钙的质量是40g,石灰石中碳酸钙的纯度是90.9%;
| 17.6g |
| 44g/mol |
(2)设碳酸钙的质量为x
CaCO3
| ||
100 44
x 17.6g
| 100 |
| x |
| 44 |
| 17.6g |
x=40g
石灰石的纯度=
| 40g |
| 44g |
答:生石灰的质量为:22.4g;碳酸钙的纯度为:90.9%.
答:(1)生成二氧化碳的物质的量是0.4mol;(2)碳酸钙的质量是40g,石灰石中碳酸钙的纯度是90.9%;
点评:本考点考查了根据化学方程式的计算,属于质量分数和化学方程式的综合应用,做题时要注意:化学方程式要写正确,始终不要忘记质量守恒定律,还要记牢“遇到差值要想气体”.是中考计算题中经常出现的题型.本考点主要出现在计算题中.

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目
下列物质属于纯净物的是( )
| A、雪碧饮料 | B、食醋 |
| C、加碘食盐 | D、蒸馏水 |
某物质不含氢氧两种元素,该物质可能是( )
| A、酸 | B、碱 | C、盐 | D、氧化物 |
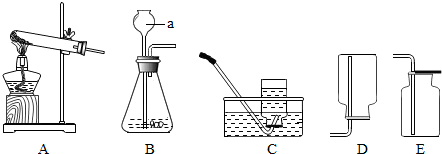
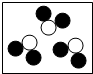
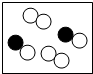


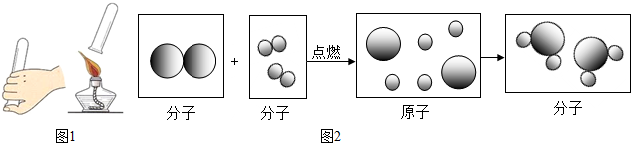
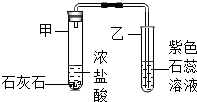 小伟设计了如图所示的装置进行实验.
小伟设计了如图所示的装置进行实验.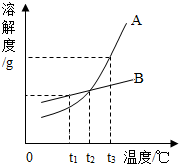 如图是A、B两种物质的溶解度曲线,根据图示回答下列问题:
如图是A、B两种物质的溶解度曲线,根据图示回答下列问题: