题目内容
为确定木炭还原氧化铜后的固体成分,请你与兴趣小组的同学完成以下探究.
【对固体猜想】
猜想Ⅰ:全部是金属铜;
猜想Ⅱ:除铜外,还含有氧化铜;
猜想Ⅲ:除铜外,还含有木炭;
猜想Ⅳ:除铜外,还含有
实验流程见如图
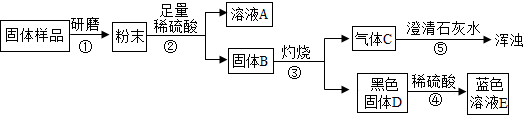
【问题与讨论】
(1)步骤②包括溶解、 两步操作.
(2)根据步骤③、④、⑤说明固体样品中含有 ;
(3)结合(2),如果溶液A显蓝色,则溶液A的溶质的化学式为 ,化学方程式为 ,则证明猜想 成立;如果溶液A无色,则证明猜想 成立.
【对固体猜想】
猜想Ⅰ:全部是金属铜;
猜想Ⅱ:除铜外,还含有氧化铜;
猜想Ⅲ:除铜外,还含有木炭;
猜想Ⅳ:除铜外,还含有
实验流程见如图

【问题与讨论】
(1)步骤②包括溶解、
(2)根据步骤③、④、⑤说明固体样品中含有
(3)结合(2),如果溶液A显蓝色,则溶液A的溶质的化学式为
考点:实验探究物质的组成成分以及含量,常见气体的检验与除杂方法,酸的化学性质,碳的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:【对固体猜想】反应物是氧化铜和碳,生成物是铜,根据数学中的组合知识,对三种物质进行组合即可得到所有的猜想,
【问题与讨论】(1)要将粉末状的固体分离成溶液和固体,需要先将样品配成溶液,然后进行过滤处理,
(2)我们所掌握的能使澄清石灰水变浑浊的气体是二氧化碳,与硫酸反应后,溶液显蓝色的是硫酸铜溶液.根据C、D 的现象推导出固体B的组成;
(3)若溶液显示蓝色,则说明含有氧化铜,若溶液不变蓝则说明没有氧化铜,可以据此进行解答.
【问题与讨论】(1)要将粉末状的固体分离成溶液和固体,需要先将样品配成溶液,然后进行过滤处理,
(2)我们所掌握的能使澄清石灰水变浑浊的气体是二氧化碳,与硫酸反应后,溶液显蓝色的是硫酸铜溶液.根据C、D 的现象推导出固体B的组成;
(3)若溶液显示蓝色,则说明含有氧化铜,若溶液不变蓝则说明没有氧化铜,可以据此进行解答.
解答:解:【对固体猜想】根据反应物是氧化铜和木炭,生成物的固体是铜,结合反应中的过量和不足问题,利用数学中的组合知识将三种物质任意组合,可以得到猜想Ⅳ为铜、氧化铜和木炭.
【问题与讨论】(1)要将粉末状的固体分离成溶液和固体,需要先将样品配成溶液,然后进行过滤操作.
(2)根据质量守恒定律,反应物中的元素有:碳、铜、氧,结合通入石灰水后出现浑浊,可以推出C是二氧化碳,固体B灼烧后得到的黑色物质与硫酸反应会得到蓝色溶液,可以推出D是氧化铜,根据C是二氧化碳、D是氧化铜,可以确定B的组成是碳和铜.
(3)氧化铜可以和稀硫酸反应生成蓝色溶液,所以加入硫酸后溶液显蓝色,可知该溶液中含有硫酸铜,故溶液A中的溶质为:CuSO4;该反应的化学方程式为:CuO+H2SO4═CuSO4+H2O;可知原粉末中有氧化铜,结合(2)中推导出B中有铜,也就是原粉末中有铜,所以原粉末中有铜和氧化铜和碳,可以判断出猜想IV正确,若溶液A不变蓝,则说明该固体粉末中没有氧化铜,故可以判断猜想Ⅲ正确.
故答案为:【对固体猜想】氧化铜和木炭.
【问题与讨论】(1)过滤.
(2)碳和铜.
(3)CuSO4;CuO+H2SO4═CuSO4+H2O;IV;Ⅲ.
【问题与讨论】(1)要将粉末状的固体分离成溶液和固体,需要先将样品配成溶液,然后进行过滤操作.
(2)根据质量守恒定律,反应物中的元素有:碳、铜、氧,结合通入石灰水后出现浑浊,可以推出C是二氧化碳,固体B灼烧后得到的黑色物质与硫酸反应会得到蓝色溶液,可以推出D是氧化铜,根据C是二氧化碳、D是氧化铜,可以确定B的组成是碳和铜.
(3)氧化铜可以和稀硫酸反应生成蓝色溶液,所以加入硫酸后溶液显蓝色,可知该溶液中含有硫酸铜,故溶液A中的溶质为:CuSO4;该反应的化学方程式为:CuO+H2SO4═CuSO4+H2O;可知原粉末中有氧化铜,结合(2)中推导出B中有铜,也就是原粉末中有铜,所以原粉末中有铜和氧化铜和碳,可以判断出猜想IV正确,若溶液A不变蓝,则说明该固体粉末中没有氧化铜,故可以判断猜想Ⅲ正确.
故答案为:【对固体猜想】氧化铜和木炭.
【问题与讨论】(1)过滤.
(2)碳和铜.
(3)CuSO4;CuO+H2SO4═CuSO4+H2O;IV;Ⅲ.
点评:在对固体猜想是要利用组合知识,总结到位,总结全面,对化学中典型的现象要加以识记,如带色的离子等.

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目
 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线. 
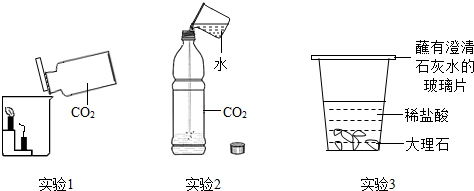
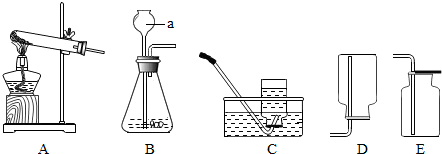
 不同类别的物质间存在着一定的关系,如图所示.(“-”表示相连的两种物质能发生反应,“→”表示某种物质可转化为另一种物质.)
不同类别的物质间存在着一定的关系,如图所示.(“-”表示相连的两种物质能发生反应,“→”表示某种物质可转化为另一种物质.) 用如图所示装置进行实验:当打开止水夹,挤压滴管将液体A滴入试管①时,观察到试管②有气泡产生,则
用如图所示装置进行实验:当打开止水夹,挤压滴管将液体A滴入试管①时,观察到试管②有气泡产生,则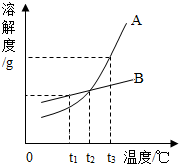 如图是A、B两种物质的溶解度曲线,根据图示回答下列问题:
如图是A、B两种物质的溶解度曲线,根据图示回答下列问题: