题目内容
9.某实验小组利用废硫酸液制备K2SO4并研究CaSO4•2H2O加热分解的产物.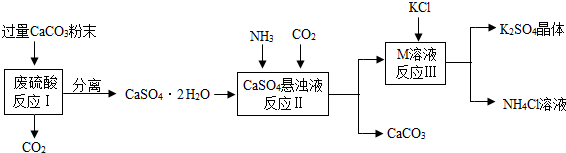
(1)将CaCO3研成粉末的目的是加快反应速率;
(2)上述流程中可循环使用的物质有CO2和CaCO3(填写化学式);
(3)反应Ⅲ中相关物质的溶解度如表.你认为反应Ⅲ在常温下能实现的原因是常温下K2SO4的溶解度小;
| 物质 | KCl | K2SO4 | NH4Cl | M |
| 溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
a、AgNO3溶液 b、过量的BaCl2溶液 c、过量的Ba(NO3)2溶液.
分析 解答此类题目时要反复阅读题意,明确题目的要求和前后的关联,然后进行解答.
(1)把反应物研成粉末是为了加快反应速率.
(2)如果生成物和反应物中都有某种物质,这种物质一般可循环利用;
(3)从生成物的溶解度大小考虑反应能否发生.
(4)结合实验目的判断,检验氯离子时要排除硫酸根的干扰.
解答 解:(1)将CaCO3研成粉末,可以增大反应物的接触面积,其目的是加快反应速率.故填:加快反应速率;
(2)观察上述流程,发现二氧化碳和碳酸钙既是反应物也是生成物,故可循环使用的物质有CO2和CaCO3.故填:CaCO3;
(3)根据复分解反应发生的条件,反应Ⅲ中随没有不溶物,但常温下K2SO4的溶解度小,在生成物中会以沉淀的形式出现,故反应可以进行.故填:常温下K2SO4的溶解度小;
(4)不用水而用饱和K2SO4溶液洗涤反应Ⅲ所得晶体的目的是减少K2SO4的溶解;为检验此晶体是否洗涤干净,可取最后一次洗涤液,先加入过量的Ba(NO3)2溶液,振荡、静置,目的是除去硫酸根,再向上层清液中滴加AgNO3溶液,如果没有白色沉淀,说明洗涤干净.故填:减少K2SO4的溶解;c;a.
点评 此题全面考查了学生对知识的掌握和应用能力,难度比较大,解答时一定要注意知识的前后的联系和综合运用.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.下列化学用语中,既能表示一种元素,又能表示一个原子,还能表示一种物质的是( )
| A. | N2 | B. | O | C. | Cu | D. | Al3+ |
4. 化学兴趣小组设计的创新实验是“火龙生字”.在成果展示现场,某同学用硝酸钾的热饱和溶液先在白纸上书写“火”字,晾干后白纸上出现硝酸钾晶体(见图1)用带火星的木条接触硝酸钾晶体,就会观察到白纸上写过字的地方燃烧并迅速蔓延,留下“火”字的黑色痕迹(见图2).在场的同学对此产生了浓厚的兴趣,并进行了如下研究:
化学兴趣小组设计的创新实验是“火龙生字”.在成果展示现场,某同学用硝酸钾的热饱和溶液先在白纸上书写“火”字,晾干后白纸上出现硝酸钾晶体(见图1)用带火星的木条接触硝酸钾晶体,就会观察到白纸上写过字的地方燃烧并迅速蔓延,留下“火”字的黑色痕迹(见图2).在场的同学对此产生了浓厚的兴趣,并进行了如下研究:
【提出问题】为什么附有硝酸钾的白纸更容易燃烧?
【查阅资料】硝酸钾受热易分解,生成亚硝酸钾(KNO2)和一种常见的气体单质.
【猜想与假设】对于生产的是什么气体,四位同学有如下猜测:
甲:二氧化氮; 乙:氮气; 丙:氧气; 丁:氢气;
同学丙指出不可能是二氧化氮、氢气,理由是:二氧化氮不是单质、硝酸钾中不含有氢元素.
【进行实验】四位同学设计了实验对同学丙的猜想进行了验证,他们的操作方法是:将少量硝酸钾晶体放在试管中加热,把带火星的木条放在试管中,观察到的现象是木条复燃,说明同学丙的猜想正确.硝酸钾分解的化学方程式是2KNO3$\frac{\underline{\;\;△\;\;}}{\;}$2KNO2+O2↑.
【解释与结论】白纸上写过字的地方更容易燃烧的原因是:硝酸钾晶体受热分解生成氧气,使写过字的白纸附近氧气的浓度增大.
【反思与评价】为什么要用“硝酸钾的热饱和溶液”书写文字?
已知硝酸钾在不同温度时的溶解度如下表:|
你对上述问题的解释是:硝酸钾的溶解度较大,用热饱和溶液能使白纸上附着更多的硝酸钾晶体.
 化学兴趣小组设计的创新实验是“火龙生字”.在成果展示现场,某同学用硝酸钾的热饱和溶液先在白纸上书写“火”字,晾干后白纸上出现硝酸钾晶体(见图1)用带火星的木条接触硝酸钾晶体,就会观察到白纸上写过字的地方燃烧并迅速蔓延,留下“火”字的黑色痕迹(见图2).在场的同学对此产生了浓厚的兴趣,并进行了如下研究:
化学兴趣小组设计的创新实验是“火龙生字”.在成果展示现场,某同学用硝酸钾的热饱和溶液先在白纸上书写“火”字,晾干后白纸上出现硝酸钾晶体(见图1)用带火星的木条接触硝酸钾晶体,就会观察到白纸上写过字的地方燃烧并迅速蔓延,留下“火”字的黑色痕迹(见图2).在场的同学对此产生了浓厚的兴趣,并进行了如下研究:【提出问题】为什么附有硝酸钾的白纸更容易燃烧?
【查阅资料】硝酸钾受热易分解,生成亚硝酸钾(KNO2)和一种常见的气体单质.
【猜想与假设】对于生产的是什么气体,四位同学有如下猜测:
甲:二氧化氮; 乙:氮气; 丙:氧气; 丁:氢气;
同学丙指出不可能是二氧化氮、氢气,理由是:二氧化氮不是单质、硝酸钾中不含有氢元素.
【进行实验】四位同学设计了实验对同学丙的猜想进行了验证,他们的操作方法是:将少量硝酸钾晶体放在试管中加热,把带火星的木条放在试管中,观察到的现象是木条复燃,说明同学丙的猜想正确.硝酸钾分解的化学方程式是2KNO3$\frac{\underline{\;\;△\;\;}}{\;}$2KNO2+O2↑.
【解释与结论】白纸上写过字的地方更容易燃烧的原因是:硝酸钾晶体受热分解生成氧气,使写过字的白纸附近氧气的浓度增大.
【反思与评价】为什么要用“硝酸钾的热饱和溶液”书写文字?
已知硝酸钾在不同温度时的溶解度如下表:|
| 温度/℃ | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 31.6 | 63.9 | 110 | 169 | 246 |
14.“鱼浮灵”主要成分是过碳酸钠(xNa2CO3•yH2O2),俗称固体双氧水.兴趣小组对其进行以下探究:
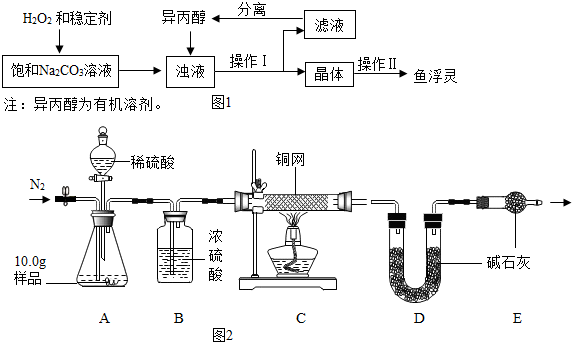
[性质探究](1)取少量“鱼浮灵”于试管中加水,有持续细小气泡缓慢放出;向试管中加入少量MnO2粉末,产生大量气泡.将带火星木条伸入试管,木条复燃,说明有O2生成;
(2)取实验(1)中上层清液,测得溶液PH>7;向溶液中滴加足量稀盐酸,产生大量气泡;将产生的气体通入澄清石灰水中,出现浑浊现象,说明有CO2生成;
结论:过碳酸钠具有Na2CO3和H2O2的双重化学性质.
[工业制备]
(3)稳定剂的作用是防止H2O2分解;稳定剂中MgCl2和Na2SiO3发生复分解反应,生成一种难溶物将过碳酸钠粒子包裹住,该反应的化学方程式为MgCl2+Na2SiO3=MgSiO3↓+2NaCl;
(4)浊液中加入异丙醇的作用是降低过碳酸钠的溶解度;
(5)图1操作Ⅱ中洗涤晶体的试剂最好选用C(填字母);
A、饱和NaCl溶液 B水 C异丙醇 D稀盐酸
(6)根据下表数据,你认为上述制备反应的最佳温度范围是15~20℃.
注:活性氧含量是指产品中能转化为O2的氧元素的质量分数.
[组成测定]
利用图2装置进行产品中活性氧含量测定和过碳酸钠(xNa2CO3•yH2O2)组成的测定(杂质对测定无影响).
查阅资料:①”鱼浮灵”中活性氧含量≥13.0%是一等品,≥10.5%是合格品.②过碳酸钠能与酸反应放出CO2和O2.
(7)实验前先缓慢通N2一段时间,加热铜网至红热后,再缓慢滴入过量稀硫酸,直至A中样品完全反应;继续缓慢通N2,其目的是使残留在装置中的气体全部被吸收;
(8)若先滴入稀硫酸,后加热铜网,会导致x:y的值偏大(填”偏大”或”偏小”);
(9)装置B的作用是①②(填序号);①除去气体中的水蒸气 ②便于观察和控制气流速度
(10)实验测得C装置中铜网增重1.2g,D装置增重2.2g.该产品中活性氧含量为12%;属于合格品(填”一等品”或”合格品”);x:y=2:3.

[性质探究](1)取少量“鱼浮灵”于试管中加水,有持续细小气泡缓慢放出;向试管中加入少量MnO2粉末,产生大量气泡.将带火星木条伸入试管,木条复燃,说明有O2生成;
(2)取实验(1)中上层清液,测得溶液PH>7;向溶液中滴加足量稀盐酸,产生大量气泡;将产生的气体通入澄清石灰水中,出现浑浊现象,说明有CO2生成;
结论:过碳酸钠具有Na2CO3和H2O2的双重化学性质.
[工业制备]
(3)稳定剂的作用是防止H2O2分解;稳定剂中MgCl2和Na2SiO3发生复分解反应,生成一种难溶物将过碳酸钠粒子包裹住,该反应的化学方程式为MgCl2+Na2SiO3=MgSiO3↓+2NaCl;
(4)浊液中加入异丙醇的作用是降低过碳酸钠的溶解度;
(5)图1操作Ⅱ中洗涤晶体的试剂最好选用C(填字母);
A、饱和NaCl溶液 B水 C异丙醇 D稀盐酸
(6)根据下表数据,你认为上述制备反应的最佳温度范围是15~20℃.
| 温度范围/℃ | 5~10 | 10~15 | 15~20 | 20~25 |
| 活性氧含量/% | 13.94 | 14.02 | 15.05 | 14.46 |
| “鱼浮灵”的产率/% | 85.49 | 85.78 | 88.38 | 83.01 |
[组成测定]
利用图2装置进行产品中活性氧含量测定和过碳酸钠(xNa2CO3•yH2O2)组成的测定(杂质对测定无影响).
查阅资料:①”鱼浮灵”中活性氧含量≥13.0%是一等品,≥10.5%是合格品.②过碳酸钠能与酸反应放出CO2和O2.
(7)实验前先缓慢通N2一段时间,加热铜网至红热后,再缓慢滴入过量稀硫酸,直至A中样品完全反应;继续缓慢通N2,其目的是使残留在装置中的气体全部被吸收;
(8)若先滴入稀硫酸,后加热铜网,会导致x:y的值偏大(填”偏大”或”偏小”);
(9)装置B的作用是①②(填序号);①除去气体中的水蒸气 ②便于观察和控制气流速度
(10)实验测得C装置中铜网增重1.2g,D装置增重2.2g.该产品中活性氧含量为12%;属于合格品(填”一等品”或”合格品”);x:y=2:3.
1.下列四组溶液,仅用组内物质就能鉴别出来的是( )
| A. | K2CO3、FeCl3、KOH、H2SO4 | B. | NaCl、MgCl2、K2SO4、CuSO4 | ||
| C. | NH4HCO3、Ba(OH)2、H2SO4、NaNO3 | D. | K2CO3、Na2SO4、BaCl2、NaOH |

