题目内容
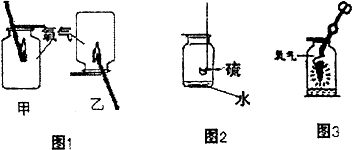
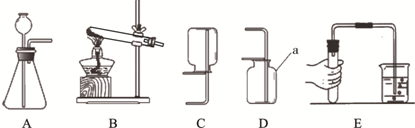
17.以下是初中化学的一些基本实验:
(1)上述实验中不能达到实验目的是A(填字母);
(2)A中可燃物应取过量的原因是确保集气瓶中的氧气完全反应;
(3)B中玻璃棒的作用是搅拌、散热;
(4)一段时间后,C中的实验现象为铁丝生锈,U型管中液面左高右低;
(5)铁丝在氧气中燃烧的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(6)D中玻璃管内实验现象是点燃未反应的CO,防止其污染空气.
分析 (1)A、B、C、D四个实验中:A实验生成物为二氧化碳气体,不能形成气压差,故不能达到实验目的;而B、C、D三个实验可以完成,能够能达到实验目的;
(2)A实验测定空气中氧气的含量,故应充分消耗氧气;
(3)B实验稀释浓硫酸,玻璃棒搅拌并及时散热;
(4)C实验铁丝生锈消耗空气中的氧气,管内外形成气压差,故U型管中液面左高右低;
(5)D实验一氧化碳还原氧化铁,已知反应物一氧化碳和氧化铁,生成物为二氧化碳和铁,反应条件为高温;
(6)反应完,将有尾气一氧化碳,故需要处理掉.
解答 解:(1)经分析A、B、C、D四个实验,A实验生成物为二氧化碳气体,不能形成气压差,故不能达到实验目的;
(2)A中可燃物应取过量的原因是确保集气瓶中的氧气完全反应;
(3)B中玻璃棒的作用是搅拌、散热;
(4)一段时间后,C中的实验现象为铁丝生锈,U型管中液面左高右低;
(5)D中硬质玻璃管内发生反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;酒精灯的作用是点燃未反应的CO,防止其污染空气.
故答为:
(1)A;
(2)确保集气瓶中的氧气完全反应;
(3)搅拌、散热;
(4)铁丝生锈,U型管中液面左高右低;
(5)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(6)点燃未反应的CO,防止其污染空气.
点评 了解金属生锈的条件,探究测定空气中氧气含量的方法;掌握浓硫酸的性质和稀释方法及其注意事项;掌握一氧化碳还原氧化铁的实验原理及注意事项.

练习册系列答案
相关题目
8.质子数和电子数都相同的两种微粒它们可能是( )?
| A. | 两种不同元素的原子 | B. | 两种不同物质的分子? | ||
| C. | 两种不同元素的阳离子 | D. | 两种不同元素的阴离子 |
12.下列各组物质只用一种化学试剂就可以鉴别的是( )
| A. | 厨房中的食盐、味精、蔗糖三种调味品 | |
| B. | 硫酸钠、碳酸钠、硝酸钠三种无色溶液 | |
| C. | 食盐、烧碱、氯化铵三种白色固体 | |
| D. | 生石灰、熟石灰、淀粉三种白色固体 |
9.某实验小组利用废硫酸液制备K2SO4并研究CaSO4•2H2O加热分解的产物.
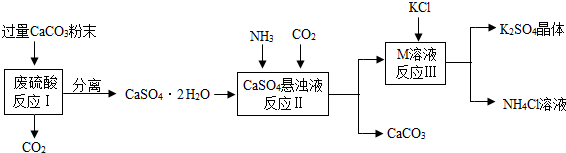
(1)将CaCO3研成粉末的目的是加快反应速率;
(2)上述流程中可循环使用的物质有CO2和CaCO3(填写化学式);
(3)反应Ⅲ中相关物质的溶解度如表.你认为反应Ⅲ在常温下能实现的原因是常温下K2SO4的溶解度小;
(4)不用水而用饱和K2SO4溶液洗涤反应Ⅲ所得晶体的目的是减少K2SO4的溶解;为检验此晶体是否洗涤干净,可取最后一次洗涤液,先加入c(选填序号,下同),振荡、静置,再向上层清液中滴加a,观察现象即可判断.
a、AgNO3溶液 b、过量的BaCl2溶液 c、过量的Ba(NO3)2溶液.

(1)将CaCO3研成粉末的目的是加快反应速率;
(2)上述流程中可循环使用的物质有CO2和CaCO3(填写化学式);
(3)反应Ⅲ中相关物质的溶解度如表.你认为反应Ⅲ在常温下能实现的原因是常温下K2SO4的溶解度小;
| 物质 | KCl | K2SO4 | NH4Cl | M |
| 溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
a、AgNO3溶液 b、过量的BaCl2溶液 c、过量的Ba(NO3)2溶液.
6.以下是小明同学在家做的四个家庭小实验,其中你认为只发生物理变化的是( )
| A. | 用食醋除去水壶中的水垢 | B. | 用灼烧的方法区别羊毛线和棉线 | ||
| C. | 铁钉锈蚀条件的探究 | D. | 用活性炭净化水 |
7.下列验证实验不能成功的是( )
| A. |  CO2与烧碱溶液反应 | B. |  不同物质着火点不同 | ||
| C. |  分子在不断运动 | D. |  质量守恒定律 |