题目内容
1.下列四组溶液,仅用组内物质就能鉴别出来的是( )| A. | K2CO3、FeCl3、KOH、H2SO4 | B. | NaCl、MgCl2、K2SO4、CuSO4 | ||
| C. | NH4HCO3、Ba(OH)2、H2SO4、NaNO3 | D. | K2CO3、Na2SO4、BaCl2、NaOH |
分析 不用其他试剂,就能将组内物质鉴别出来,首先需考虑物质的颜色,然后将鉴别出来的物质与其他物质混合,根据现象的不同加以鉴别,若物质都是没有颜色,则让溶液之间两两混合,根据不同的实验现象加以鉴别.
解答 解:A、观察,呈黄色的为FeCl3溶液,将FeCl3少量分别滴加到盛有剩余三种溶液少量的试管中,出现红褐色沉淀的是KOH溶液,取剩余溶液中的一种滴加到红褐色沉淀中,沉淀消失,加入的是H2SO4溶液,剩余一种是K2CO3溶液,故选项正确;
B、首先依据铜离子显蓝色鉴别出CuSO4溶液,然后将CuSO4溶液滴入剩余的三种溶液中,均无现象发生,不能鉴别,故选项错误;
C、组内四种物质的溶液两两混合时,其中有一种溶液与其它三种溶液混合时出现一次白色沉淀和同时产生白色沉淀和放出有刺激性气味的气体,该溶液为Ba(OH)2溶液;与Ba(OH)2溶液只产生白色沉淀的溶液为H2SO4,同时产生白色沉淀和放出有刺激性气味的气体的为NH4HCO3;与Ba(OH)2溶液混合无任何明显现象的为NaNO3溶液;不加其他试剂可以鉴别;且均为无色溶液,故选项正确;
D、组内四种物质的溶液两两混合时,BaCl2溶液与K2CO3、Na2SO4溶液反应均能产生白色沉淀,但其余两两混合均没有明显现象,不加其他试剂无法鉴别,故选项错误.
故选:AC.
点评 本题考查了常见物质的鉴别,解答不另加试剂就能鉴别的题目时,若选项中有带色的离子,首先鉴别,然后再鉴别其它的物质;若都没有颜色,可将溶液两两混合,根据混合后的现象进行鉴别.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
11.硒元素具有抗衰老、抑制癌细胞的功能,其化学性质与硫相似.硒的元素符号为Se,相对原子质量为79,其对应的含氧酸为H2SeO4.下列说法正确的是( )
| A. | H2SeO4应读作硒酸 | |
| B. | H2SeO4的相对分子质量为145 | |
| C. | H2SeO4中Se的化合价为+4 | |
| D. | H2SeO4中组成元素H、Se、O的质量比为2:1:4 |
12.下列各组物质只用一种化学试剂就可以鉴别的是( )
| A. | 厨房中的食盐、味精、蔗糖三种调味品 | |
| B. | 硫酸钠、碳酸钠、硝酸钠三种无色溶液 | |
| C. | 食盐、烧碱、氯化铵三种白色固体 | |
| D. | 生石灰、熟石灰、淀粉三种白色固体 |
9.某实验小组利用废硫酸液制备K2SO4并研究CaSO4•2H2O加热分解的产物.
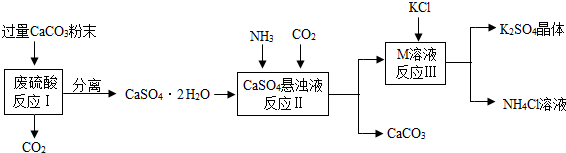
(1)将CaCO3研成粉末的目的是加快反应速率;
(2)上述流程中可循环使用的物质有CO2和CaCO3(填写化学式);
(3)反应Ⅲ中相关物质的溶解度如表.你认为反应Ⅲ在常温下能实现的原因是常温下K2SO4的溶解度小;
(4)不用水而用饱和K2SO4溶液洗涤反应Ⅲ所得晶体的目的是减少K2SO4的溶解;为检验此晶体是否洗涤干净,可取最后一次洗涤液,先加入c(选填序号,下同),振荡、静置,再向上层清液中滴加a,观察现象即可判断.
a、AgNO3溶液 b、过量的BaCl2溶液 c、过量的Ba(NO3)2溶液.

(1)将CaCO3研成粉末的目的是加快反应速率;
(2)上述流程中可循环使用的物质有CO2和CaCO3(填写化学式);
(3)反应Ⅲ中相关物质的溶解度如表.你认为反应Ⅲ在常温下能实现的原因是常温下K2SO4的溶解度小;
| 物质 | KCl | K2SO4 | NH4Cl | M |
| 溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
a、AgNO3溶液 b、过量的BaCl2溶液 c、过量的Ba(NO3)2溶液.
6.以下是小明同学在家做的四个家庭小实验,其中你认为只发生物理变化的是( )
| A. | 用食醋除去水壶中的水垢 | B. | 用灼烧的方法区别羊毛线和棉线 | ||
| C. | 铁钉锈蚀条件的探究 | D. | 用活性炭净化水 |
13.某同学为探究X.Y.Z三种金属(都不是银)的活动性顺序,做了以下实验:(1)把X和Y分别放在稀硫酸中,X溶解并放出氢气,Y不反应.(2)把Y和Z放入硝酸银溶液中,在Y表面有银析出,而Z没有变化,则三属的活动性顺序有强到弱的是.( )
| A. | X>Y>Z | B. | X>Z>Y | C. | Y>Z>X | D. | Z>X>Y |
10.复习时,常用专题探究的方法学习常见物质的组成、性质与制取,课堂上老师引导我们回顾了几个探究实验.
探究1:研究常见物的质组成.

实验A、B、C都是研究物质组成的实验.从研究方法得知,实验A是利用可燃物消耗瓶内的氧气,使瓶内压强减小来推测空气里氧气含量的.B实验是通过证明生成物的元素种类来推断水的组成的.而C实验与B(填实验代号)实验的方法相同.
探究2:研究常见物质性质--氢氧化钠与硫酸是否刚好完全中和.
(1)探索:用玻璃棒蘸取反应后的溶液滴在pH试纸上,发现该溶液的pH<7,说明硫酸过量.
(2)验证:
探究3:研究常见物质制取--制取氢氧化钠溶液.
小京同学向盛有澄清石灰水的烧杯中加入过量的碳酸钠溶液,生成白色沉淀,过滤后得到无色溶液,他说:“我制得了氢氧化钠溶液!”
小欢同学却说:“这种无色溶液中不一定含有氢氧化钠.”提出了如下实验:
小红认为小欢的实验方案也不严密,不能证实无色溶液中一定含有氢氧化钠,理由是碳酸钠溶液也能使无色酚酞试液变红.
小红设计了另一个实验,证明上述溶液中有氢氧化钠.实验步骤实验现象实验结论用试管取无色溶液少许,滴加过量的氯化钙(氯化钡)溶液,充分反应后静置,取上层清液滴加无色酚酞试液无色产生白色沉淀,无色酚酞试液变红无色溶液中确实含有氢氧化钠
实验小结:上述溶液的溶质中有NaOH和Na2CO3(写化学式).
探究1:研究常见物的质组成.

实验A、B、C都是研究物质组成的实验.从研究方法得知,实验A是利用可燃物消耗瓶内的氧气,使瓶内压强减小来推测空气里氧气含量的.B实验是通过证明生成物的元素种类来推断水的组成的.而C实验与B(填实验代号)实验的方法相同.
探究2:研究常见物质性质--氢氧化钠与硫酸是否刚好完全中和.
(1)探索:用玻璃棒蘸取反应后的溶液滴在pH试纸上,发现该溶液的pH<7,说明硫酸过量.
(2)验证:
| 实验内容 | 实验现象 | 解释与结论 |
| 取反应后少量溶液于试管中, 加入锌粒 | 有气泡产生 | 证明硫酸过量 |
小京同学向盛有澄清石灰水的烧杯中加入过量的碳酸钠溶液,生成白色沉淀,过滤后得到无色溶液,他说:“我制得了氢氧化钠溶液!”
小欢同学却说:“这种无色溶液中不一定含有氢氧化钠.”提出了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 用试管取无色溶液少许,滴入2滴无色酚酞试液 | 无色酚酞试液变红 | 无色溶液中含有氢氧化钠 |
小红设计了另一个实验,证明上述溶液中有氢氧化钠.实验步骤实验现象实验结论用试管取无色溶液少许,滴加过量的氯化钙(氯化钡)溶液,充分反应后静置,取上层清液滴加无色酚酞试液无色产生白色沉淀,无色酚酞试液变红无色溶液中确实含有氢氧化钠
实验小结:上述溶液的溶质中有NaOH和Na2CO3(写化学式).
 胃酸过多须服用抗酸药物(能与盐酸反应).如图为铝碳酸镁说明书的部分内容.兴趣小组对该药物开展如下探究.
胃酸过多须服用抗酸药物(能与盐酸反应).如图为铝碳酸镁说明书的部分内容.兴趣小组对该药物开展如下探究.