��Ŀ����
����Ŀ����ͼ1��ʵ���ҳ��������Ʊ�װ�ã���ͼ�ش����⣺
![]() ѡ��Cװ���ռ���������Ϊ______���������ǵ�ľ̿����ʢ�������ļ���ƿ�У�ʵ��������______��
ѡ��Cװ���ռ���������Ϊ______���������ǵ�ľ̿����ʢ�������ļ���ƿ�У�ʵ��������______��
![]() ʵ������ȡ������
ʵ������ȡ������![]() ��
��![]() �̣�
�̣�![]()
![]() ��
��![]() ��Ҫ��ȡ���ռ�����İ�������ѡװ����ȷ������˳����______
��Ҫ��ȡ���ռ�����İ�������ѡװ����ȷ������˳����______![]() ______
______![]() ______
______![]() ����ĸ����
����ĸ����![]() ��
��
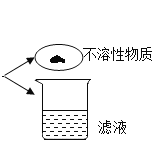
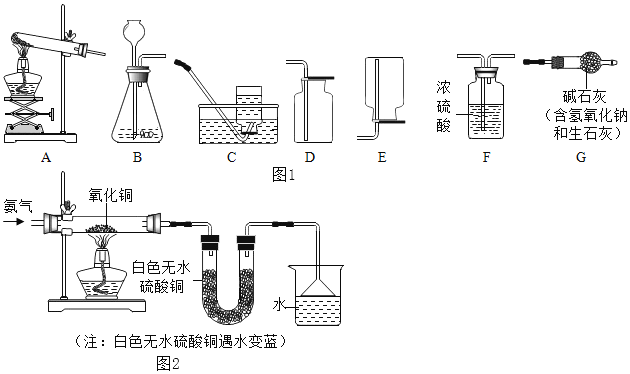
![]() Ϊ̽�����������ʣ�����ͼ2װ�ý���ʵ�顣�۲쵽��ɫ��ĩ��죬��ɫ��ˮ����ͭ������ͬʱ��Ӧ�л���һ�����嵥�����ɡ�
Ϊ̽�����������ʣ�����ͼ2װ�ý���ʵ�顣�۲쵽��ɫ��ĩ��죬��ɫ��ˮ����ͭ������ͬʱ��Ӧ�л���һ�����嵥�����ɡ�
���������ϣ�������ͭ![]() �Ǻ�ɫ���壬����ϡ���ᷴӦ��
�Ǻ�ɫ���壬����ϡ���ᷴӦ��![]() ��
��
��������⣩�õ��ĺ�ɫ������ʲô��
�����룩����Cu������![]() ������______��
������______��
������ٳ������������з�����Ӧ�Ļ�ѧ����ʽΪ______��˵��![]() ���л�ԭ�ԡ�
���л�ԭ�ԡ�
�����ʵ�飩�������һ����ʵ������֤��ɫ�������Ƿ����![]() ��______��
��______��
���𰸡�������������ˮ ľ̿��ȼ�������� A G E Cu��![]()
![]() ʵ�鲽�裺ȡ������ɫ�������Թ��У���������ϡ���ʵ�������ۣ����ɫ���岿���ܽ⣬��Һ������֤����ɫ��������Cu2O������Һ����ɫ������Cu2O��
ʵ�鲽�裺ȡ������ɫ�������Թ��У���������ϡ���ʵ�������ۣ����ɫ���岿���ܽ⣬��Һ������֤����ɫ��������Cu2O������Һ����ɫ������Cu2O��
��������
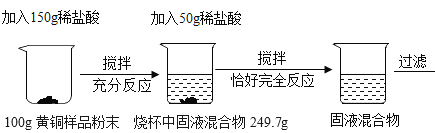
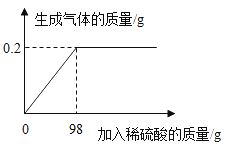
��1��������������ˮ��������ˮ���ռ����������ǵ�ľ̿����ʢ�������ļ���ƿ��ʱ��ľ̿��ȼ�������⡣
��2����ȡ�����ķ�Ӧ��Ϊ���壬��Ӧ����Ϊ���ȣ���ѡ��Aװ������Ӧװ�ã�Ũ���������ԣ�������������NH3��Ӧѡ��Gװ�ã���������Է�������Ϊ17��С�ڿ�����ƽ��ֵ29��������ܶ�С�ڿ���������������ſ������ռ�����ѡ��Eװ�á�
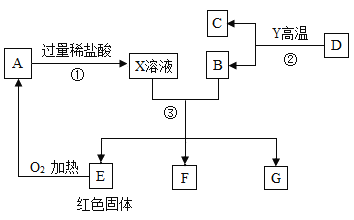
��3���ȵ��ĺ�ɫ���ʿ���������һ�֣�Ҳ���������ֻ�ϣ���˿�����Cu��Cu2O����
������![]() ��������������Cu����ɫ��ˮ����ͭ������֤��������H2O�����������غ㶨�ɿ�֪����һ�����嵥�����ɵ�Ԫ����ɵģ���N2����ѧ����ʽΪ
��������������Cu����ɫ��ˮ����ͭ������֤��������H2O�����������غ㶨�ɿ�֪����һ�����嵥�����ɵ�Ԫ����ɵģ���N2����ѧ����ʽΪ![]() ��
��
������֪��������ͭ![]() �Ǻ�ɫ���壬����ϡ���ᷴӦ����ѧ����ʽΪ
�Ǻ�ɫ���壬����ϡ���ᷴӦ����ѧ����ʽΪ![]() ��������Ʒ�м���ϡ���ᣬͨ���ж��Ƿ���CuSO4��Cu�������ƶ���Ʒ������Cu2O��ʵ�鲽�裺ȡ������ɫ�������Թ��У���������ϡ���ʵ�������ۣ����ɫ���岿���ܽ⣬��Һ������֤����ɫ��������Cu2O������Һ����ɫ������Cu2O��
��������Ʒ�м���ϡ���ᣬͨ���ж��Ƿ���CuSO4��Cu�������ƶ���Ʒ������Cu2O��ʵ�鲽�裺ȡ������ɫ�������Թ��У���������ϡ���ʵ�������ۣ����ɫ���岿���ܽ⣬��Һ������֤����ɫ��������Cu2O������Һ����ɫ������Cu2O��

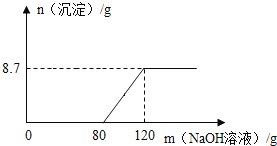
����Ŀ�������Ƿ������ÿ����е�NaOH��������ʵ��![]() ������ˮ��
������ˮ��![]() �����в���������
�������������![]() ����
����![]()
��� | ʵ��Ŀ�� | ʵ�鷽�� |
�� | ֤������ | ȡ�������壬��ˮ�ܽ⣬�μ�����ϡ���ᣬ�۲��Ƿ������ݲ��� |
�� | ȷ���ɷ� | ȡ�������壬����ʯ��ˮ�����ˣ�����Һ�еμӷ�̪��Һ |
�� | �ⶨ���� | ȡag��Ʒ�������Ȼ�����Һ��ַ�Ӧ�����������ˡ�ϴ�ӡ�����õ�mg���� |
�� | ��ȥ���� | ȡһ�������壬��ˮ�ܽ⣬�μӳ���ʯ��ˮ��ǡ����ȫ��Ӧ������ |
A.��B.��C.��D.��