题目内容
【题目】向盛有100g稀硫酸的烧杯中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入NaOH溶液,所得沉淀质量与加入NaOH溶液的质量关系如图所示。
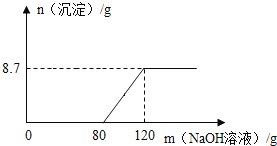
(1)反应生成沉淀的质量为_____克。
(2)镁粉完全溶解后所得溶液中的溶质成分为_____。
(3)计算氢氧化钠溶液的溶质质量分数_____(要求写出计算过程)。
【答案】8.7 H2SO4、MgSO4 30%
【解析】
(1)由图可知,生成沉淀即氢氧化镁的质量为 8.7g
(2)镁粉完全溶解后所得溶液中由于加入氢氧化钠开始没有沉淀,说明有剩余的硫酸,所以溶质成分为 H2SO4、MgSO4。
(3)设氢氧化钠溶液的溶质质量分数为x。
与氢氧化镁生成有关的氢氧化钠溶液的质量为120g-80g=40g
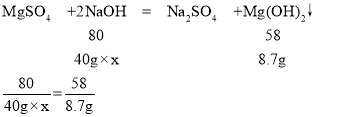
x=30%
故答案为:
(1)8.7;
(2)H2SO4、MgSO4;
(3)30%。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】2018年5月18日我国第一艘国产航母试海成功,航母的许多电子元件使用了黄铜。为测定某黄铜(假设合金中仅含铜、锌)中铜的质量分数,兴趣小组同学称取20g黄铜粉末于烧杯中,将80g稀硫酸分四次加入,充分反应,测得实验数据如下表所示:
第一次 | 第二次 | 第三次 | 第四次 | |
加入稀硫酸的质量/g | 20 | 20 | 20 | 20 |
烧杯中剩余物的质量/g | 39.92 | 59.84 | 79.80 | 99.80 |
(1)黄铜粉末完全反应生成氢气的总质量为________g
(2)该黄铜中铜的质量分数为多少_______?(写出计算过程)
(3)第三次实验后所得溶液的溶质为__________。
【题目】如图是A物质的溶解度曲线图,下表是B物质在不同温度时的溶解度。
温度/℃ | 0 | 20 | 40 | 60 | 80 |
B物质溶解度/g | 32 | 35 | 40 | 45 | 55 |

(1)请根据上表数据在图上绘制出B物质的溶解度曲线_____。
(2)_____℃时,A、B两种物质的饱和溶液中溶质的质量分数相等。
(3)若要从A的溶液中提取A物质,小明同学认为要用蒸发溶剂水的方法;小娟同学认为要用冷却热饱和溶液结晶的方法。你认为_____同学的方法合理。
(4)40℃时,要使240g A物质M点的溶液变成该温度下的饱和溶液,需要加A的质量为_____g。