题目内容
11.用置换反应验证锌的金属活动性比铜强,下列各组药品不能达到目的是( )| A. | Fe、ZnSO4、CuSO4 | B. | Zn、Cu、H2SO4 | C. | Zn、Cu、FeSO4 | D. | Zn、Cu、AgNO3 |
分析 根据已有的知识进行分析,在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,氢前的金属能与酸反应生成氢气,据此解答.
解答 解:A、将铁加入硫酸锌溶液中,没有现象,说明铁位于锌的后面,将铁加入硫酸铜溶液中,锌的表面有红色固体出现,说明铁位于铜的前面,能证明锌和铜的活动性强弱,故能达到目的;
B、将锌、铜加入硫酸溶液中,锌反应有气泡冒出,铜不反应,无现象,说明铜位于氢的后面,锌位于氢的前面,能证明锌和铜的活动性强弱,故能达到目的;
C、将铜加入硫酸亚铁溶液中,没有现象,说明铜位于铁的后面,将锌加入硫酸亚铁溶液中,能置换出铁,说明锌位于铁的前面,能证明锌和铜的活动性强弱,故能达到目的;
D、将锌和铜加入硝酸银溶液中,均发生反应,证明铜、锌位于银的前面,但是不能证明铁和铜的活动性强弱,故不能达到目的.
故选:D.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
相关题目
15.松花蛋也叫皮蛋,于明朝初年问世,一向为国人所喜好.但近日美国CNN将皮蛋列入全球十大最恶心的食品之一.消息一出,舆论哗然.其实这只是东西方饮食文化的差异所致,我们中国人不是把肯德基、麦当劳称之为垃圾食品.某兴趣小组决定探个究竟?查阅资料得知其腌制配方有多种,但主要配料为生石灰(CaO)、Na2CO3和食盐(NaCl).将一定比例的配料用水和粘土调制成糊状,敷于蛋上,密封保存数日后可食用.
(1)松花皮蛋外的糊状物经水溶解,过滤,滤液中肯定含有的溶质为NaOH、NaCl,可能含有的物质为Ca(OH)2或Na2CO3.
(2)某同学设计如上表所示的实验方案,探究(1)所得滤液中可能含有的物质是否存在,请你帮他完善实验方案.
(1)松花皮蛋外的糊状物经水溶解,过滤,滤液中肯定含有的溶质为NaOH、NaCl,可能含有的物质为Ca(OH)2或Na2CO3.
| 实 验 步 骤 | 实 验 现 象 | 实 验 结 论 |
| ①取少量滤液,滴加适量HCl溶液 | 若出现气泡 | 滤液中含Na2CO3 |
| 若无上述现象 | 滤液中无Na2CO3 | |
| ②取少量滤液,滴加适量 碳酸钠溶液 | 若出现白色沉淀 | 滤液中含Ca(OH)2 |
| 若无上述现象 | 滤液中无Ca(OH)2 |
6. 氢化钙固体是登山运动员常用的能源提供剂,某探究小组的同学通过查阅是知氢化钙(CaH2)遇水反应生成氢氧化钙和氢气.
氢化钙固体是登山运动员常用的能源提供剂,某探究小组的同学通过查阅是知氢化钙(CaH2)遇水反应生成氢氧化钙和氢气.
探究小组的同学把一定量的CaH2加入NaCO3溶液中,充分反应后过滤,得到了滤渣和滤液,经检验滤渣的万分是碳酸钙.
提出问题,溶液溶质成分是什么?
猜想与假设:
猜想1:NaOH
猜想2:NaOH Ca(OH)2
猜想3:NaOH Na2CO3
猜想4:NaOH Na2CO3 Ca(OH)2
经过讨论大家一致认为猜想不合理,请用化学方程式说明原因Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
实验验证:
反思与拓展:
(1)若向NH4Cl的溶液中加一定量的CaH2充分反应,产生的气体是氢气、氨气
(2)登山运动员常用作为能源提供剂,与氢气相比,其优点是携带安全
(3)取某碳酸钠样品放入烧杯中,加入95.5g水充分溶解,再向其中加入稀硫酸,反应放出气体的总质量与所加入稀硫酸的质量关系如图,请回答:
①当加入196g稀硫酸时,放出气体的质量为4.4g
②计算加入的稀硫酸溶液的浓度10%
③试计算求出加入96g稀硫酸(即烧杯中的溶液的浓度)
 氢化钙固体是登山运动员常用的能源提供剂,某探究小组的同学通过查阅是知氢化钙(CaH2)遇水反应生成氢氧化钙和氢气.
氢化钙固体是登山运动员常用的能源提供剂,某探究小组的同学通过查阅是知氢化钙(CaH2)遇水反应生成氢氧化钙和氢气.探究小组的同学把一定量的CaH2加入NaCO3溶液中,充分反应后过滤,得到了滤渣和滤液,经检验滤渣的万分是碳酸钙.
提出问题,溶液溶质成分是什么?
猜想与假设:
猜想1:NaOH
猜想2:NaOH Ca(OH)2
猜想3:NaOH Na2CO3
猜想4:NaOH Na2CO3 Ca(OH)2
经过讨论大家一致认为猜想不合理,请用化学方程式说明原因Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
实验验证:
| 实验 | 现象 | 结论 |
| 实验一:取滤液,向其中滴入少量碳酸钠溶液 | 无明显现象 | 猜想2不成立 |
| 实验二:另取滤液向其中加入稀盐酸 | 先无变化后产生气泡 | 猜想3成立. |
(1)若向NH4Cl的溶液中加一定量的CaH2充分反应,产生的气体是氢气、氨气
(2)登山运动员常用作为能源提供剂,与氢气相比,其优点是携带安全
(3)取某碳酸钠样品放入烧杯中,加入95.5g水充分溶解,再向其中加入稀硫酸,反应放出气体的总质量与所加入稀硫酸的质量关系如图,请回答:
①当加入196g稀硫酸时,放出气体的质量为4.4g
②计算加入的稀硫酸溶液的浓度10%
③试计算求出加入96g稀硫酸(即烧杯中的溶液的浓度)
20.下列图象能正确反映相关实验过程中量的变化的是( )
| A. | 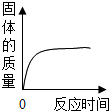 加热分解高锰酸钾 | B. | 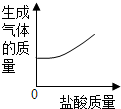 在变质的NaOH溶液中滴加稀盐酸 | ||
| C. | 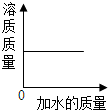 稀释NaCl溶液 | D. | 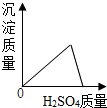 将H2SO4滴入BaCl2溶液中 |
1.对于二氧化锰具有的作用,叙述正确的是(( )
| A. | 加快反应速率 | B. | 改变反应速率 | ||
| C. | 对氯酸钾的分解反应有催化作用 | D. | 能增加氯酸钾放出氧气的质量 |