题目内容
6.氯化钠和氯化镁是重要的化工原料.某粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4等物质,为了从中提取较纯的氯化镁和氯化钠,设计如图实验方案: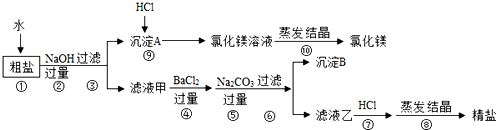
请回答下列问题:
Ⅰ.步骤①溶解过程中用玻璃棒搅拌的目的是加速溶解.
Ⅱ.步骤④⑤的顺序颠倒会引发的后果是精盐中会混有氯化钡.
Ⅲ.滤液乙中所含的溶质除氯化钠外还含有碳酸钠和氢氧化钠;
Ⅳ.写出步骤⑨中反应的化学方程式Mg(OH)2+2HCl=MgCl2+2H2O.
Ⅴ.实验所得精盐质量大于粗盐中氯化钠的质量,实验中产生新的NaCl的反应共有6个.
分析 Ⅰ.根据溶解过程玻璃棒的作用来解答;
Ⅱ.根据氯化钡除SO42-,碳酸钠除Ca2+和前面过量的钡离子;加入的碳酸钠溶液应该放在氯化钡溶液之后,否则多余的钡离子无法除去进行分析;
Ⅲ.根据除杂过程进行分析;
Ⅳ.根据氢氧化镁和盐酸反应生成氯化镁和水进行分析;
Ⅴ.根据除杂过程进行分析.
解答 解:正确的操作步骤为:
(1)将粗盐溶于足量水中制成溶液;
(2)向溶液中加入足量的NaOH溶液,除去Mg2+,反应的方程式为:2NaOH+MgCl2=Mg(OH)2↓+2NaCl,过滤,除去滤渣;
(3)向上述溶液中加入足量的BaCl2溶液,除去SO42-,反应的化学方程式为:Na2SO4+BaCl2=BaSO4↓+2NaCl;
(4)向上述滤液中加入足量的Na2CO3溶液,除去Ca2+、Ba2+,反应的方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl,Na2CO3+BaCl2=BaCO3↓+2NaCl;
(5)向(4)滤液中滴加稀盐酸,调节PH=7,除去CO32-和OH-,反应的化学方程式为:Na2CO3+2HCl=H2O+CO2↑+2NaCl,NaOH+HCl=NaCl+H2O;
(6)将NaCl溶液蒸发,洗涤干燥,即得较纯净的食盐;
其中加入氢氧化钠的顺序中,只要放在过滤之前即可,加入碳酸钠溶液必须放在加入氯化钡溶液之后,否则多余的钡离子无法除去,
Ⅰ.溶解过程中用玻璃棒搅拌的目的是加速溶解;
Ⅱ.氯化钡除SO42-,碳酸钠除Ca2+和前面过量的钡离子;加入的碳酸钠溶液应该放在氯化钡溶液之后,否则多余的钡离子无法除去;
Ⅲ.根据上述除杂过程可知,滤液乙中所含的溶质除氯化钠外还含有碳酸钠和氢氧化钠;
Ⅳ.在步骤⑦中若加入的盐酸略过量,不会对实验结果造成影响,因为盐酸具有挥发性,蒸发时氯化氢气体挥发掉;
Ⅴ.根据上述除杂过程可知,整个过程中产生新的NaCl的反应共有6个.
故答案为:Ⅰ.加速溶解;
Ⅱ.精盐中会混有氯化钡;
Ⅲ.碳酸钠和氢氧化钠;
Ⅳ.Mg(OH)2+2HCl=MgCl2+2H2O;
Ⅴ.6.
点评 本题主要考查了盐的性质、除杂的方法和原则,除去多种杂质时,要考虑加入试剂的顺序,为了保证将杂质除尽,所加试剂必须过量,因此为了不引进新的杂质,后面加入的试剂要能够除去前面所进入的过量试剂.

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案(1)提出问题:氢氧化钙是否变质?
(2)猜想与假设:同学们经过讨论认为样品存在三种可能情况:
①没有变质,为Ca(OH)2;②部分变质,为CaCO3、Ca(OH)2(或碳酸钙、氢氧化钙);③全部变质,为CaCO3.
(3)实验探究:
| 实验步骤及操作 | 实验现象 | 实验结论 |
| 取样于试管中,加入足量蒸馏水振荡,静置 ①取上层清液,滴入无色酚酞试液 ②倒去上层清液,再向试管中的残渣注入稀盐酸 | ①无色酚酞试液变红 ② | 部分变质 |
| ①无色酚酞试液不变红 ② | ||
| ①无色酚酞试液变红 ②没有气泡产生 |
| A. | 干冰用作制冷剂-干冰升华吸收大量热 | |
| B. | 白磷要保存在水中-白磷着火点低 | |
| C. | 氧气可以用于气焊气割-氧气有可燃性 | |
| D. | 用炭黑作画可以保存很长时间不变色-常温下炭黑的化学性质稳定 |
| A. | 降低可燃物的着火点 | B. | 防止燃烧产物污染空气 | ||
| C. | 降低温度到可燃物的着火点以下 | D. | 水分解出不助燃的物质 |
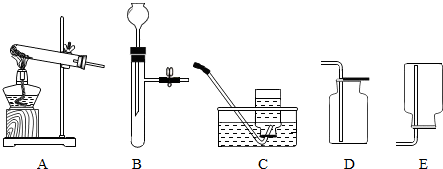
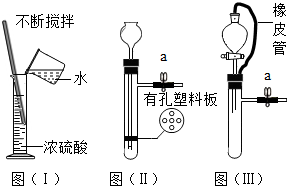
 如图是某同学用来除去水中难溶性杂质时所采用的过滤装置图.试回答:
如图是某同学用来除去水中难溶性杂质时所采用的过滤装置图.试回答: