题目内容
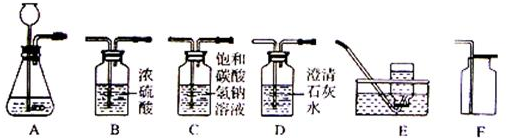
15.用集气瓶可完成多种实验,请根据如下实验装置示意图,回答有关问题: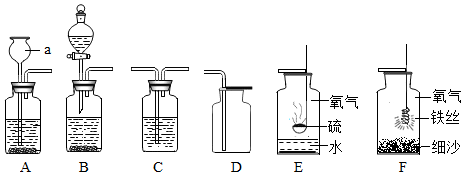
(1)写出仪器a的名称分液漏斗,装置A和D组合可用于实验室制备二氧化碳气体,写出该反应的化学方程式CaCO3+2HCl=CaCl2+CO2↑+H2O,用装置B代替A的优点是可以随时控制反应的发生和停止.
(2)实验装置E的集气瓶中预先加入了少量水,其作用是吸收反应生成的二氧化硫.
(3)通过E、F两个实验,结合课堂学习,你认为在“集气瓶中进行燃烧的实验”应该注意的问题是(说出一点即可)防止炸裂集气瓶.
分析 (1)根据实验室常用仪器解答;根据实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳; 不同的实验装置,功能不同;
(2)二氧化硫有毒,是一种污染环境的物质.
(3)在集气瓶中进行燃烧实验时,要注意防止环境污染,防止安全事故的发生.
解答 解:
(1)根据实验室常用仪器可知:a分液漏斗;二氧化碳能够溶于水,不能用排水法收集,密度比空气大,可以用向上排空气法收集,即用D装置收集;
该反应的化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O;
若用C装置代替B装置进行实验,优点为:可以随时控制反应的发生和停止;
(2)硫在氧气中燃烧生成二氧化硫,二氧化硫能和水反应生成亚硫酸,加入水的目的是吸收二氧化硫,防止污染环境.
(3)在“集气瓶中进行燃烧的实验”时应该注意:要防止生成物污染环境,要防止炸裂集气瓶.
答案:
(1)分液漏斗;二氧化碳;CaCO3+2HCl=CaCl2+CO2↑+H2O;可以随时控制反应的发生和停止;
(2)吸收反应生成的二氧化硫;
(3)防止炸裂集气瓶
点评 本题主要考查仪器的用途、反应表达式的书写,实验装置的选择,选择发生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气体的水溶性、能否和水发生化学反应、密度、能否和空气中的物质发生化学反应等因素.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
10.甲和乙在一定条件下反应生成丙和丁,结合微观示意图分析,下列结论正确的是( )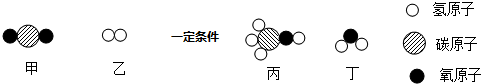

| A. | 该反应是置换反应 | |
| B. | 反应前后分子总数不变 | |
| C. | 发生反应的甲和乙的质量比为22:3 | |
| D. | 反应前后各元素的化合价不发生变化 |
5.最近科学家成功制备出了一种含铱(Ir)和氧两种元素的阳离子,在这种离子中铱元素显+9价,该离子的符号是( )
| A. | IrO4+ | B. | IrO5+ | C. | IrO3+ | D. | IrO2+ |