题目内容
18.某学习小组设计分离NaCl和CaCl2两种固体混合物方案如下: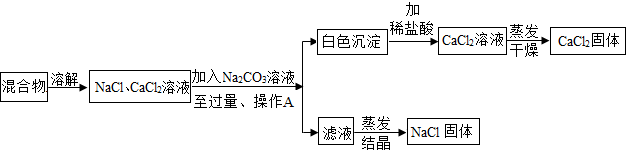
(1)操作A是过滤.
(2)蒸发氯化钙溶液过程中需要用到的仪器除蒸发皿、烧杯、铁架台(带铁圈)、酒精灯、火柴外,还必须要有的一种仪器是玻璃棒.
(3)有同学提出滤液中含有少量的碳酸钠,应加入稀盐酸至过量,再蒸发结晶才能得到纯净的氯化钠.
分析 根据反应流程图分析可知:分离NaCl和CaCl2两种固体混合物,可采取溶解后加入过量碳酸钠溶液,生成碳酸钙沉淀和氯化钠,然后通过过滤将碳酸钙和氯化钠溶液分离;碳酸钙和盐酸发生反应得到氯化钙溶液,经蒸发可得到氯化钙固体;由于碳酸钠过量,所以滤液中的物质有氯化钠和碳酸钠,因此要得到纯净的氯化钠就需要除去碳酸钠,加入稀盐酸最合适,碳酸钠和稀盐酸生成氯化钠和水和二氧化碳,盐酸中的溶质是氯化氢气体,蒸发时氯化氢挥发出去,蒸发后最后的固体物质是氯化钠.(1)NaCl和CaCl2混合物样品加入过量的碳酸钠溶液,氯化钠不反应,氯化钙和碳酸钠反应生成碳酸钙白色沉淀和氯化钠,通过操作A固体和液体分离开来,因此操作A是过滤;
(2)根据蒸发操作需要的仪器分析;
(3)通过A过滤后的滤液中含有氯化钠和过量的碳酸钠,因此可加适量稀盐酸除去过量的碳酸钠;
解答 解:(1)NaCl和CaCl2混合物样品加入过量的碳酸钠溶液,氯化钠不反应,氯化钙和碳酸钠反应生成碳酸钙白色沉淀和氯化钠,其化学方程式是:Na2CO3+CaCl2═CaCO3↓+2NaCl;通过操作A固体和液体分离开来,因此操作A是过滤;故填:过滤;
(2)蒸发过程中需要用到的仪器除蒸发皿、烧杯、铁架台(带铁圈)、酒精灯、火柴外,还必须要有的一种仪器是玻璃棒,玻璃棒的作用是搅拌,使液体受热均匀,防止液滴飞溅;故填:玻璃棒;
(3)通过A过滤后的滤液中含有氯化钠和过量的碳酸钠,要得到氯化钠,应该加入的试剂是稀盐酸,作用是除去过量的碳酸钠;故填:稀盐酸;
故答案为:
(1)过滤;(2)玻璃棒;(3)稀盐酸.
点评 考虑过滤是分离固体和液体的一种方法,解答此类题目时,要认真分析实验目的和反应流程图,明确加入的试剂和发生的化学反应才能正确解答.

(1)配制硫酸铜溶液常常用到胆矾晶体,它的化学式为CuSO4•5H2O.
(2)农业上配制成的波尔多液不能用金属铝罐盛放,试用化学方程式进行解释.2Al+3CuSO4=Al2(SO4)3+3Cu
(3)测量人体血液密度的方法是:在几只试管内分别装有密度不同的硫酸铜溶液,然后向每支试管中分别滴入一滴血液,分析人员只要看到某个玻璃管中的血液呈悬浮状态就能知道血液的密度.
(4)下图是某同学为测定胆矾中结晶水质量分数的主要实验步骤示意图:
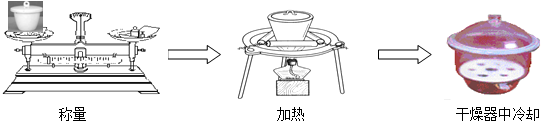
实验中称量得到如下数据:
| 加热前坩埚的质量/g | 加热后坩埚的总质量/g | |
| m1(坩埚) | m2(坩埚+晶体) | m3 |
A.加热后坩埚放在空气中冷却 B.加热时搅拌不当使晶体溅出坩埚外
C.加热温度过高,最终坩埚中固体部分变黑 D.晶体尚带蓝色,即停止加热.
| A. | 氯化钠 食盐 NaCl | B. | 氢氧化钠 纯碱 Na2CO3 | ||
| C. | 硫酸铜晶体 胆矾 CuSO4 | D. | 碳酸钙 生石灰 Ca(OH)2 |
| A. | KNO3+Na2SO4═K2SO4+NaNO3 | |
| B. | ZnSO4+2Ag═Ag2SO4+Zn | |
| C. | 氯化铁溶液中加入氢氧化钠有蓝色絮状沉淀产生 | |
| D. | 把熟石灰放入硫酸铵溶液中有有气泡产生 |
 向一定量的碳酸钾溶液中缓慢滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中离子数目也相应地发生变化.如图所示,四条曲线与溶液中的离子的对应关系,完全正确的( )
向一定量的碳酸钾溶液中缓慢滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中离子数目也相应地发生变化.如图所示,四条曲线与溶液中的离子的对应关系,完全正确的( )| a | b | c | d | |
| A | Cl- | K+ | CO32- | HCO3- |
| B | K+ | CO32- | HCO3- | Cl- |
| C | K+ | CO32- | Cl- | HCO3- |
| D | K+ | HCO3- | Cl- | CO32- |
| A. | A | B. | B | C. | C | D. | D |