题目内容
8.“端午节”前,质监部门对市场上的粽叶进行专项检查时,发现有些颜色翠绿的粽叶是用硫酸铜溶液浸泡的,人吃了用这种粽叶包的粽子,严重影响身体健康.但硫酸铜在农业上可用于配制农药--波尔多液.可见,合理利用化学物质可以造福于人类,反之则会给人类带来危害.请回答:(1)配制硫酸铜溶液常常用到胆矾晶体,它的化学式为CuSO4•5H2O.
(2)农业上配制成的波尔多液不能用金属铝罐盛放,试用化学方程式进行解释.2Al+3CuSO4=Al2(SO4)3+3Cu
(3)测量人体血液密度的方法是:在几只试管内分别装有密度不同的硫酸铜溶液,然后向每支试管中分别滴入一滴血液,分析人员只要看到某个玻璃管中的血液呈悬浮状态就能知道血液的密度.
(4)下图是某同学为测定胆矾中结晶水质量分数的主要实验步骤示意图:
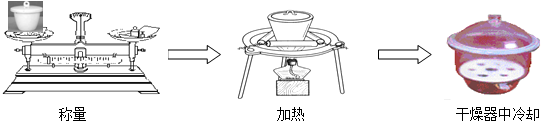
实验中称量得到如下数据:
| 加热前坩埚的质量/g | 加热后坩埚的总质量/g | |
| m1(坩埚) | m2(坩埚+晶体) | m3 |
A.加热后坩埚放在空气中冷却 B.加热时搅拌不当使晶体溅出坩埚外
C.加热温度过高,最终坩埚中固体部分变黑 D.晶体尚带蓝色,即停止加热.
分析 (1)考虑硫酸铜晶体的化学式为CuSO4•5H2O;
(2)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可;
(3)考虑浮力和重力的关系;
(4)根据质量的变化求出生成的水的质量,在求出结晶水含量.
解答 解:(1)硫酸铜晶体的化学式为CuSO4•5H2O,
(2)铝的活动性比铜强,铝和硫酸铜反应会生成硫酸铝溶液和铜,不能用铝制容器配制波尔多液,反应的化学方程式为:2Al+3CuSO4=Al2(SO4)3+3Cu;
(3)根据浮力和重力,结合G=F浮;则ρ物gv=ρ液gv,故ρ物=ρ液,故分析人员只要看到某个玻璃管中的血液呈悬浮状态就能知道血液的密度.
(4)由表中的数据可知,该样品中结晶水的质量分数的计算公式可表示为:w(H2O)=$\frac{{m}_{2}{-m}_{3}}{{m}_{2}-{m}_{1}}$或100$\frac{{m}_{2}{-m}_{3}}{{m}_{2}-{m}_{1}}$%;
实验过程中,下列操作会使结晶水的质量分数w(H2O)计算值偏小的是:
A.加热后坩埚放在空气中冷却,会吸收空气中的水重新形成晶体;
B.加热时搅拌不当使晶体溅出坩埚外,不会影响;
C.加热温度过高,最终坩埚中固体部分变黑,硫酸铜分解,不会影响水的多少;
D.晶体尚带蓝色,即停止加热,结晶水没有完全分解.
故选AD.
故答案为:
(1)CuSO4•5H2O.(2)2Al+3CuSO4=Al2(SO4)3+3Cu
(3)悬浮.(4)$\frac{{m}_{2}{-m}_{3}}{{m}_{2}-{m}_{1}}$或100$\frac{{m}_{2}{-m}_{3}}{{m}_{2}-{m}_{1}}$%; AD.
点评 本题考查了硫酸铜晶体的制备方案的设计,涉及铜及其化合物的性质应用,化学实验基本操作,误差的分析等知识.

 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案关注食品安全,购买前请认真阅读食品标签.下表是某品牌钙奶包装袋上的部分内容.
| 品名 | XX牌钙奶饼干 |
| 配料 | 小麦粉、白砂糖、花生油含(维生素E)鲜鸡蛋、奶粉、食品添加剂(碳酸氢铵碳酸氢钠碳酸钙蛋白酶) |
| 保质期 | 8个月 |
| 生产日期 | 2015年10月22 |
①主要提供蛋白质的物质有鲜鸡蛋、奶粉,能提供人体主要供能物质的有小麦粉、白砂糖.
②检验饼干中含有淀粉的方法是取样,滴加碘液,如果变成蓝色,说明饼干中含有淀粉.
(2)配料中的食品添加剂
①碳酸氢钙的作用是使饼干蓬松,烘焙时发生反应的化学方程式是2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
②老年人缺钙会导致骨质疏松症,配料中碳酸钙能提供钙(填“单质”“分子”“元素”)元素.
(3)结合生产日期保质期,最好在保质期内食用完.
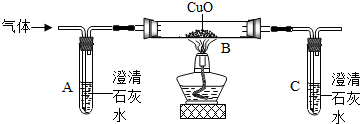 不少同学都被蚊虫叮咬过,感觉又痛又痒.同学们从化学课上知道:蚊虫叮咬时能在人的皮肤内分泌出蚁酸 CH2O2刺激皮肤.课外兴趣小组同学决定对蚁酸进行探究.
不少同学都被蚊虫叮咬过,感觉又痛又痒.同学们从化学课上知道:蚊虫叮咬时能在人的皮肤内分泌出蚁酸 CH2O2刺激皮肤.课外兴趣小组同学决定对蚁酸进行探究.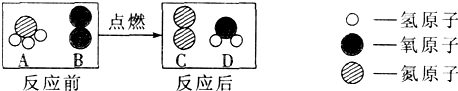
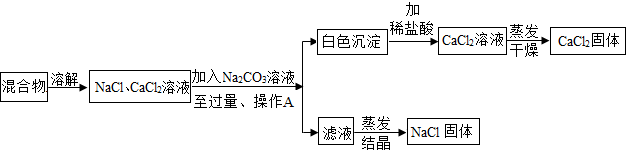
 小敏同学在实验室中制取CO2气体,为对废液进行后续探究,他向一定质量的含CaCl2和HCl的溶液中逐滴加入溶质质量分数为10%的Na2CO3溶液.实验过程中加入Na2CO3溶液的质量与溶液的pH变化关系如图所示,那么hk段出现的实验现象为产生白色沉淀,在K点的溶液中的溶质为NaCl.
小敏同学在实验室中制取CO2气体,为对废液进行后续探究,他向一定质量的含CaCl2和HCl的溶液中逐滴加入溶质质量分数为10%的Na2CO3溶液.实验过程中加入Na2CO3溶液的质量与溶液的pH变化关系如图所示,那么hk段出现的实验现象为产生白色沉淀,在K点的溶液中的溶质为NaCl.