题目内容
19.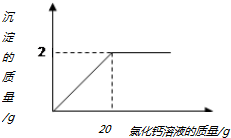 小林在做实验时发现,实验室的纯碱样品中混入了少量的食盐,为测定该纯碱样品中碳酸钠的含量,小明称取该纯碱样品2.5g,再滴加氯化钙溶液至不再产生沉淀,产生沉淀的质量与加入氯化钙溶液的质量关系如图所示
小林在做实验时发现,实验室的纯碱样品中混入了少量的食盐,为测定该纯碱样品中碳酸钠的含量,小明称取该纯碱样品2.5g,再滴加氯化钙溶液至不再产生沉淀,产生沉淀的质量与加入氯化钙溶液的质量关系如图所示求:
(1)该纯碱样品中碳酸钠的质量分数
(2)反应后所得溶液的溶质质分数(精确到0.1%)
分析 (1)欲求该纯碱样品中碳酸钠的质量分数,须先根据化学方程式求出样品中碳酸钠的质量,再利用质量分数公式计算即可.
(2)欲求反应后所得溶液的溶质质分数,须先根据化学方程式求出溶质的质量,再根据溶质质量分数的计算公式进行计算即可.
解答 解:设该纯碱样品中碳酸钠的质量为x,生成氯化钠的质量为y,则
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100 117
x 2.0g y
$\frac{106}{x}$=$\frac{100}{2.0g}$=$\frac{117}{y}$
解之得:x=2.12g,y=2.34g;
所以,该纯碱样品中碳酸钠的质量分数为:$\frac{2.12g}{2.5g}$×100%=84.8%;
反应后所得溶液的溶质质分数$\frac{2.34g+(2.5g-2.12g)}{2.5g+20g-2g}$×100%=13.3%;
答:(1)该纯碱样品中碳酸钠的质量分数为84.8%;
(2)所加入氯化钙溶液的溶质质量分数为13.3%.
点评 本题主要考查学生对完全反应的概念的认识,以及运用化学方程式和质量分数公式进行计算的能力.

练习册系列答案
相关题目
14.下列有关分子、原子、离子的叙述正确的是( )
| A. | 决定原子质量大小的主要是质子和电子 | |
| B. | 带电的微粒一定是离子 | |
| C. | 分子是保持物质性质的-种粒子 | |
| D. | 分子、原子、离子都能直接构成物质 |
4.蜡烛燃烧实验,证明蜡烛燃烧生成( )
| A. | 水 | B. | 氧气 | C. | 水和氧气 | D. | 水和二氧化碳 |